Clear Sky Science · ru
Реактивные формы кислорода (ROS) при раке: от механизмов к терапевтическим выводам
Когда полезные молекулы становятся опасными
Внутри каждой клетки постоянно образуются крошечные химические искры — реактивные формы кислорода, или ROS — в рамках нормального жизнедеятельности. В подходящих концентрациях они помогают клеткам расти, взаимодействовать и защищаться от микробов. Но этот обзор объясняет, как те же молекулы могут повреждать ДНК, искажать клеточные сигнальные сети и способствовать росту, распространению и лекарственной устойчивости рака. Понимание этой «двойной жизни» ROS помогает учёным разрабатывать новые противораковые стратегии, которые либо смягчают вредный окислительный стресс, либо намеренно усиливают его, чтобы уничтожить опухолевые клетки.
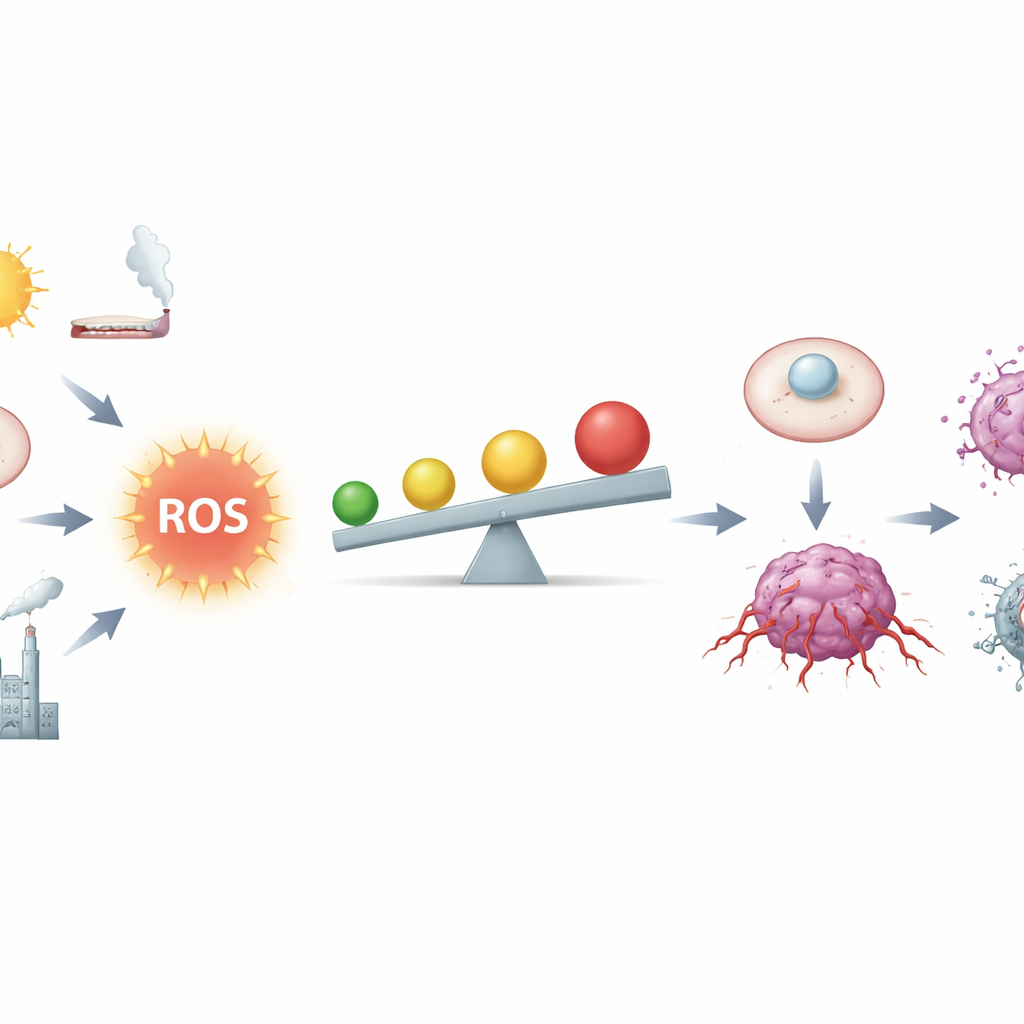
Тонкая грань между топливом и огнём
Авторы описывают ROS как химические побочные продукты дыхания и метаболизма, а также как мощные посредники сигналов. В здоровых тканях низкие уровни ROS помогают контролировать клеточный цикл, восстанавливать повреждения и тонко настраивать иммунитет. Клетки удерживают эти сигналы под контролем с помощью сложной антиоксидантной сети, включающей молекулы вроде глутатиона и ферменты под управлением ключевого фактора Nrf2. Раковые клетки, однако, живут ближе к зоне риска: дефектные гены, перегруженные митохондрии, хроническое воспаление, табачный дым, радиация и некоторые металлы повышают уровень ROS. При умеренно высоких концентрациях ROS они могут повреждать ДНК, дестабилизировать хромосомы и постоянно активировать сигнальные цепи роста и выживания, облегчая превращение нормальной клетки в злокачественную.
Как оксидативный стресс формирует поведение опухоли
После установления опухоли ROS продолжают определять её биологию. Умеренный оксидативный стресс активирует многие пути роста, которые побуждают клетки делиться, формировать сосуды, внедряться в соседние ткани и выдерживать химиотерапию. ROS могут перепрограммировать использование сахаров, жиров и аминокислот, направляя метаболизм в пути, которые увеличивают производство антиоксидантов и строительных блоков для новых клеток. Они также влияют на решения о судьбе клетки: в зависимости от интенсивности и контекста ROS могут склонять баланс в сторону сигналов выживания или в сторону различных программированных форм гибели, включая классическую апоптозу и более новые формы вроде ферроптоза, некроптоза и купроптоза. Это делает ROS одновременно соучастниками прогрессирования опухоли и потенциальными триггерами её самоуничтожения.
Перепрограммирование иммунитета и ответа на лекарства
В обзоре подчёркивается, что ROS действуют не только внутри раковых клеток — они перестраивают и микроокружение опухоли. Высокий оксидативный стресс может истощать или убивать Т‑клетки и натуральные киллеры, борющиеся с опухолью, в то время как способствует появлению супрессивных клеток, защищающих опухоль от атак. ROS также помогают опухолям повышать экспрессию «не убивайте меня» сигналов, таких как контрольные белки (checkpoint), снижая эффективность иммуннотерапии. Одновременно умеренные уровни ROS могут стимулировать лекарственную устойчивость, усиливая насосы выведения препаратов и стресс‑ответы, что позволяет раковым клеткам выбрасывать химиопрепараты или восстанавливать вызванные ими повреждения. Тем не менее в других условиях доведение ROS выше критического порога может разрушить эти защиты и вернуть опухоли чувствительность к лечению.
Преобразование редокс‑слабостей в терапевтическую стратегию
Поскольку раковые клетки балансируют между использованием ROS и их отравляющим действием, авторы рассматривают управление редокс‑балансом как рычаг терапии. Одна широкая стратегия — снижать вредные ROS или укреплять антиоксиданты, в основном для профилактики или защиты здоровых тканей во время лечения. Другая — делать обратное в опухолях: ингибировать антиоксидантные системы или усиливать продукцию ROS до тех пор, пока раковые клетки не переступят летальную грань, особенно в сочетании с радиацией, таргетной терапией или иммуннотерапией. Третий подход — не менять уровни ROS напрямую, а блокировать конкретные ROS‑чувствительные переключатели — сигнальные белки, метаболические ферменты или пути гибели, на которые опираются опухоли. Сквозь все эти идеи проходит тема персонализации: разные раки имеют разные «редокс‑подписи», поэтому будущие терапии, возможно, потребуют анализов крови или тканей на оксидативные повреждения, антиоксидантный потенциал и гены, связанные с ROS, чтобы выбрать подходящее редокс‑направленное лечение для каждого пациента.
Что это значит для пациентов
Проще говоря, в статье делается вывод, что ROS не являются исключительно плохими или исключительно хорошими; это мощные инструменты, которыми пользуются клетки и опухоли. Раковые клетки, как правило, функционируют ближе к порогу оксидативного стресса, чем здоровые клетки, что может создать терапевтическое окно. Однако поскольку антиоксиданты и прооксиданты могут помогать или вредить в зависимости от дозы, времени и типа опухоли, бездумный приём добавок или препаратов, усиливающих ROS, рискован. Авторы приходят к выводу, что будущее — за тщательно разработанными терапиями и диагностикой, которые оценивают редокс‑состояние каждой опухоли и затем аккуратно регулируют ROS и антиоксидантные системы — либо вниз, чтобы защитить нормальные ткани, либо вверх, чтобы довести раковые клетки до предела их выносливости.
Цитирование: Akter, S., Madhuvilakku, R., Kar, A.K. et al. Reactive oxygen species (ROS) in cancer: from mechanism to therapeutic implications. Sig Transduct Target Ther 11, 111 (2026). https://doi.org/10.1038/s41392-026-02583-x
Ключевые слова: реактивные формы кислорода, окислительный стресс, метаболизм рака, редокс-терапия, микроокружение опухоли