Clear Sky Science · ru
Консенсусные молекулярные подтипы плоскоклеточного рака пищевода
Почему это исследование важно для пациентов
Плоскоклеточный рак пищевода — смертоносная опухоль с ограниченным набором индивидуализированных вариантов лечения и в целом неблагоприятным прогнозом. Врачи знают, что опухоли ведут себя по‑разному, но до сих пор не существовало единой, общепринятой схемы, позволяющей разделить эти раки на биологически значимые группы. В этом исследовании объединены разнообразные данные генетики и визуализации, определяющие четыре основных типа этого рака, и показано, что зачастую по простому изображению со слайда под микроскопом можно распознать тип пациента. Это открывает путь к более точному лечению с меньшим количеством проб и ошибок.
Приведение в порядок запутанной картины болезни
За последнее десятилетие разные исследовательские коллективы предложили по крайней мере семь способов классификации этого рака на основе мутаций ДНК, изменений числа копий генов, активности генов и других молекулярных показателей. Каждая система опиралась на разные данные и методы, в результате чего подтипы пересекались, но не совпадали, что усложняло их клиническое применение. Авторы сначала повторно проанализировали хорошо охарактеризованную когорту из 152 китайских пациентов, для которых были доступны многослойные данные, включая секвенирование всего генома, экспрессию генов, метилирование ДНК и профили микроРНК. С помощью метода, называемого слиянием сетей сходства (similarity network fusion), они объединили все эти данные в единую картину и выделили четыре мультиомных подтипа. Затем они построили статистическую «сеть подтипов», связав свои новые группы с 21 ранее опубликованной классификацией, что выявило сильные связи между исследованиями.
Четыре основные биологические «личности» опухоли
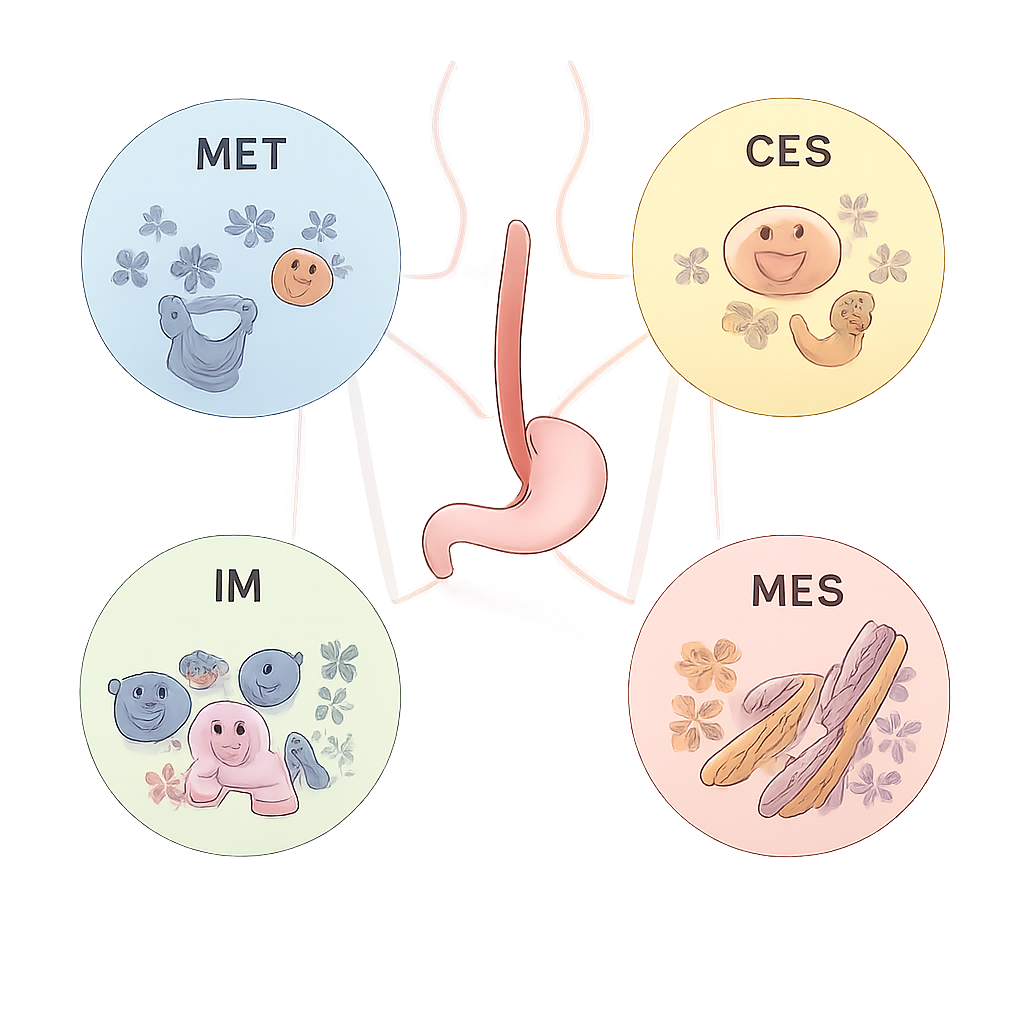
Из этой сети команда выделила четыре консенсусных молекулярных подтипа, названные ECMS1–ECMS4, каждый со своими отличительными свойствами. ECMS1, метаболический тип (MET), демонстрирует повышенную активность путей, обрабатывающих лекарственные и питательные вещества, и частую активацию гена NFE2L2, что может способствовать устойчивости к химио‑ и радиотерапии. ECMS2, классический тип (CLS), характеризуется выраженной активностью клеточного цикла и ростовых сигналов и часто имеет увеличение числа копий гена ERBB2 (HER2). ECMS3, иммунный тип (IM), имеет меньшую суммарную мутационную нагрузку, но сильную активацию иммунной системы, включая высокую активность пути PD‑1. ECMS4, мезенхимальный тип (MES), демонстрирует признаки ремоделирования тканей, роста сосудов и тенденцию клеток к повышенной подвижности и инвазивности — черты, связанные с худшим прогнозом.
Связь подтипов с прогнозом и выбором лечения
Сопоставление этих четырех групп с клиническими данными пациентов выявило четкие закономерности. Пациенты с мезенхимальными опухолями ECMS4 имели наивысший риск рецидива и худшие общую и безрецидивную выживаемость. Иммунный ECMS3, несмотря на активную иммунную среду, плохо отвечал на стандартную химиолучевую терапию, но показал более высокий уровень пользы от против PD‑1 иммунотерапии. Классические ECMS2 опухоли выглядели более чувствительными к распространенным химиопрепаратам, таким как цисплатин и таксаны, а частая амплификация HER2 указывает на возможность пользы от HER2‑таргетной терапии. Метаболические ECMS1 опухоли, обогащенные активностью NFE2L2 и определенных рецепторов факторов роста, могут лучше реагировать на препараты, нацеленные на метаболические и сигнальные пути. Вкратце, четыре подтипа предполагают разные уязвимые места и разные вероятные ответы на лечение.
Обучение компьютера видеть молекулярные подсказки на рутинных слайдах
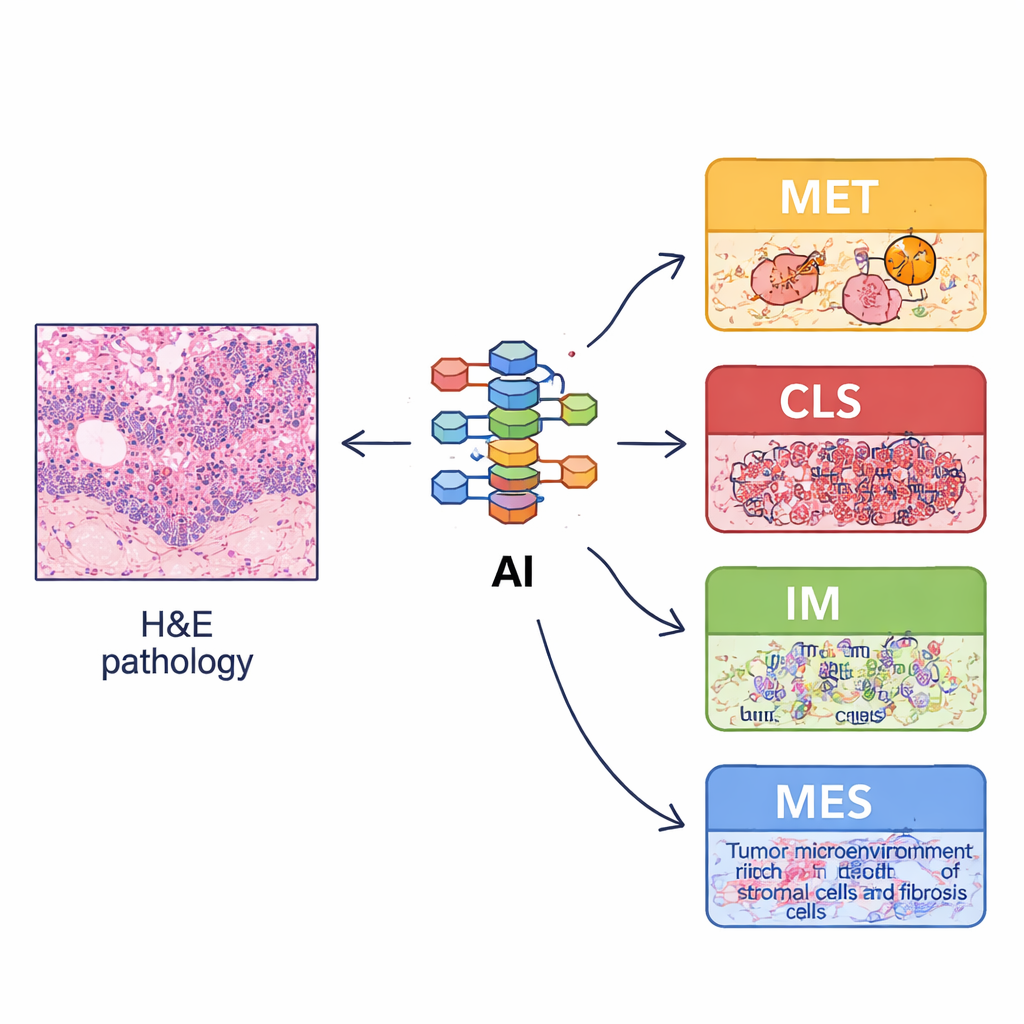
Поскольку полноценное молекулярное профилирование дорого и недоступно во многих больницах, команда выяснила, могут ли обычные гематоксилин‑эозиновые (H&E) слайды служить прокси. Они обучили систему глубокого обучения на десятках тысяч аннотированных фрагментов изображений для распознавания базовых тканевых компонентов: опухолевых клеток, стромы, лимфоцитов, желез и мышечной ткани. По целым слайдам затем вычислялись «признаки пространственной организации» — сколько каждого типа ткани присутствует, как они расположены и насколько смешаны или разделены. Эти паттерны, выведенные из изображений, отражали биологию четырех подтипов: например, иммунный ECMS3 демонстрировал больше лимфоцитов и сохраняющихся нормальных структур, тогда как мезенхимальный ECMS4 — больше поддерживающей стромы. Используя эти признаки, они создали образный классификатор imECMS, который мог с хорошей точностью в нескольких независимых когортах относить слайды к MET, CLS, IM или MES.
Что это значит для будущего помощи пациентам
Для неспециалистов вывод в том, что это исследование преобразует казавшийся однородным рак в четыре биологически различных заболевания, каждое со своей вероятной траекторией и оптимальными стратегиями лечения. Еще важнее то, что большую часть этой информации можно автоматически извлечь из стандартных микроскопических изображений, которые уже есть у каждого пациента, без необходимости дорогостоящего секвенирования. При дальнейшем подтверждении в более крупных и разнообразных популяциях системы ECMS и imECMS могли бы помочь врачам подобрать пациентам с плоскоклеточным раком пищевода те терапии, от которых они с наибольшей вероятностью получат пользу, и оградить их от неэффективных методов лечения.
Цитирование: Cui, H., Zhu, Z., Xu, E. et al. The consensus molecular subtypes of esophageal squamous cell carcinoma. Sig Transduct Target Ther 11, 65 (2026). https://doi.org/10.1038/s41392-026-02577-9
Ключевые слова: рак пищевода, подтипы опухолей, персонализированная онкология, патология с глубоким обучением, иммунотерапия