Clear Sky Science · ru
Гиперглутаминолиз ускоряет сенесценцию и старение через активацию оси аргинин–mTORC1
Почему это исследование важно для здорового старения
Старение — это не только морщины и седые волосы: это процесс, при котором клетки по всему телу постепенно теряют способность восстанавливаться и обновляться. В этом исследовании задают на первый взгляд простой, но важный вопрос: способствует ли способ утилизации аминокислоты глутамина тем самым сдвигам в клетках, которые ведут к старению? Авторы открывают ранее неописанную метаболическую цепочку, связывающую переработку глутамина с мощным регулятором роста mTORC1, и показывают, что чрезмерная активация этого пути может активно ускорять клеточное старение у дрозофил и мышей.
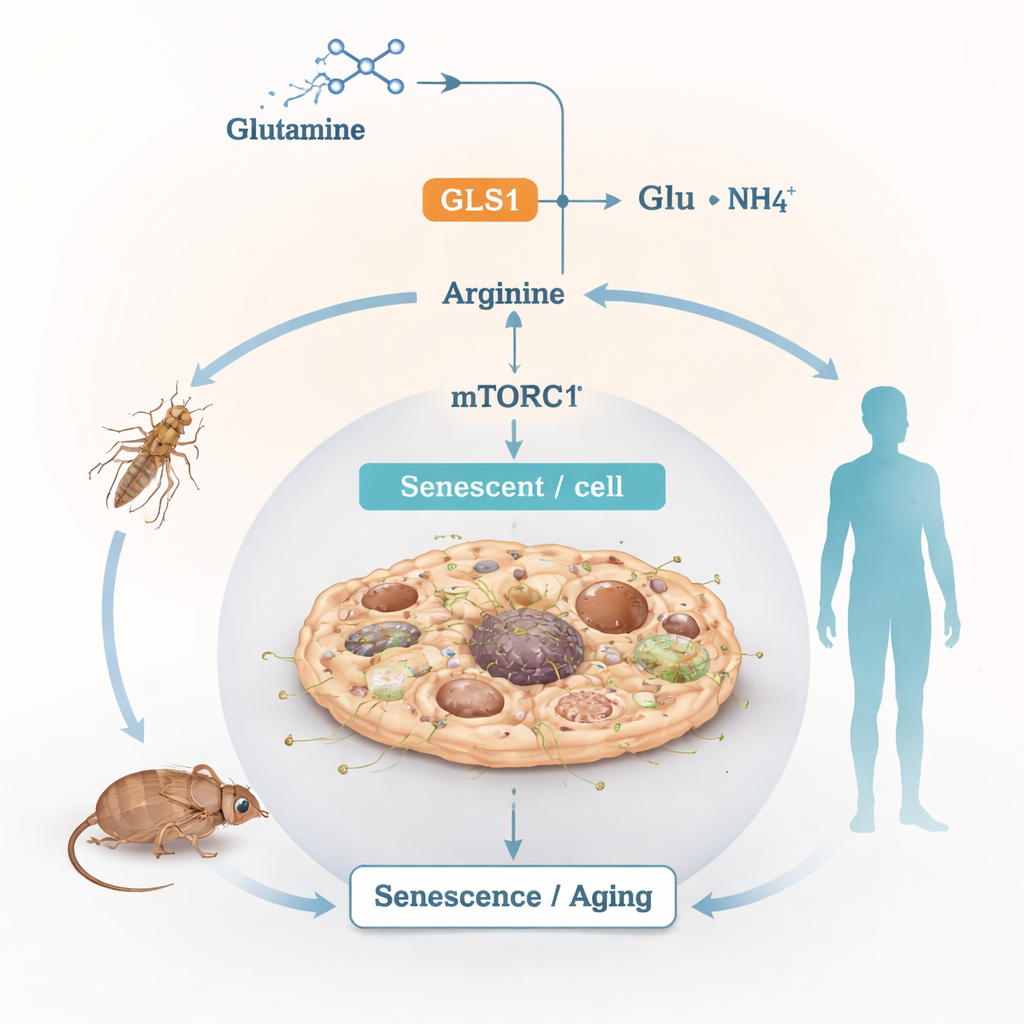
Трубопровод топлива, работающий слишком жарко
Глутамин — самая распространённая свободная аминокислота в крови и тканях. Клетки используют его и как универсальное топливо, и как строительный блок, расщепляя в процессе, называемом глутаминолизом. Первый шаг катализирует фермент GLS1, который превращает глутамин в глутамат и аммоний; далее продукты включаются в выработку энергии, антиоксидантную защиту и синтез других аминокислот. Хотя такое расщепление необходимо для нормальной жизни, авторы заинтересовались, что происходит, когда этот процесс хронически гиперактивен в условиях старения и стресса.
Обнаружение «гиперглутаминолиза» в старых клетках и организмах
С помощью углублённого профилирования метаболитов команда сравнила молодые делящиеся клетки и сенесцентные клетки — старые клетки, переставшие делиться и выделяющие провоспалительные факторы. Они обнаружили повышение многих аминокислот, с глутамином в центре перестроенной сети. Сенесцентные клетки потребляли больше глутамина, имели повышенные уровни и активность GLS1 и накапливали больше глутамата и аммония. Похожие изменения выявлены и в целом организме: у пожилых плодовых мушек и старых мышей повышалась активность GLS в нескольких тканях. Авторы назвали это общее состояние усиленного расщепления глутамина «гиперглутаминолизом», полагая, что это консервативная черта старения, а не незначительный побочный эффект.
Снижение расщепления глутамина замедляет признаки старения
Если гиперглутаминолиз сопутствует старению, то является ли он движущей силой? Чтобы проверить это, исследователи блокировали глутаминолиз разными способами: снижая глутамин в среде культивирования, ингибируя GLS фармпрепаратами или генетически уменьшая экспрессию GLS1. В стрессовых или репликативно постаревших клетках эти вмешательства сокращали классические маркёры сенесценции — покраску SA-β-gal, ингибитор клеточного цикла p16 и провоспалительные сигналы SASP. У дрозоф генетическое подавление GLS или приём низких доз ингибитора GLS увеличивали продолжительность жизни, улучшали способность к лазанию (тест физической активности) и снижали возрастную проницаемость кишечника. Важно, что при ограничении глутаминолиза с самого начала воздействия стресса эффект объяснялся не преимущественным отмиранием старых клеток, а предотвращением их перехода в состояние сенесценции.
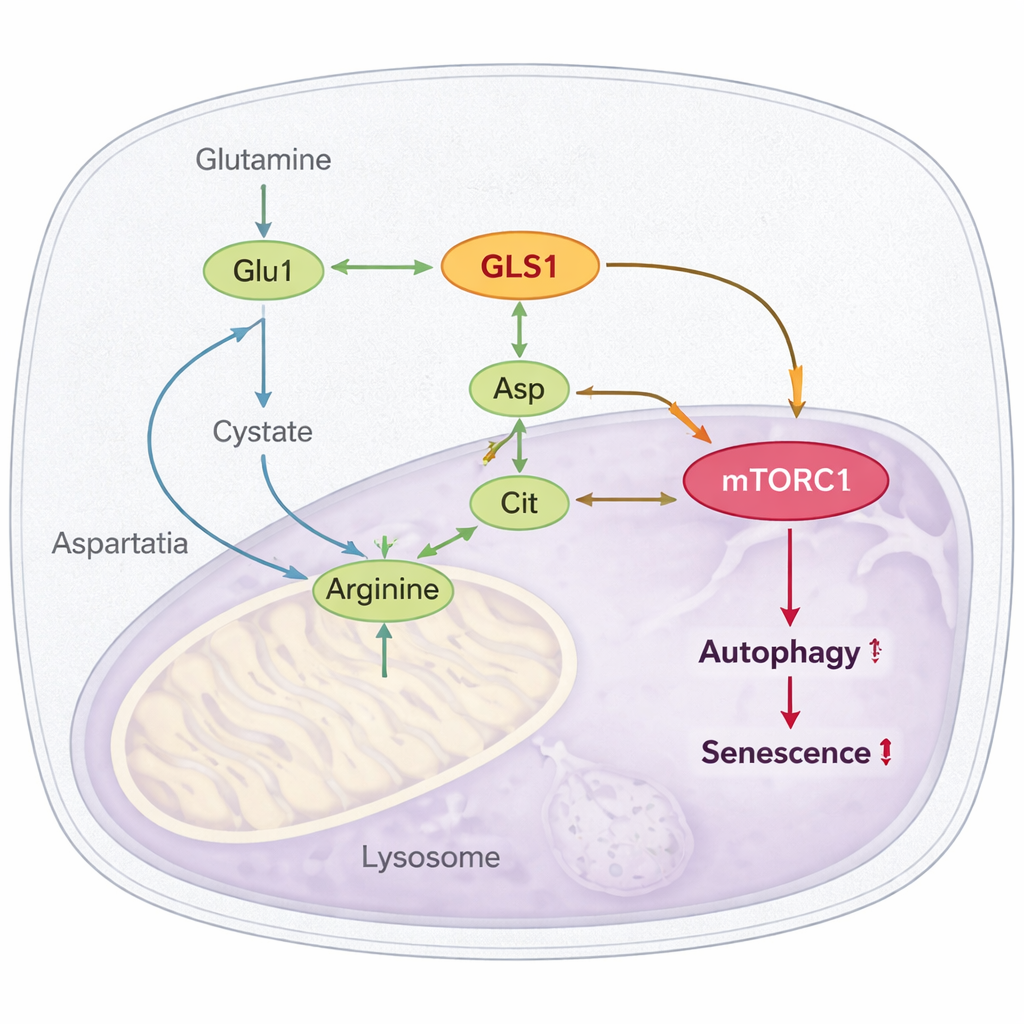
Скрытая цепь: от глутамина к аргинину и mTORC1
Самое примечательное открытие — как этот гиперактивный путь подключается к mTORC1, главному регулятору, который при хронической активации известен как фактор, способствующий старению и блокирующий клеточный «уборочный» процесс (аутофагию). Авторы показывают, что гиперглутаминолиз усиливает производство аргинина — другой аминокислоты, напрямую активирующей mTORC1. Глутамат и аммоний, образующиеся из глутамина, идут на синтез аспартата и цитруллина, которые затем соединяются в аргинин. В старых клетках и у мушек повышаются уровни аргинина и его предшественников; блокада GLS или подавление ключевого фермента синтеза аргинина (ASL) снижает аргинин и ослабляет активность mTORC1. Авторы также показывают, что белок‑сенсор аргинина CASTOR1 необходим для этого эффекта: при инактивированном CASTOR1 блокада глутаминолиза больше не угнетает mTORC1 и не улучшает аутофагию, а облегчение сенесценции исчезает.
Когда избыток полезного ускоряет старение
Чтобы проверить, достаточно ли простого усиления этого пути для ускорения старения клеток, команда подливала здоровым клеткам в течение недель дополнительный глутамин, аргинин или комбинации промежуточных метаболитов. Результат — явный рост маркёров сенесценции и провоспалительных генов. У дрозоф длительное добавление глутамина или аргинина сократило медиану и максимум продолжительности жизни. В совокупности работа описывает полный каскад: избыток расщепления глутамина (гиперглутаминолиз) усиливает синтез аргинина, что фиксируется CASTOR1, поддерживает аномальную активность mTORC1, подавляет клеточную очистку и способствует сенесценции и старению организма.
Что это значит для будущих стратегий против старения
Для неспециалистов это исследование перекалибрует восприятие метаболизма глутамина как палки о двух концах: он необходим для здоровья, но может быть вреден при хроническом гиперстимуле в среднем и пожилом возрасте. Проследив конкретный путь от катаболизма глутамина до гиперактивации mTORC1, авторы выделяют новые точки вмешательства — такие как ферменты GLS1 и ASL или этап распознавания аргинина — которые потенциально можно настроить для замедления возрастного упадка, не закрывая полностью жизненно важные метаболические процессы. Хотя преждевременно переводить эти результаты в диетические рекомендации или терапевтические подходы, работа добавляет важный фрагмент в пазл понимания того, как повседневная переработка питательных веществ может подталкивать наши клетки либо к устойчивости, либо к ускоренному старению.
Цитирование: Chen, H., Huang, N., Xu, W. et al. Hyperglutaminolysis drives senescence and aging through arginine-mTORC1 axis activation. Sig Transduct Target Ther 11, 64 (2026). https://doi.org/10.1038/s41392-026-02576-w
Ключевые слова: метаболизм глутамина, клеточная сенесценция, сигналинг mTORC1, биосинтез аргинина, интервенции при старении