Clear Sky Science · ru
Экзогенный нуклеарный антиген 1 вируса Эпштейна—Барра индуцирует резистентность опухолей к иммунотерапии через ADAR1
Почему обычный вирус важен для лечения рака
Многие виды рака сейчас лечат иммунотерапией, которая мобилизует собственную иммунную систему организма. Тем не менее большинство пациентов по-прежнему не получают пользы, поскольку их опухоли учатся прятаться от иммунной атаки. В этом исследовании показано, как очень распространённый вирус — вирус Эпштейна—Барра (EBV) — помогает опухолям отключать иммунную защиту и становиться устойчивыми к этим мощным препаратам, а также как новый тип конструируемой молекулы может снова вернуть эту защиту в рабочее состояние.
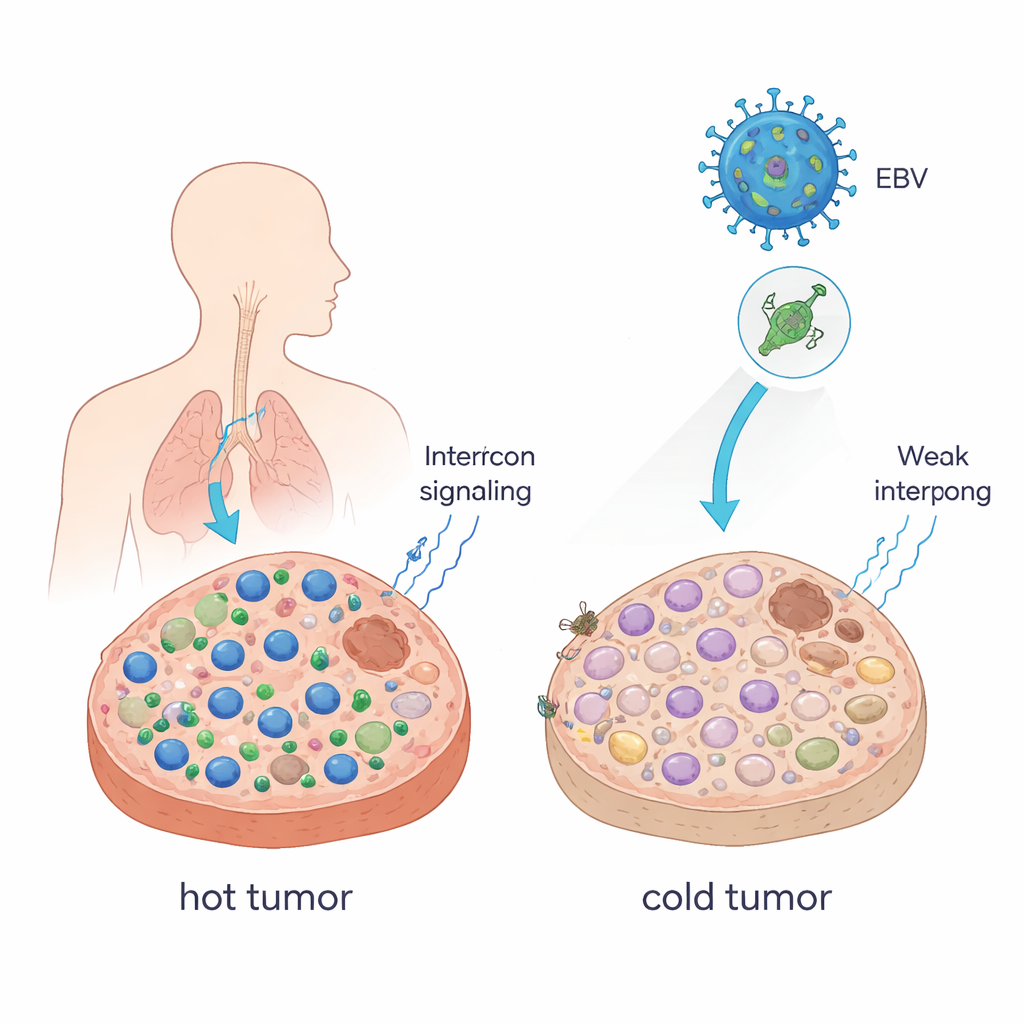
Превращение «горячих» опухолей в «холодные»
Врачи часто называют опухоли «горячими», когда они наполнены Т‑клетками, убивающими раковые клетки, и «холодными», когда этих клеток мало. «Горячие» опухоли обычно хорошо отвечают на блокаду иммунных контрольных точек (ICB), например анти–PD-1‑антитела; «холодные» опухоли часто нет. Авторы показали, что один белок EBV — EBNA1 — способен сместить опухоль в более холодное, уклончивое состояние. Когда они заставляли мышиные опухолевые клетки продуцировать EBNA1 и выращивали их в мышах с интактной иммунной системой, опухоли росли сильнее, содержали меньше CD8+ Т‑клеток и клеток естественного киллерного ответа, а также больше иммуноподавляющих макрофагов. Сигналы интерферонов — ключевые посредники, помогающие мобилизовать иммунные клетки — также были сильно снижены. В образцах пациентов с назофарингеальной карциномой, раком, тесно связанным с EBV, опухоли, экспрессирующие EBNA1, аналогично имели меньше CD8+ Т‑клеток по сравнению с нормальной тканью.
Вирусный кратчайший путь к механизму контроля РНК в клетке
Чтобы понять, как EBNA1 перестраивает опухолевую среду, исследователи искали человеческие белки, которые физически взаимодействуют с ним. Они сосредоточились на белке IGF2BP3, который «читает» небольшие химические метки (m6A) на матричных РНК и может повышать их стабильность или трансляцию в белок. EBNA1 прочно связывался с IGF2BP3 в нескольких типах клеток, включая EBV‑положительные раковые клетки. Данные из опухолей пациентов показали, что высокий уровень IGF2BP3 сопровождался низкой активностью генов, связанных с интерфероном, и меньшей инфильтрацией CD8+ Т‑клеток, что указывает на то, что этот вирусно-хозяинский альянс может ослаблять противоопухолевый иммунитет.
Усиление редактора РНК, который заглушает сигналы опасности
Более глубокий анализ выделил одну ключевую мишень этого взаимодействия: ADAR1, фермент, который редактирует двуцепочечную РНК, изменяя некоторые буквы «A» на «I». Такое редактирование может делать вирусоподобную РНК внутри клеток менее опасной для внутренних датчиков, снижая интерфероновые ответы. Авторы обнаружили, что EBNA1, IGF2BP3 и фактор инициации трансляции EIF4G1 образуют трёхкомпонентный комплекс на мРНК ADAR1. Этот комплекс увеличивает метки m6A, привлекает машинерию трансляции и избирательно повышает продукцию белка ADAR1 без увеличения уровня его РНК. В результате опухолевые клетки выполняют больше редактирования РНК в повторяющихся генетических элементах, расположенных рядом с генами, связанными с интерфероном. Эти правки сокращают пул неотредактированной двуцепочечной РНК, которая обычно бы активировала датчики, такие как MDA5 и PKR, притупляя производство интерферонов и помогая опухолям скрываться от иммунной атаки.
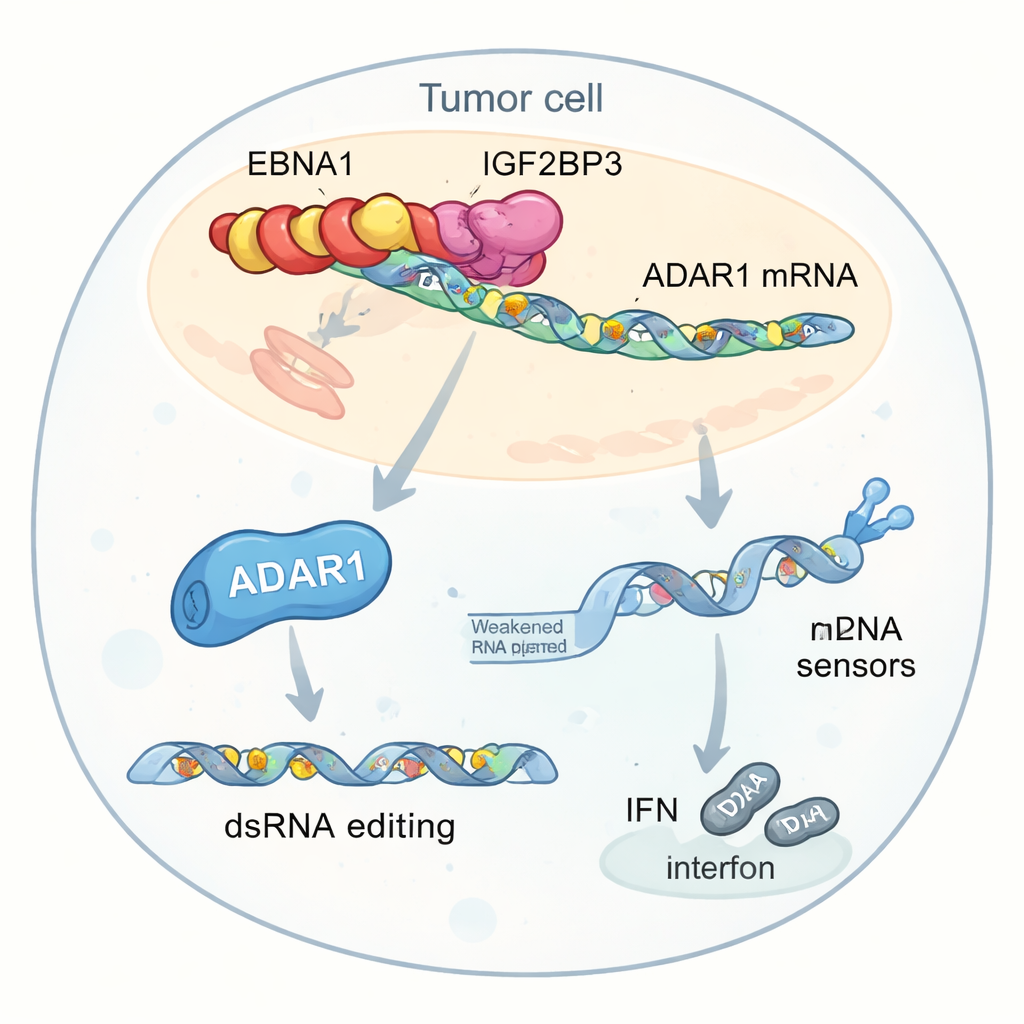
Меньше интерферона — слабее иммунотерапия
Когда опухолевые клетки, экспрессирующие EBNA1, подвергали воздействию Т‑клеток и анти–PD-1‑антител в лаборатории, их было труднее убить по сравнению с контрольными клетками, и они выделяли меньше интерферона. Даже при прямой обработке интерфероном клетки с EBNA1 были менее чувствительны, и их внутренние РНК‑датчики активировались слабее. Снижение уровней ADAR1 частично обращало эти эффекты, восстанавливая активность датчиков и интерфероновое сигнальнование. Генетические и секвенирующие эксперименты подтвердили, что клетки с EBNA1 демонстрировали больше событий A‑to‑I редактирования в специфических областях РНК, особенно после стимуляции интерфероном, что дополнительно подтверждает идею о том, что вирусное усиление ADAR1 помогает нейтрализовать сигналы опасности, которые в противном случае вызвали бы сильные иммунные ответы.
Дизайнерский деградатор, который пробуждает иммунную атаку
Команда затем спросила, можно ли вернуть уязвимость опухолей к иммунотерапии, избавив их от EBNA1. Они спроектировали молекулу PROTAC под названием EP-1215, которая помечает EBNA1 для разрушения системой утилизации клетки. При низких дозах EP-1215 эффективно деградировал EBNA1 и снижал уровни белка ADAR1. В экспериментах на мышах EP-1215 в одиночку имел ограниченный эффект на EBNA1‑положительные опухоли, как и анти–PD-1 сам по себе. Но в комбинации оба лечения резко сокращали опухоли, увеличивали инфильтрацию CD8+ Т‑клеток и увеличивали число Т‑клеток, продуцирующих интерферон. В гуманизированных моделях мышей с человеческими иммунными клетками и EBV‑связанными опухолями комбинация снова превзошла монотерапию, без очевидной токсичности для печени или почек.
Что это значит для будущего ухода за больными раком
Для непрофессионалов смысл в том, что обычный вирус может тихо перенастроить раковые клетки, подавляя внутренние системы оповещения и отключая химические сигналы, которые в противном случае привлекали бы и активировали иммунные клетки. EBNA1 делает это, захватывая читатель m6A (IGF2BP3) и фактор трансляции (EIF4G1), чтобы перепродуцировать редактор РНК ADAR1, который «стирает» именно те структуры РНК, которые предназначены для распознавания иммунными датчиками. Разрушая EBNA1 с помощью нацеленного PROTAC, такого как EP-1215, авторы смогли восстановить эти сигналы опасности и сделать резистентные опухоли вновь восприимчивыми к существующим препаратам, блокирующим контрольные точки. Если аналогичные стратегии окажутся безопасными и эффективными у людей, нацеливание на вирусных «помощников», таких как EBNA1, может предложить новый путь превращения холодных EBV‑связанных опухолей в горячие мишени, на которые современные иммунотерапии смогут эффективно воздействовать.
Цитирование: Liu, C., Sun, Z., Li, C. et al. Exogenous Epstein–Barr virus nuclear antigen 1 induces ADAR1-driven tumor resistance against immunotherapy. Sig Transduct Target Ther 11, 63 (2026). https://doi.org/10.1038/s41392-026-02574-y
Ключевые слова: вирус Эпштейна—Барра, резистентность к иммунотерапии, ADAR1, редактирование РНК, назофарингеальная карцинома