Clear Sky Science · ru
Молекулярный механизм холестерин-зависимого слияния мембран при проникновении SARS-CoV-2
Почему холестерин важен для респираторного вируса
Вирус, вызывающий COVID-19, SARS-CoV-2, проникает в наши клетки путем слияния своей внешней оболочки с мембранами клеток. В этой статье задают на вид простейший, но важный вопрос: насколько холестерин — жироподобное вещество, известное по болезням сердца — влияет на этап слияния? Авторы показывают, что холестерин в вирусной мембране не просто меняет эффективность инфекции; он фактически организует спайк‑белки вируса в мощные «доковые» платформы, которые облегчают и делают проникновение более надежным.
Создание минимальной модели вирусного проникновения
Чтобы прояснить процесс, исследователи воссоздали взаимодействие вируса и клетки в пробирке, используя крошечные жировые пузырьки — липосомы. Один набор липосом нес спайк‑белок SARS-CoV-2 и имитировал вирусную мембрану; другой — рецептор ACE2, имитируя поверхность клетки хозяина. При смешивании и активации специфическими ферментами, «рассекающими» спайк до готовой к слиянию формы, эти искусственные мембраны сливались, позволяя флуоресцентному красителю перейти из одного пузырька в другой. Эта упрощенная система позволила точно регулировать состав липидов — включая уровень холестерина — по обе стороны и пошагово наблюдать за процессом слияния. 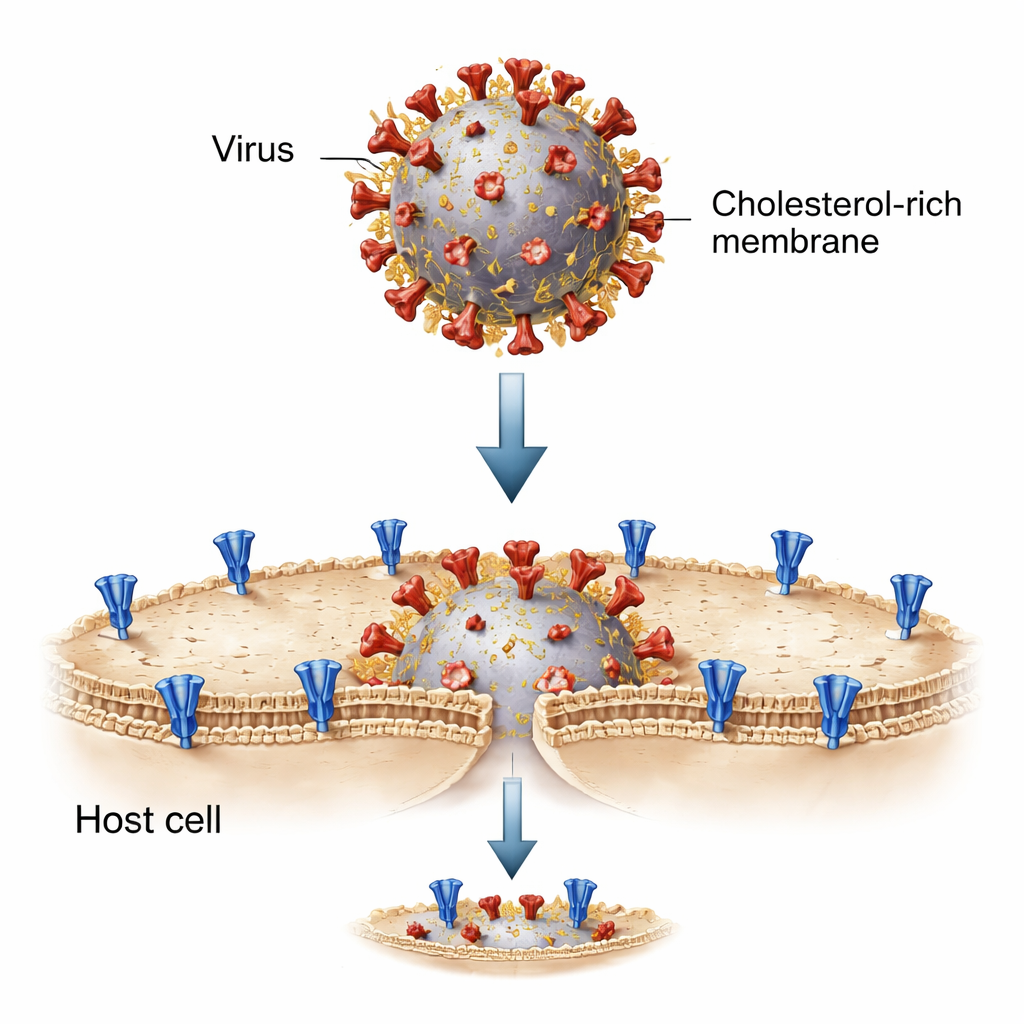
Холестерин усиливает докинг больше, чем собственно слияние
Путем изменения содержания холестерина команда обнаружила: добавление холестерина в мембрану, содержащую спайк, делало слияние более частым, но не так, как можно было бы ожидать. Высокий уровень холестерина существенно не увеличивал вероятность того, что уже прикрепленные мембраны действительно сольются. Вместо этого он резко повышал частоту первичного докинга везикул со спайком к везикулам с ACE2. Покадровая флуоресцентная визуализация показала гораздо больше успешных событий докинга, когда спайк находился в холестерин-обогащенных мембранах, тогда как вероятность того, что прикрепленная пара перейдет к полномасштабному слиянию, оставалась примерно постоянной. Примечательно, что насыщение холестерином стороны с ACE2 давало мало пользы и при очень высоких уровнях даже мешало слиянию, что указывает на то, что главным драйвером является вирусный, а не клеточный холестерин.
От модельных мембран к живым клеткам
Затем исследователи проверили, сохраняется ли тот же рисунок в живых клетках. Они модифицировали человеческие клетки так, чтобы одни экспрессировали спайк, а другие — ACE2, и наблюдали образование крупных сросшихся структур, или синцитиев, при их смешивании. Удаление холестерина из клеток, экспрессирующих спайк, почти полностью прекращало образование синцитиев, тогда как восстановление холестерина возвращало способность к слиянию. В параллельных экспериментах с псевдовирусами SARS-CoV-2 (безопасными частицами, использующими спайк коронавируса для входа в клетки) удаление холестерина из вирусной мембраны резко снижало инфицирование, а его добавление обратно увеличивало инфицирование в дозозависимой манере. Напротив, изменение холестерина только в клетках с ACE2 давало небольшие изменения. Во всех тестах вывод был одинаков: холестерин в мембране со спайком необходим для эффективного проникновения.
Кластеры спайка: тайное оружие холестерина
Почему холестерин на вирусной стороне так важен? Снимки высокой разрешающей способности мембран показали, что спайк‑белки склонны формировать плотные кластеры при избытке холестерина и остаются более разреженными при его дефиците. Измерения на одиночных молекулах показали дальше, что в таких кластерах находится больше копий спайка при холестерин‑богатых условиях. Авторы проследили этот эффект до богатой цистеином области (CRR) на хвостовой части спайка, внутри вирусной мембраны. Этот участок модифицируется палмитоилированием — типом жирной «якорной» модификации, предпочитающей холестерин‑богатые домены. Когда команда укоротила хвост спайка или мутировала все десять цистеинов, блокируя палмитоилирование, спайк перестал кластеризоваться с холестерином, и холестерин‑опосредованное усиление докинга и слияния исчезло. 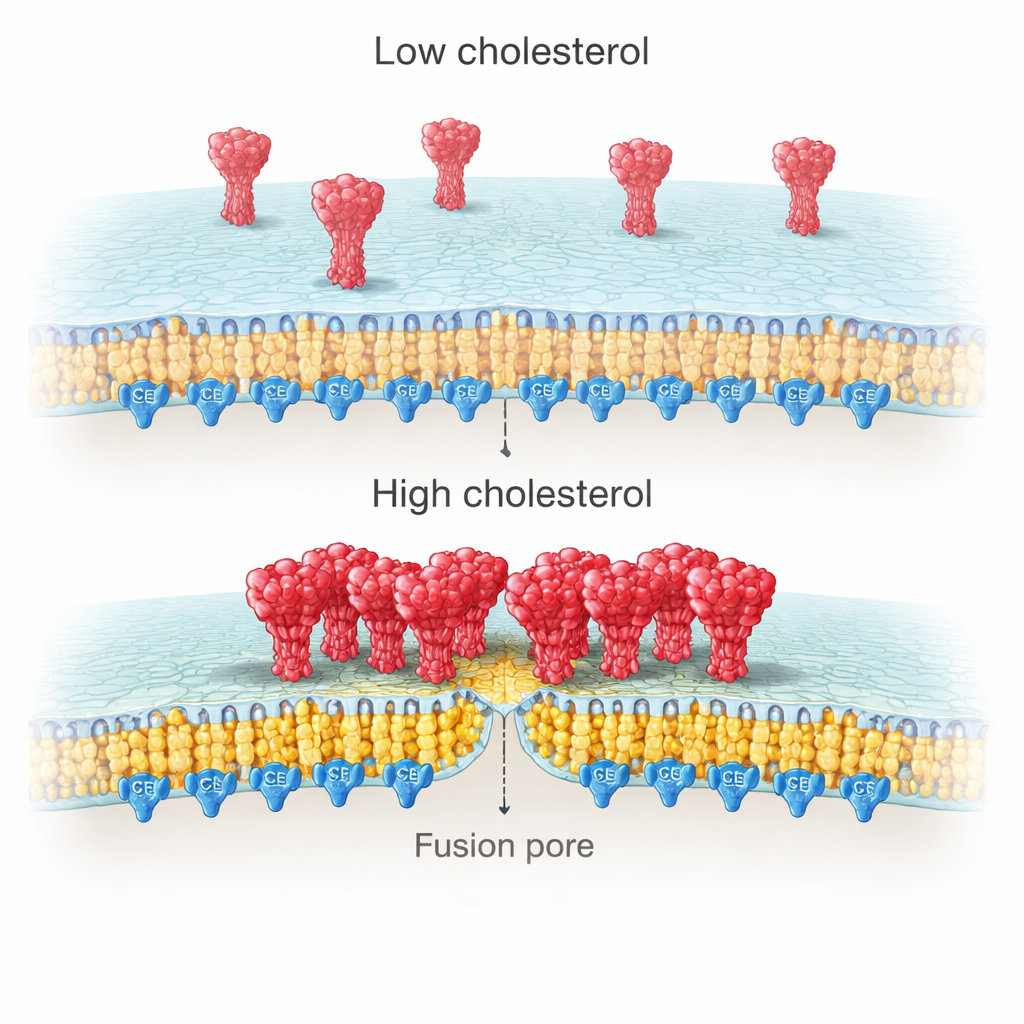
Как это может помочь будущим лечениям
Проще говоря, исследование делает вывод, что холестерин превращает вирусную мембрану в платформу для слияния, собирая множество молекул спайка в плотные кластеры через их палмитоилированную хвостовую область. Эти кластеры эффективнее докируют к ACE2 на клетках хозяина, увеличивая шансы, что каждая встреча завершится успешным слиянием и инфицированием. Для неспециалистов главный вывод таков: холестерин — не просто пассивный компонент вирусной оболочки, а активный организатор машинерии спайка. Это делает цистеин‑богатый, чувствительный к холестерину хвост спайка и ферменты, ответственные за его палмитоилирование, многообещающими мишенями для широких противовирусных стратегий, которые могли бы быть эффективны против разных вариантов коронавирусов.
Цитирование: Li, W., Wu, M., Feng, S. et al. Molecular mechanism of cholesterol-dependent membrane fusion in SARS-CoV-2 entry. Sig Transduct Target Ther 11, 57 (2026). https://doi.org/10.1038/s41392-026-02573-z
Ключевые слова: холестерин, SARS-CoV-2 spike, слияние мембран, вирусное проникновение, палмитоїлирование