Clear Sky Science · ru
PKC-η способствует метастазированию рака молочной железы путем регуляции сигнального пути Hippo–YAP
Почему это исследование важно
Тройной негативный рак молочной железы (TNBC) — одна из самых опасных форм рака молочной железы, потому что он рано дает метастазы и лишен таргетной терапии. В этом исследовании показано, как специфический фермент внутри раковых клеток, называемый PKC‑η (PKCη), действует как главный переключатель, помогая опухолям отделяться, распространяться по организму и образовывать новые очаги. Поняв этот переключатель, исследователи также выявили крошечный природный пептид, который способен его выключать, что указывает на потенциально новый подход к лечению этой агрессивной болезни. 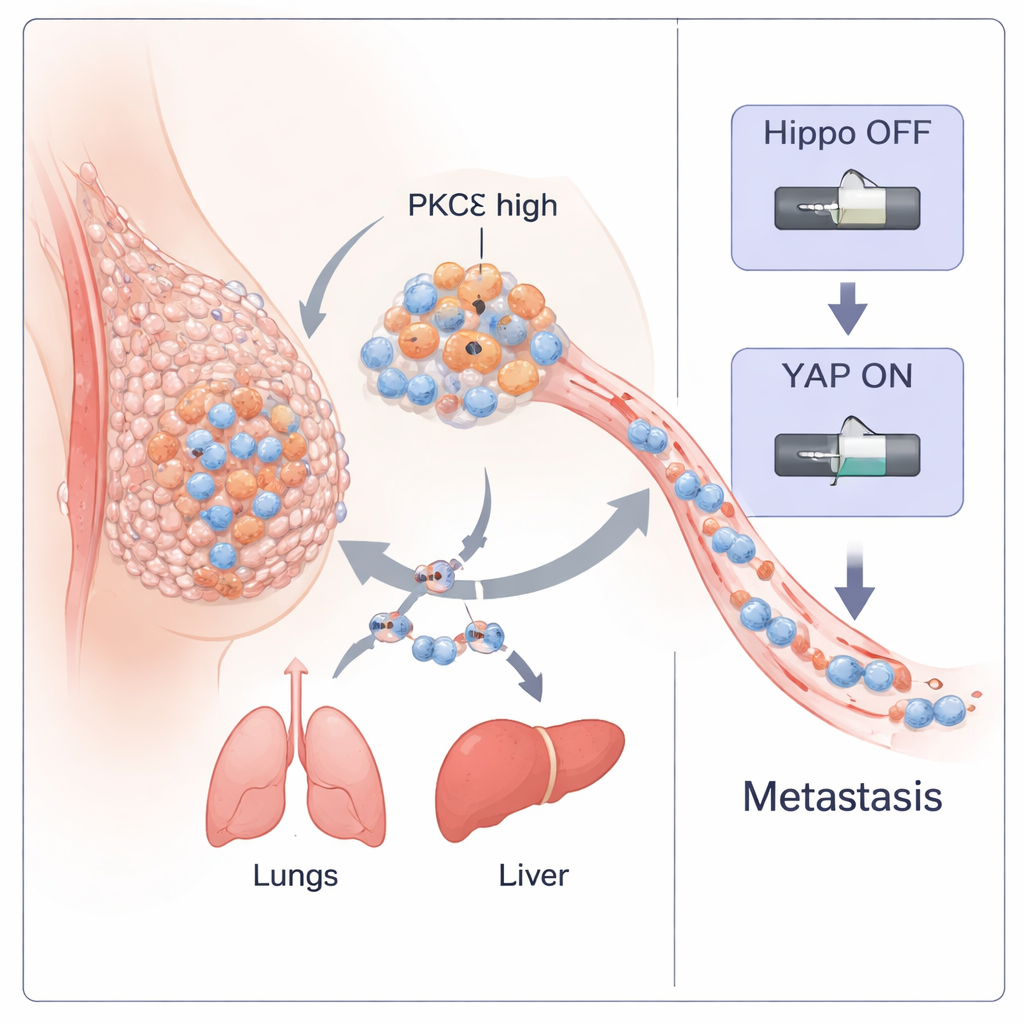
Скрытый драйвер в агрессивных опухолях молочной железы
Команда начала с анализа больших коллекций клинических данных по раку молочной железы. Они обнаружили, что ген, кодирующий PKCη (PRKCH), особенно высоко экспрессируется в подтипе опухолей, известном как «claudin‑low», который сильно пересекается с TNBC и богат стволоподобными, подвижными клетками. В нескольких когортах пациентов опухоли с высокой экспрессией PRKCH демонстрировали сильные сигнатуры эпителиально‑мезенхимального перехода (EMT) — процесса, при котором ранее упорядоченные клетки теряют прикрепление, меняют форму и становятся более инвазивными. Уровни PRKCH также были выше в метастатических образцах по сравнению с первичными опухолями, а окрашивание белков в тканях человеческого TNBC показало более активный перинуклеарный PKCη в опухолях более высокой степени злокачественности и на поздних стадиях. В совокупности эти данные указывали на тесную связь PKCη с агрессивностью опухоли и ее способностью к распространению.
От чашки Петри до мыши: доказательство, что PKCη питает распространение
Чтобы проверить причинно‑следственную связь, исследователи использовали редактирование генома CRISPR для удаления PKCη в двух высоко метастазирующих клеточных линиях TNBC: мышиной (4T1) и человеческой (MDA‑MB‑231). При отсутствии PKCη клетки смещались в более «эпителиальное» состояние: повышалась экспрессия адгезивных белков, таких как E‑кадгерин и EpCAM, и снижались классические мезенхимальные маркеры, включая виментин и N‑кадгерин. Такие клетки с дефицитом PKCη формировали меньше и меньшие колонии, мигрировали и инвазировали менее эффективно, были более чувствительны к гибели при отрыве от субстрата и демонстрировали резкое снижение стволовых признаков рака, включая меньшее число CD44high/CD24low и ALDH‑положительных клеток и уменьшенную способность образовывать сферы. При введении в мышей клетки без PKCη давали меньше и меньшие первичные опухоли и значительно меньше метастазов в легких, печени, мозге и других органах; выживаемость животных также увеличивалась. Восстановление экспрессии PKCη возвращало исходные свойства, что подтвердило активную роль фермента в прогрессии и распространении TNBC.
Как PKCη захватывает путь контроля роста
Далее исследование сосредоточилось на механизмах, с помощью которых PKCη оказывает это прометастатическое действие. Клинические данные показали, что уровни PKCη колеблются синфазно с YAP — мощным регулятором экспрессии генов, контролируемым путем Hippo, который служит «предохранителем», обычно сдерживающим рост. Высокая экспрессия либо PRKCH, либо YAP1 предсказывала худший прогноз пациента, а их одновременная высокая экспрессия была связана с особенно низкой выживаемостью без отдаленных метастазов. В клетках TNBC удаление PKCη снижало общий уровень YAP и смещало его из ядра в цитоплазму, где он неактивен. Биохимические эксперименты показали, что PKCη физически связывается с YAP и специфически фосфорилирует его в позиции Ser128. Эта модификация стабилизирует YAP и способствует его транслокации в ядро для включения генов, запускающих EMT, стволовость и метастазирование. При отсутствии PKCη YAP фосфорилируется в других сайтах (Ser127 и Ser397), что приводит к его связыванию с белками 14‑3‑3, задержке в цитоплазме и последующему разрушению. PKCη также усиливает PTEN — естественный тормоз для кинзы AKT — тем самым удерживая активность AKT низкой и подавляя верхние кинзы Hippo, которые в противном случае инактивировали бы YAP. Таким образом, PKCη одновременно прямо активирует YAP и косвенно отключает «тормоз» Hippo. 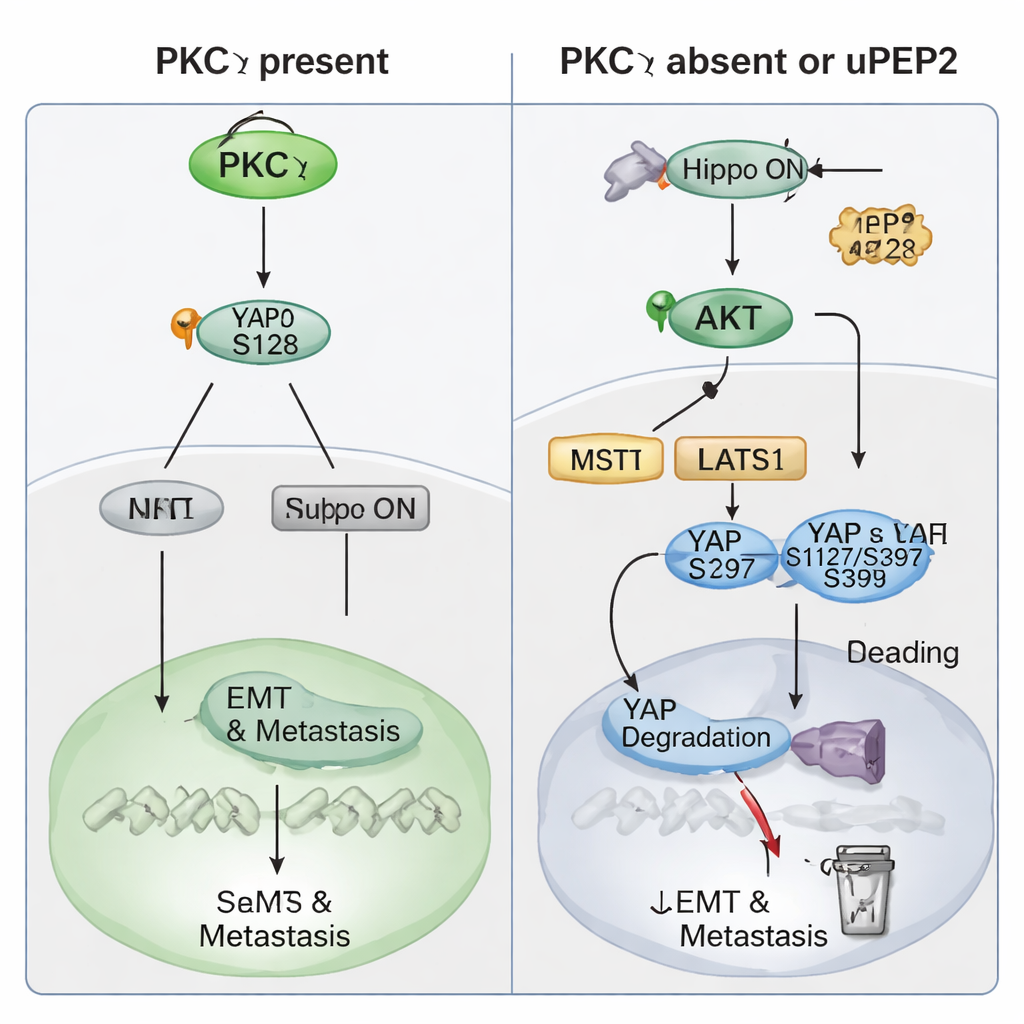
Крошечный пептид, который обезвреживает раковый переключатель
Любопытно, что ген PKCη содержит короткую верхнюю открыту́ю рамку считывания (uORF), кодирующую микропептид uPEP2. Предыдущие работы показали, что uPEP2 может связываться с PKCη и ингибировать родственные к ней киназы. В настоящем исследовании обработка клеток TNBC синтетическим uPEP2 воспроизводила эффекты нокаута PKCη: миграция, инвазия и стволоподобное поведение снижались, профили маркеров EMT смещались в менее агрессивный вариант, а уровни YAP падали при повышении фосфориляции, характерной для его инактивации. В опухолях у мышей uPEP2 снижал уровни PKCη и YAP в первичных опухолях, усиливал инактивацию YAP и ассоциировался с меньшим числом микрометастазов в печени и легких. Механистически uPEP2 способствует деградации PKCη, возвращая активность пути Hippo и направляя YAP к удержанию в цитоплазме и разрушению.
Что это означает для будущих методов лечения
Для непрофессионального читателя главный вывод таков: исследователи выявили PKCη как ключевое звено, помогающее самым агрессивным ракам молочной железы расшатывать прикрепления, двигаться и колонизировать отдаленные органы, отключая природную систему контроля роста и активируя «газ» YAP. Удаление PKCη или использование небольшого природного пептида uPEP2 для его деградации позволяли восстановить «тормоз» Hippo, заглушить YAP и значительно снизить метастазирование в доклинических моделях. Хотя работа находится на экспериментальной стадии и выполнена на клеточных линиях и иммунодефицитных мышах, она выделяет PKCη и его взаимодействие с YAP как перспективные мишени для новых терапий против TNBC и указывает, что препараты, подобные uPEP2, однажды могут помочь предотвратить или ограничить распространение этого трудно поддающегося лечению рака.
Цитирование: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
Ключевые слова: тройной негативный рак молочной железы, PKC-η, путь Hippo‑YAP, эпителиально-мезенхимальный переход, метастазирование рака