Clear Sky Science · ru
Serpina3c защищает от метаболически ассоциированного стеатотического заболевания печени у потомства, вызванного пренатальным приёмом преднизона
Почему это исследование важно для будущих детей
Многим женщинам требуется преднизон во время беременности для контроля тяжёлых аутоиммунных и воспалительных заболеваний. Врачи знают, что он может спасти жизнь матери, но гораздо меньше понятно, как он влияет на долгосрочное здоровье их детей. В этом исследовании задают актуальный вопрос: может ли приём преднизона во время беременности незаметно запрограммировать печень ребёнка так, что у него позже разовьётся жировая болезнь печени, особенно при сочетании с нездоровой диетой? И если да, существует ли способ обратить этот риск?
Нарастающая проблема печени в мире
Метаболически ассоциированное стеатотическое заболевание печени (MASLD) сейчас является одним из самых распространённых хронических заболеваний печени — оно затрагивает примерно треть населения Земли, и ожидается, что распространённость будет расти. Болезнь включает простое накопление жира в печени, воспалительную «жировую гепатит», фиброз, цирроз и даже рак печени. MASLD тесно связано с ожирением, высоким кровяным давлением и сахарным диабетом 2 типа. Всё чаще учёные приходят к выводу, что корни этого заболевания могут закладываться ещё до рождения, когда плод подвергается стрессам — плохому питанию, загрязнению или лекарствам. Эта идея — что ранняя среда жизни формирует пожизненный риск заболеваний — известна как «происхождение здоровья и болезней в развитии». 
Преднизон до рождения как «первый удар»
Чтобы изучить, как пренатальный приём преднизона влияет на печень, исследователи лечили беременных крыс и мышей дозами, подобранными так, чтобы имитировать низкие клинические дозы у людей. Затем они наблюдали за потомством до рождения и в молодом взрослом возрасте. Сами по себе детёныши, подвергшиеся преднизону в утробе, были мельче и уже демонстрировали признаки нарушенного обращения с жирами в печени: больше жировых капель, повышенные триглицериды в печени и ослабленное использование жиров для выработки энергии. По мере роста потомства их печень продолжала откладывать больше жира, чем обычно, даже при обычном питании. Когда животных позднее подвергали высокожировой диете — эквиваленту западной диеты быстрого питания — различия стали драматичными. Потомки, экспонированные преднизону, развивали более тяжёлую форму жировой болезни печени, воспаление и, у самцов, явные признаки фиброза. У них также ухудшался контроль уровня сахара в крови, что указывает на более широкие метаболические нарушения.
Защитный печёночный белок исчезает
Углубляясь, команда использовала масштабный профилинг генов, чтобы найти общие молекулярные изменения в печени у мужского и женского потомства. Один ген выделялся: Serpina3c, который кодирует секретируемый белок из семейства естественных ингибиторов ферментов. В обоих полах пренатальный преднизон резко и устойчиво снижал уровень Serpina3c в печени и в крови — от позднего фетального периода и далее во взросление. Когда учёные искусственно снижали Serpina3c только в печени здоровых мышей, эти животные также становились восприимчивыми к жировой болезни печени и нарушению регуляции глюкозы, особенно на высокожировой диете. Наоборот, повышение уровня Serpina3c в печени потомства, подвергшегося преднизону, после рождения во многом их спасало: в печени откладывалось меньше жира, лучше регулировалась глюкоза, и отмечалось меньше воспаления и фиброза.
Как преднизон перенастраивает печёночные переключатели
Исследователи затем попытались выяснить, как пренатальный преднизон подавляет Serpina3c. Они обнаружили, что активная форма преднизона, преднизолон, чрезмерно активирует глюкокортикоидный рецептор — белок, чувствительный к действию препарата, присутствующий в клетках печени. Этот рецептор затем взаимодействует с другим белком, HDAC3, который уплотняет упаковку ДНК, снимая небольшие «ацетильные» метки с гистонов. Как в тканях печени животных, так и в культивируемых печёночных клетках преднизолон усиливал активность глюкокортикоидного рецептора и HDAC3 прямо в области гена Serpina3c, удаляя ацетильные метки в ключевом месте, называемом H3K27. После удаления этих меток активность гена снижалась, и уровни белка Serpina3c падали. Блокирование рецептора или HDAC3, либо ингибирование деацетилирования восстанавливало эти ацетильные метки, повышало Serpina3c и улучшало обращение с жирами и глюкозой в печёночных клетках.
Вредная каскадная реакция внутри печени
Низкий уровень Serpina3c запускал вторую пагубную цепочку. В норме Serpina3c помогает сдерживать ферменты, такие как химаза, которые локально в тканях генерируют гормон ангиотензин II. При дефиците Serpina3c уровни и активность химазы возрастали, продуцируя больше ангиотензина II в печени и сверхактивируя его рецептор AT1R на печёночных клетках. Этот локальный всплеск гормона известен тем, что способствует окислительному стрессу, инсулинорезистентности, накоплению жира, воспалению и образованию рубцов. И у животных, подвергшихся преднизону, и у мышей с печёночным снижением Serpina3c, путь химаза–ангиотензин II–AT1R был включён, а ключевые гены, поддерживающие сжигание жира и поглощение глюкозы, оказались подавлены. Восстановление Serpina3c после рождения успокаивало этот путь и возрождало более здоровый метаболизм. 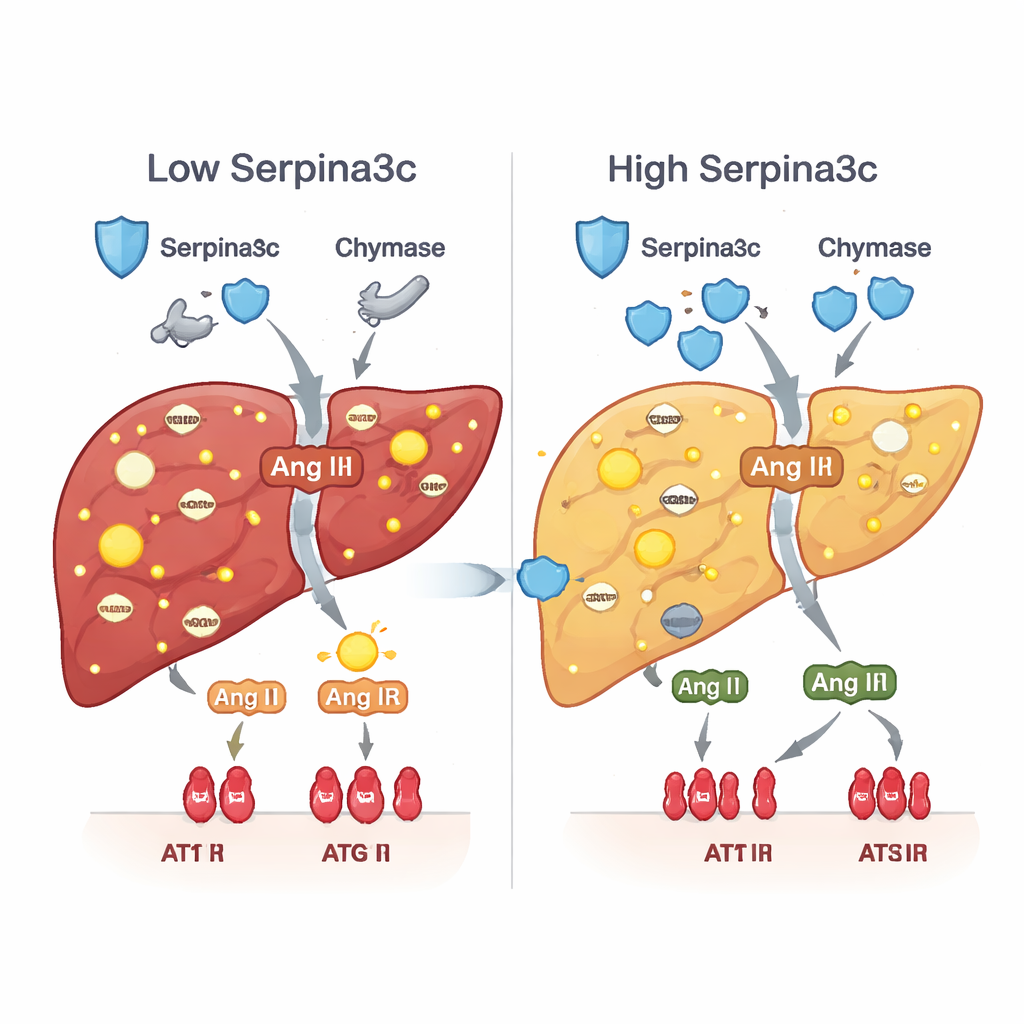
Что это значит для пациентов и семей
Для неспециалистов главный вывод таков: лекарства, принимаемые во время беременности, могут оставить молекулярный отпечаток на развивающейся печени, который сохраняется во взрослой жизни. В этом исследовании преднизон выступал как «первый удар», снижая защитный белок (Serpina3c) через эпигенетические изменения — химические метки на белках, упаковывающих ДНК — так что последующий «второй удар», например высокожировая диета, легче запускал жировую болезнь печени. Обнадеживающая сторона заключается в том, что этот риск не был необратим: повторное повышение Serpina3c в печени после рождения значительно снижало повреждение печени. Хотя эти результаты получены на грызунах, они ставят важные вопросы о том, как мы наблюдаем и поддерживаем детей, матери которых нуждались в преднизоне во время беременности, и указывают на Serpina3c и систему химаза–ангиотензин II как перспективные цели для профилактики или лечения жировой болезни печени, начинающейся ещё до рождения.
Цитирование: Dai, Y., Lu, Z., Peng, Y. et al. Serpina3c protects against metabolic dysfunction-associated steatotic liver disease in offspring induced by prenatal prednisone exposure. Sig Transduct Target Ther 11, 71 (2026). https://doi.org/10.1038/s41392-025-02569-1
Ключевые слова: пренатальный преднизон, жировая болезнь печени, эпигенетика, Serpina3c, происхождение в развитии