Clear Sky Science · ru
Фототерапевтические системы на основе наночастиц: молекулярные механизмы и клинические применения
Свет как деликатный медицинский инструмент
Большинство из нас воспринимает свет как то, что позволяет видеть, согревает кожу или питает солнечные батареи. В этом обзорном статье исследуется более неожиданная роль: использование тщательно настроенного света в сочетании с крошечными инженерными частицами для диагностики и лечения заболеваний изнутри. Авторы описывают, как «фототерапия на основе наночастиц» может фокусировать повреждение на раковых клетках, подавлять воспаление в сердце и суставах и даже помогать мозгу очищать токсичные белки при таких состояниях, как болезнь Альцгеймера, при этом по возможности сохраняя здоровые ткани.
Как крошечные частицы превращают свет в лекарство
В основе этого подхода — наночастицы: структуры в тысячи раз тоньше человеческого волоса, способные переносить лекарства, поглощать свет и преобразовывать его либо в тепло, либо в короткие химические всплески. Доминируют две основные стратегии. В фотодинамической терапии молекулы, активируемые светом на поверхности или внутри наночастицы, порождают реактивные формы кислорода — высокоэнергетические виды кислорода, повреждающие близлежащие клеточные компоненты. В фототермической терапии другие частицы, например золото или черный фосфор, преобразуют ближний инфракрасный свет в тепло, кратковременно «запаривая» опухолевые клетки изнутри. Поскольку свет можно направлять, а частицы проектировать так, чтобы они преимущественно накапливались в пораженных тканях, врачи получают уровень пространственной точности, которого лишены традиционная химиотерапия и облучение. 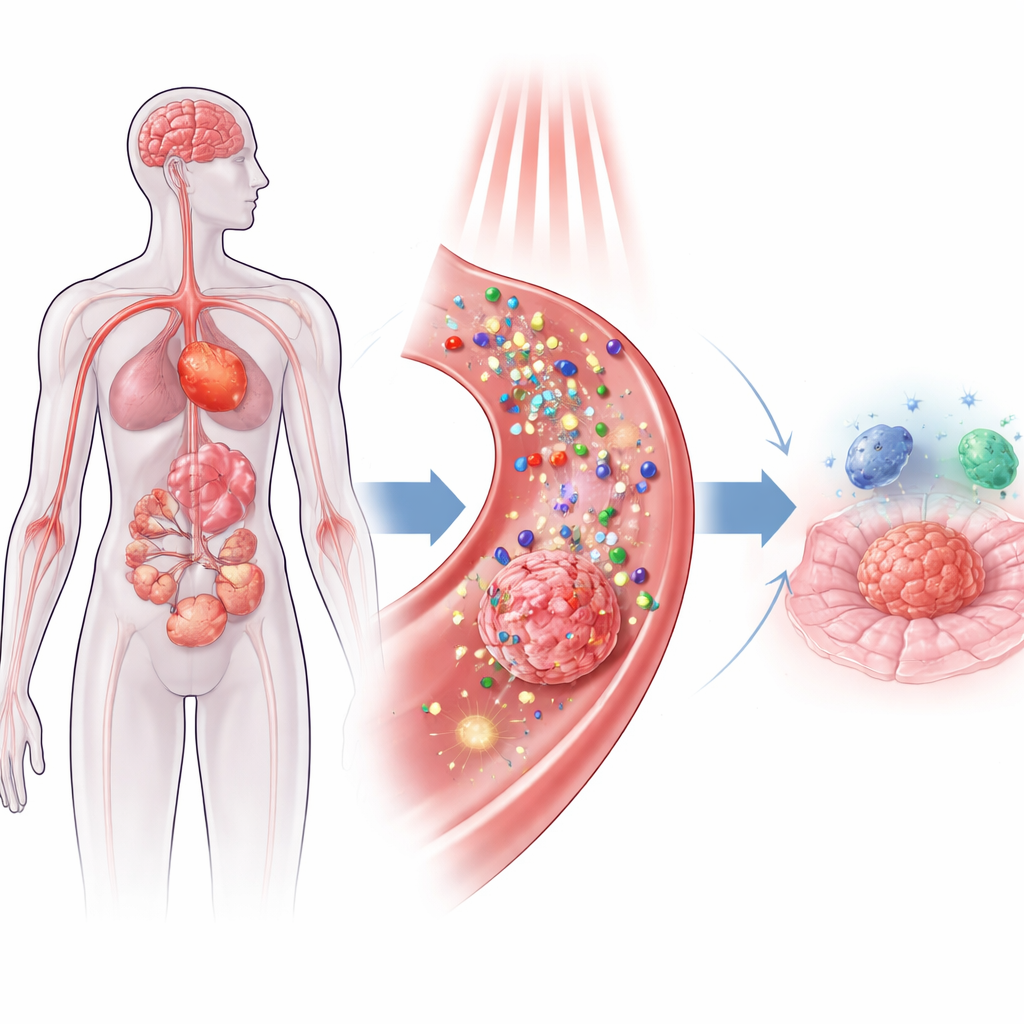
Создание умных носителей и путей доставки
Простое облучение тела светом недостаточно; задача — доставить нужные частицы в нужное место и удержать их там достаточно долго, чтобы они подействовали. Обзор перечисляет набор систем доставки, включая мягкие носители, такие как липосомы, твердые липидные частицы и полимерные сферы или мицеллы, а также жесткие каркасы из кремнезема, металлов, углерода или металл‑органических каркасов. Их поверхности можно покрывать «невидимыми» полимерами для продления циркуляции, натуральными клеточными мембранами для уклонения от иммунного надзора или «адресными метками», распознающими маркеры на раковых или воспаленных клетках. Некоторые конструкции — «умные»: они остаются неактивными в кровотоке, но меняют размер, заряд или форму в ответ на кислотность, ферменты или редокс‑условия внутри опухоли, высвобождая содержимое только там, где это необходимо.
Что происходит внутри клеток при воздействии света
Когда свет включается, запускается каскад молекулярных событий. Авторы объясняют, как зоны возбуждения частиц генерируют всплески окислителей, атакующих мембраны, ДНК и жизненно важные структуры, такие как митохондрии и лизосомы. Это может толкнуть клетку к аккуратному самоуничтожению (апоптозу) или, при сильном повреждении, к более хаотичной гибели. Клетки также могут усиливать аутофагию — механизм внутреннего утилизации, который при мягком стрессе помогает выжить, а при перегрузке ускоряет гибель. Принципиально важно, что умирающие опухолевые клетки могут посылать «сигналы опасности», мобилизуя иммунную систему: экспонировать определенные белки на поверхности, выделять факторы, привлекающие дендритные клетки, и перестраивать иммунные клетки в опухоли с супрессивного состояния в противоопухолевое. По сути, локальная световая терапия может работать как персонализированная онковакцина. 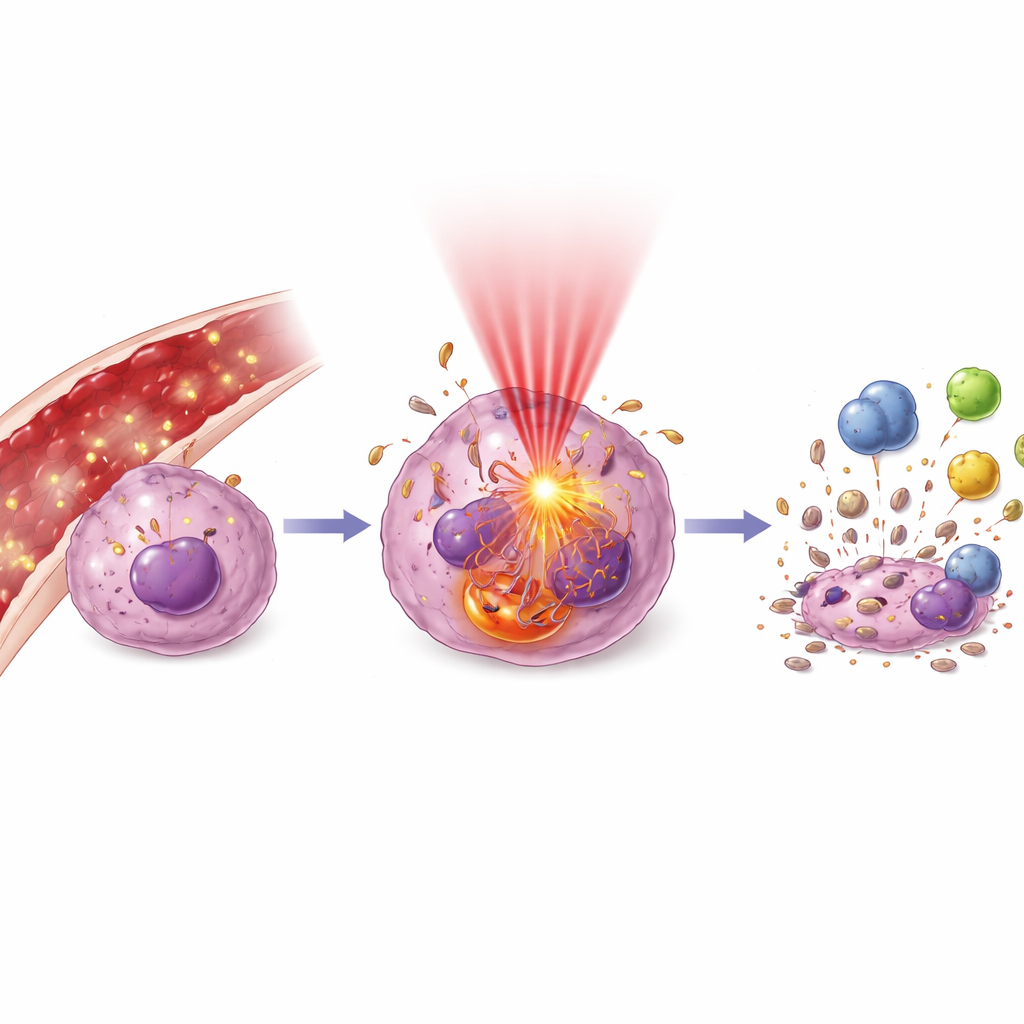
За пределами рака: сердце, мозг и аутоиммунные мишени
Хотя рак — наиболее развитая область, те же принципы адаптируют и для хронических состояний. При сердечно‑сосудистых заболеваниях световые подходы направлены не на уничтожение клеток, а на снижение окислительного стресса, стабилизацию эндотелия и даже на уменьшение или уплотнение опасных бляшек. В мозге, где нейроны особенно чувствительны, более щадящие режимы света — часто называемые фотобиомодуляцией — стремятся повысить митохондриальную энергообразующую способность, уменьшить скопления токсичных белков и ослабить воспаление, вызванное микроглией и астроцитами. Обзор также отмечает ранние работы в области метаболических и аутоиммунных заболеваний, где аккуратно дозированный свет и наночастицы способны сместить иммунные клетки от агрессивного, разрушающего ткани поведения к более регуляторным, успокаивающим ролям, одновременно умеренно улучшая чувствительность к инсулину и сигнальную активность жировой ткани.
От лаборатории к клинике: обещания и препятствия
Несмотря на десятилетия исследований, лишь немногие светоактивные препараты полностью одобрены, в основном для глазных заболеваний и некоторых опухолей. Авторы утверждают, что нанотехнологии начинают открывать следующий виток развития, обеспечивая более глубокое проникновение света, лучшее таргетирование и встроенную визуализацию для мониторинга лечения в реальном времени. Тем не менее остаются серьезные препятствия: масштабирование производства наночастиц с устойчивым качеством, подтверждение долгосрочной безопасности и выведения из организма, эффективная доставка света в глубокие органы и соответствие строгим регуляторным требованиям. Обзор делает вывод, что объединение материаловедения, оптики, биологии и подходов, управляемых искусственным интеллектом, ставит фототерапию на основе наночастиц на путь трансформации из нишевой процедуры в более широкую, неинвазивную опору прецизионной медицины.
Цитирование: Chauhan, D.S., Prasad, R., Dhanka, M. et al. Nanoparticles-based phototherapy systems: molecular mechanisms and clinical applications. Sig Transduct Target Ther 11, 95 (2026). https://doi.org/10.1038/s41392-025-02536-w
Ключевые слова: фототерапия на основе наночастиц, фототермическая терапия, фотодинамическая терапия, наномедицина при раке, фотобиомодуляция