Clear Sky Science · ru
IFFO1 ингибирует рак молочной железы, координируя деление митохондрий и синтез жирных кислот через ось LaminA/C-PGC1α
Почему это исследование важно
Рак молочной железы по‑прежнему остается одной из ведущих причин смертности от рака у женщин, во многом потому, что некоторые опухоли продолжают расти, метастазировать и ускользать от текущих методов лечения. В этом исследовании выявлен ранее недооцененный клеточный «тормоз» — белок IFFO1, который замедляет развитие рака молочной железы, одновременно сдерживая два ключевых двигателя опухолевого роста: энергетические фабрики клетки — митохондрии, и её способность синтезировать и запасать жиры. Понимание работы этого тормоза открывает новый угол для терапии, который может быть эффективен против нескольких подтипов рака молочной железы.
Скрытый страж внутри клеток молочной железы
Исследователи начали с анализа образцов от 30 женщин с раком молочной железы и больших общедоступных онкологических баз данных. Они обнаружили, что уровень белка IFFO1 в опухолевой ткани систематически ниже, чем в прилежащей нормальной ткани молочной железы. Чем более продвинута стадия рака, тем меньше присутствовало IFFO1, а у пациентов с более высоким уровнем IFFO1 в опухоли наблюдалась более высокая выживаемость. В культурах клеток рака молочной железы вынужденная сверхэкспрессия IFFO1 резко снижала их способность к росту, делению и миграции — поведенческим проявлениям, необходимым для расширения и распространения опухолей. IFFO1 также подавлял клеточную программу эпителиально‑мезенхимального перехода, которая помогает раковым клеткам отделяться и проникать в другие ткани.
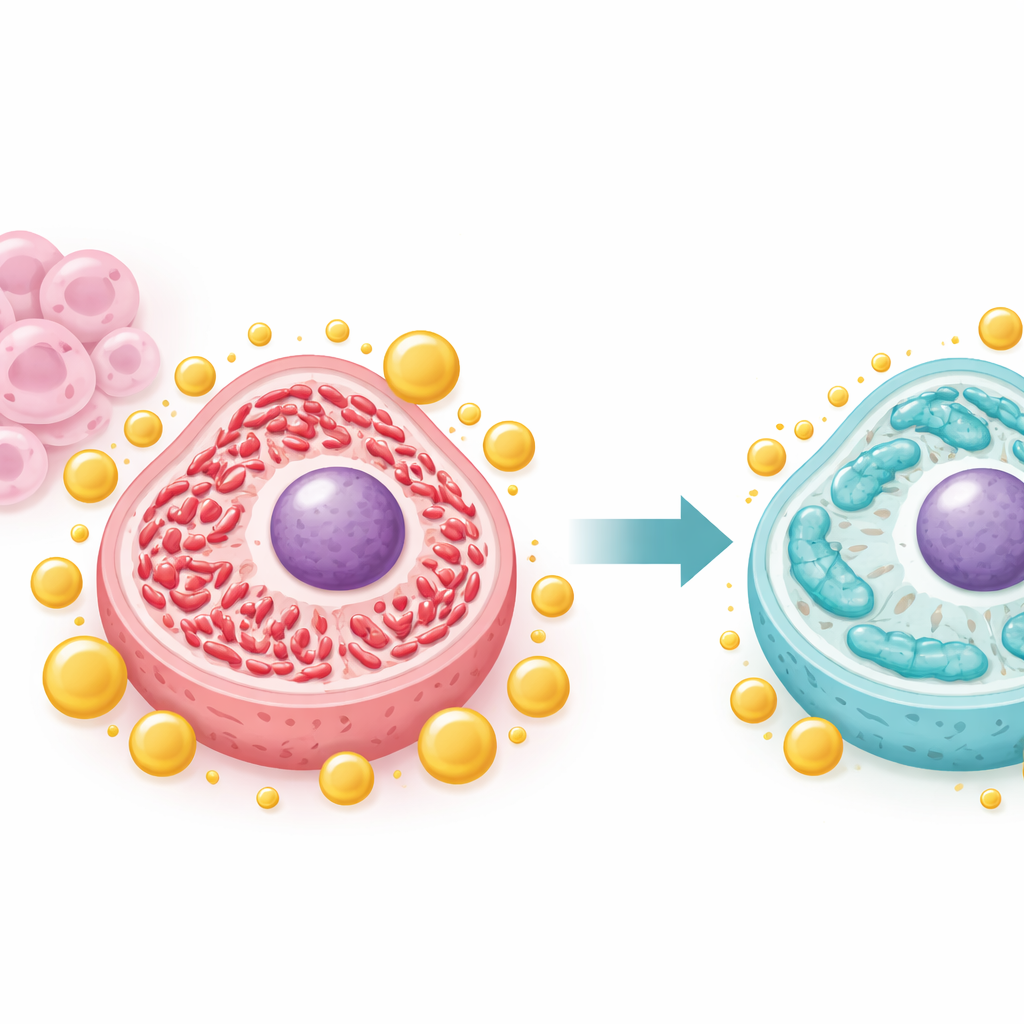
Успокаивая чрезмерно активные энергетические фабрики
Раковые клетки часто перестраивают свои митохондрии — крошечные электростанции внутри клетки — чтобы подпитывать быстрый рост. Команда показала, что IFFO1 смещает баланс от сильно фрагментированного состояния «деления» (fission) в сторону более удлинённого состояния «слияния» (fusion), которое обычно ассоциируется со здоровыми, более стабильными митохондриями. При высокой экспрессии IFFO1 ключевые белки деления, такие как Drp1 и Fis1, снижались, тогда как белки слияния увеличивались. Микроскопия показала удлинение митохондрий и уменьшение их фрагментации, а показатели митохондриальной ДНК и энергетической активности снижались по сравнению с аномально высокими уровнями, характерными для агрессивных клеток. Эти изменения указывают на то, что IFFO1 препятствует переходу митохондрий в гиперактивную конфигурацию, поддерживающую бесконтрольный рост опухоли.
Перекрывая линию снабжения жирами
Быстро растущим опухолям нужно не только много энергии; им также необходим постоянный приток жиров для построения новых мембран и сигнальных молекул. Исследование показало, что IFFO1 также подавляет этот метаболический ускоритель. В клетках с повышенным уровнем IFFO1 снижались основные белки липогенеза — включая FASN, SREBP‑1, SCD1 и другие. Ферментные тесты подтвердили уменьшение активности синтеза жиров, а химические анализы показали снижение уровня свободных жирных кислот, триглицеридов и холестерина. Красители для визуализации жировых запасов выявляли меньше липидных капель и меньше нейтральных жиров внутри раковых клеток. Напротив, увеличение уровня белка деления Drp1 имело противоположный эффект — усиливало синтез жиров, тогда как подавление Drp1 его тормозило, что подтверждает прямую связь между формой митохондрий и обеспечением опухоли липидами.
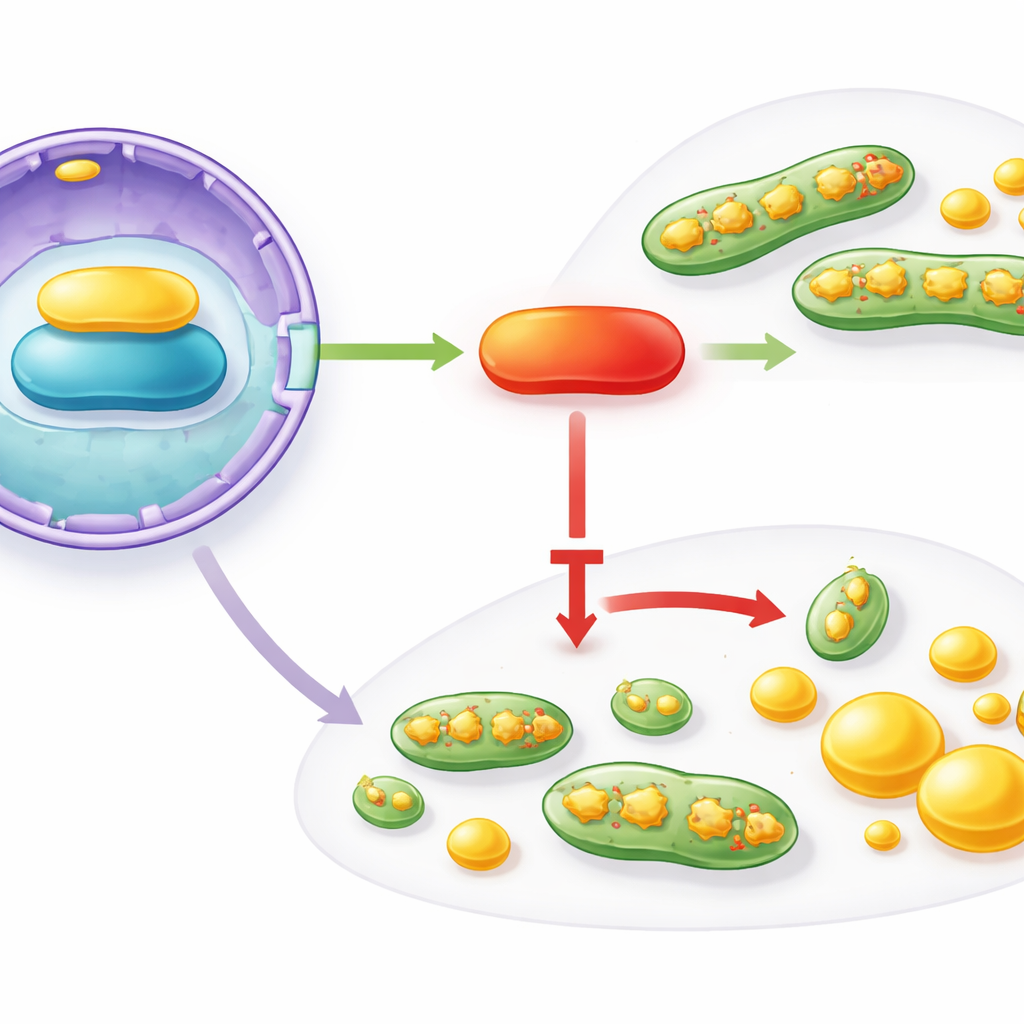
Сигнальная цепочка от ядра к митохондриям
Как IFFO1 координирует эти широкие изменения? Авторы проследили цепочку взаимодействий, которая начинается в ядре клетки и заканчивается на митохондриях и механизмах синтеза липидов. IFFO1 физически связывается со структурным белком ядерной оболочки Lamin A/C и повышает его уровни. Lamin A/C, в свою очередь, поддерживает активность PGC1α — главного регулятора, управляющего здоровьем митохондрий и метаболизмом. В тканях рака молочной железы и в клеточных моделях и Lamin A/C, и PGC1α были снижены, повторяя картину потери IFFO1. При искусственном повышении IFFO1 уровни Lamin A/C и PGC1α росли, митохондриальное деление уменьшалось, а синтез жиров ослабевал. Подавление Lamin A/C нивелировало эти преимущества, но восстановление PGC1α возвращало их, указывая на функциональную ось IFFO1 → Lamin A/C → PGC1α, которая сдерживает опухоле-стимулирующие митохондриальные и липидные изменения.
Испытание тормоза в живых организмах
Чтобы понять, переносятся ли эти клеточные эффекты на реальные опухоли, команда имплантировала человеческие клетки рака молочной железы с повышенным уровнем IFFO1 или без него в мышей. Опухоли с усиленным IFFO1 росли медленнее, имели меньшую массу в конце эксперимента и демонстрировали меньше признаков накопления жиров. В отдельной модели, где клетки вводили в кровоток для образования метастаз в лёгких, клетки, перепроизводящие IFFO1, формировали заметно меньше лёгочных узелков. Анализы тканей этих мышей подтвердили результаты клеточных культур: более высокие уровни Lamin A/C и PGC1α, меньше митохондриального деления и сниженный синтез жиров.
Что это означает для будущих методов лечения
В совокупности работа представляет IFFO1 как многоуровневый опухолевый супрессор, который связывает структурный каркас клетки, её энергетические фабрики и механизмы синтеза жиров. Стабилизируя Lamin A/C и усиливая PGC1α, IFFO1 предотвращает чрезмерную фрагментацию митохондрий и блокирует перепроизводство липидов, от которых зависят раковые клетки. Для неспециалистов ключевая мысль такова: этот белок действует как внутренний тормоз как энергии, так и строительных блоков, подпитывающих рост и распространение рака молочной железы. Лекарства, которые повышают уровень IFFO1 или имитируют его влияние на путь Lamin A/C–PGC1α, могли бы в будущем предложить новые подходы, особенно при агрессивных или резистентных к лечению формах рака молочной железы.
Цитирование: Cai, H., He, J. IFFO1 inhibits breast cancer by coordinating mitochondrial fission and fatty acid synthesis via the LaminA/C-PGC1α axis. Oncogenesis 15, 16 (2026). https://doi.org/10.1038/s41389-026-00609-1
Ключевые слова: рак молочной железы, митохондриальная динамика, синтез жирных кислот, метаболизм опухоли, путь PGC1α