Clear Sky Science · ru
Онкогенный контроль синтеза нуклеотидов
Почему раковые клетки заботятся о строительных блоках
Рак часто описывают как клетки, которые не останавливаются в делении. Но чтобы копировать себя, эти клетки нуждаются в постоянном поступлении крошечных строительных блоков — нуклеотидов, которые входят в состав ДНК и РНК и также участвуют в энергообеспечении множества клеточных процессов. В этом обзоре объясняется, как онкогены перенастраивают клеточную химию, чтобы поддерживать высокий уровень синтеза нуклеотидов, как опухоли переключаются между разными путями получения этих молекул и как врачи могут использовать эти трюки с помощью старых и новых препаратов.
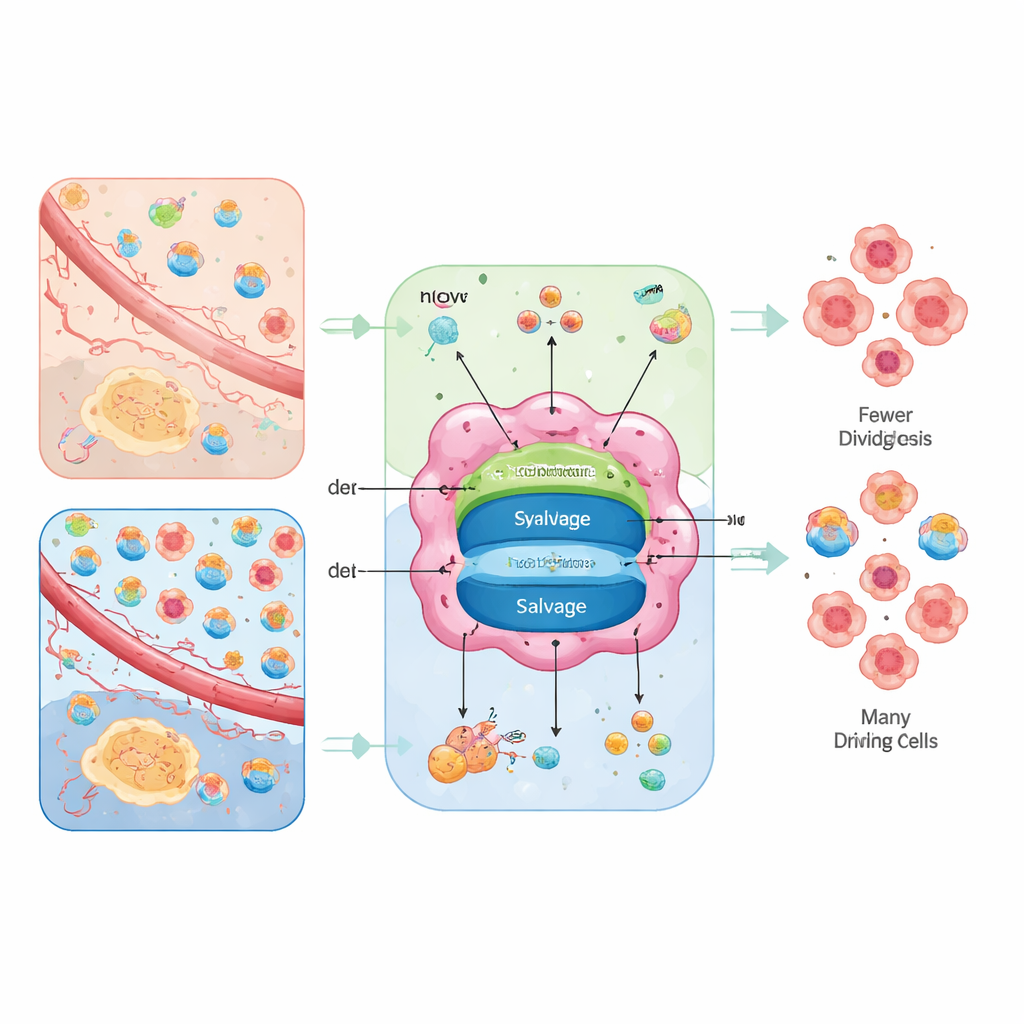
Два пути к одним и тем же строительным блокам
Клетки могут синтезировать нуклеотиды «с нуля» или перерабатывать их повторно. Путь «с нуля», называемый de novo синтезом, собирает кольца из простых питательных веществ, таких как глюкоза, аминокислоты, углекислый газ и бикарбонат, с помощью многоступенчатых, энергозатратных реакций. Путь утилизации (salvage) принимает расщеплённые основания и нуклеозиды из внешней среды или клеточного мусора и восстанавливает их в пригодные нуклеотиды с куда меньшими энергетическими затратами. Опухоли используют оба варианта, но их соотношение зависит от внутреннего энергетического состояния клетки и от того, что предоставляет окружающая ткань.
Как микроокружение опухоли управляет выбором
Авторы рассматривают снабжение нуклеотидов как задачу «маршрутизации, сформированной окружением». В плохо питаемых областях, где аминокислоты есть, но свободных нуклеозидов мало, раковые клетки сильно полагаются на de novo пути и становятся уязвимыми к препаратам, блокирующим эти шаги. В лучше перфузируемых зонах, где кровь доставляет много нуклеозидов или митохондрии ослаблены, опухоли могут больше опираться на путь утилизации и чувствительны скорее к блокаторам транспортёров, мешающим усвоению нуклеозидов. Когда открыты оба пути, опухоль демонстрирует метаболическую гибкость и может уклоняться от монотерапии; когда оба пути закрыты, клетки останавливаются в репликации ДНК, накапливают повреждения и могут погибнуть или перейти в более зрелые, менее агрессивные состояния.
Скрытые линии поддержки, питающие снабжение нуклеотидов
Чтобы фабрики по производству нуклеотидов продолжали работать, необходимы несколько вспомогательных цепочек. Пентозофосфатный путь обеспечивает сахаро-скелет и восстановительную силу; глутамин и энергетический цикл в митохондриях дают азот и аспартат; серин, глицин и фолатная химия поставляют одноуглеродные фрагменты, завершающие построение колец; бикарбонат приносит необходимые углеродные атомы. Онкоприводители, такие как PI3K–AKT–mTORC1, RAS–MAPK и MYC, активируют эти пути совместно, усиливают ключевые ферменты и даже собирают многоферментные комплексы, которые эффективно направляют нестабильные интермедиаты. Напротив, сенсоры стресса, такие как LKB1–AMPK и p53, обычно действуют как тормоза, снижая выпуск нуклеотидов при угрозе энергетического дефицита или повреждения ДНК — тормоза, которые во многих опухолях отключаются.
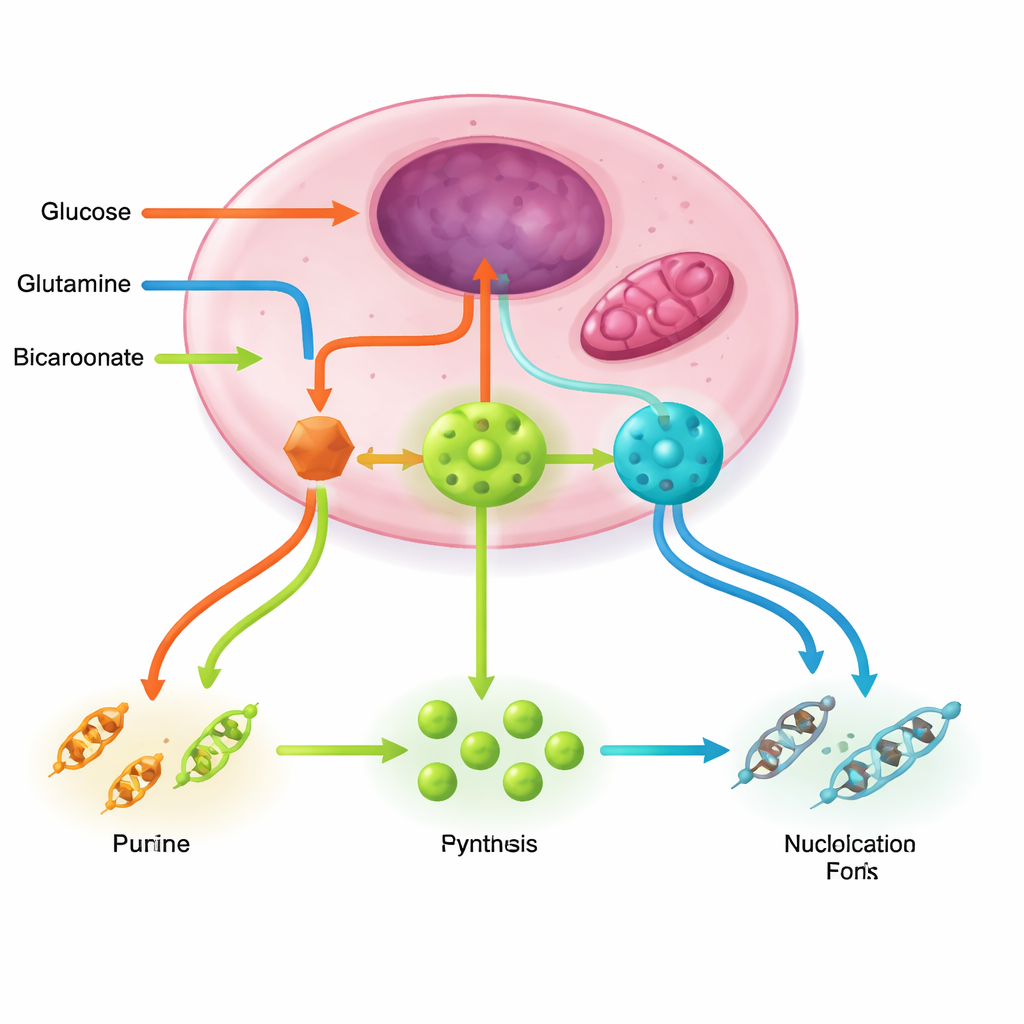
Старая химиотерапия, новая метаболическая логика
Поскольку быстрорастущие клетки сильно зависят от нуклеотидов, одни из первых химиопрепаратов нацеливались на эту слабость. Классические лекарства, такие как метотрексат, 5‑фторурацил, цитарабин, гемцитабин и разнообразные аналоги пуринов, либо блокируют использование фолатов, либо ингибируют специфические ферменты, либо маскируются под дефектные строительные блоки, отравляющие ДНК и РНК. Обзор пересматривает эти препараты в свете модели маршрутизации, объясняя, почему побочные эффекты и резистентность распространены: нераковые ткани тоже нуждаются в нуклеотидах, и опухоли часто могут перенаправить поток через путь утилизации или параллельные ветви, когда одна точка заблокирована.
Стратегии следующего поколения и открытые вопросы
Новые подходы стремятся быть более селективными, атакуя наиболее специфичные для рака участки сети. Ведутся разработки экспериментальных препаратов против митохондриальных одноуглеродных ферментов, таких как MTHFD2, пиримидинового фермента DHODH и пуриновых ферментов, например IMPDH и PAICS, часто в комбинациях с ингибиторами транспортёров пути утилизации. Авторы предлагают практичные маркеры — такие как уровни транспортёров, плотность кровеносных сосудов, состояние митохондрий и экспрессия конкретных метаболических ферментов — чтобы решать, какие опухоли больше зависят от de novo или salvage, и подбирать пациентам таргетные терапии. В будущем они выделяют ключевые вопросы: как эти маршруты меняются в пространстве и времени внутри реальных опухолей, как окружающие иммунные и стромальные клетки формируют доступность нуклеотидов и как разрабатывать терпимые схемы лечения, эксплуатирующие репликационный стресс без чрезмерного ущерба для нормальных тканей. В целом работа утверждает, что понимание и нацеливание на метаболизм нуклеотидов могут превратить базовую потребность деления клеток в мощный, персонализированный рычаг борьбы с раком.
Цитирование: Vidal-Cruchez, O., Ben-Sahra, I. The oncogenic control of nucleotide synthesis. Oncogenesis 15, 17 (2026). https://doi.org/10.1038/s41389-026-00608-2
Ключевые слова: метаболизм нуклеотидов, метаболизм рака, de novo синтез, пути утилизации, метаболические терапии