Clear Sky Science · ru
Поглощение жирных кислот, опосредованное FABP4, способствует старению CD8+ T-клеток через перекисное окисление липидов в адипоцит-обогащённой микросреде рака яичников
Почему жир и иммунные клетки важны при раке яичников
Рак яичников часто распространяется в брюшную полость, где сталкивается с большими отложениями жира. Эта жировая среда — не просто пассивный фон: она активно формирует поведение иммунных клеток. В частности, она может ослаблять CD8 «киллерные» T-клетки, которые должны атаковать опухоль. В данном исследовании изучается, как вещества, происходящие из жира, заставляют эти T-клетки переходить в стареющее, функционально угнетённое состояние, и как блокирование ключевого белка-транспортёра жиров может помочь восстановить их противоопухолевую активность.
Жировая среда, которая старит иммунных защитников
Клиники давно отмечают, что у многих женщин с прогрессирующим раком яичников накапливается жидкость в брюшной полости, а опухоли локализуются в жиросодержащих тканях, называемых сальником. Анализ данных одноядерной РНК и изучение образцов опухолей под микроскопом показали: CD8 T-клетки вблизи этих жировых отложений чаще проявляли признаки клеточного старения — сенесценции. Такие «постаревшие» T-клетки накапливают пигменты отработанных материалов, перестают делиться и вместо уничтожения раковых клеток продуцируют провоспалительные сигналы. Как в образцах человека, так и в мышиных моделях CD8 T-клетки, извлечённые из опухольных зон, богатых жиром и асцитом, были заметно более сенесцентными по сравнению с клетками из лимфоузлов или селезёнки, что прямо связывает адипоцит-обогащённую микросреду с процессом старения T-клеток.
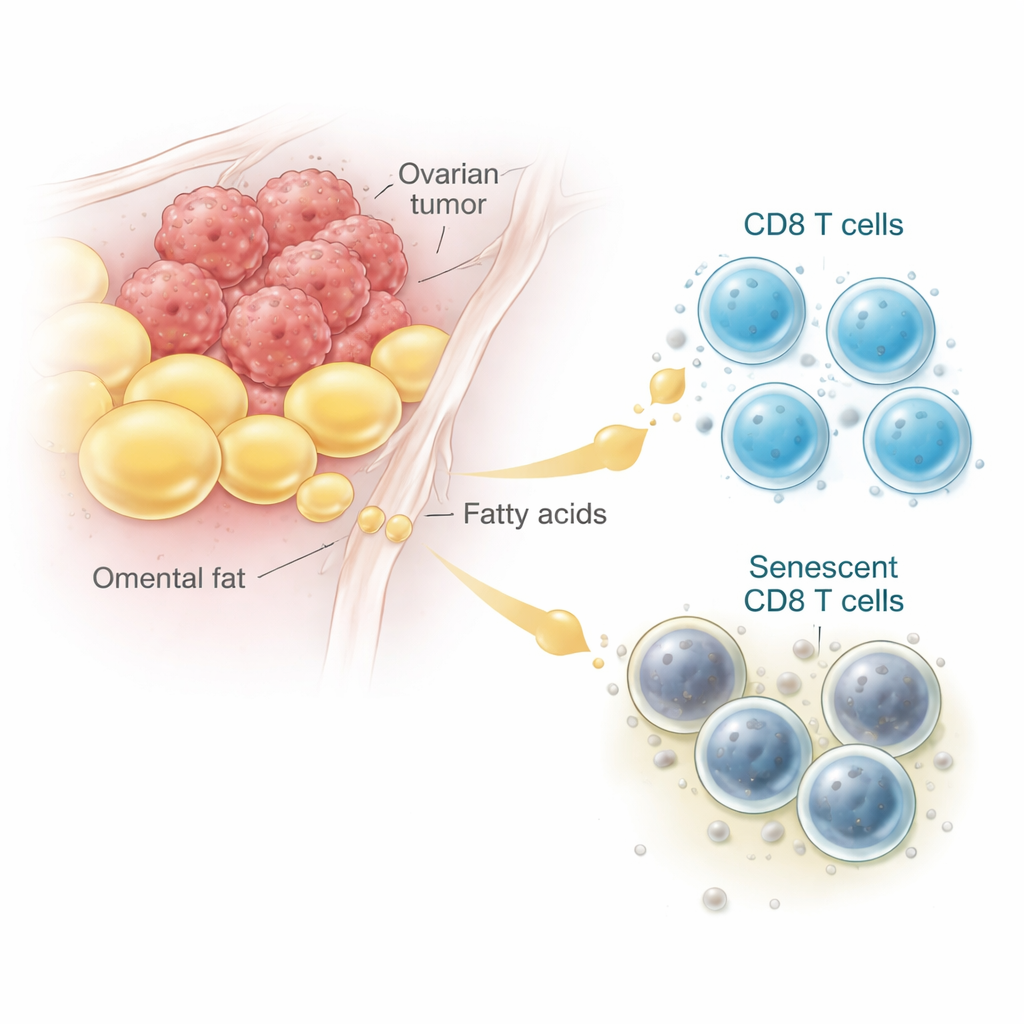
Как распространённая жирная кислота превращает полезное топливо во вред
Чтобы понять, что делает жир с T-клетками, команда воссоздала опухолевую обстановку в лаборатории. Они выращивали клетки рака яичников вместе с мышиными CD8 T-клетками и добавляли либо экстракты жировой ткани, либо специфическую жирную кислоту — олеиновую кислоту, которая широко представлена в жидкости при раке яичников. При умеренных и высоких дозах олеиновая кислота вызывала повышение доли сенесцентных CD8 T-клеток — но только в присутствии опухолевых клеток. Вместо того чтобы сжигать поступившие липиды в качестве энергии, T-клетки накапливали липиды, которые затем подвергались химическому повреждению — процессу, известному как перекисное окисление липидов. Генные и липидные анализы показали увеличение маркеров окисленных жиров и клеточного стресса, тогда как энергетическое производство из жира оставалось прежним. Иными словами, в присутствии опухоли жир, который должен был служить топливом, направлялся в повреждающие реакции, старящие и инактивирующие T-клетки.
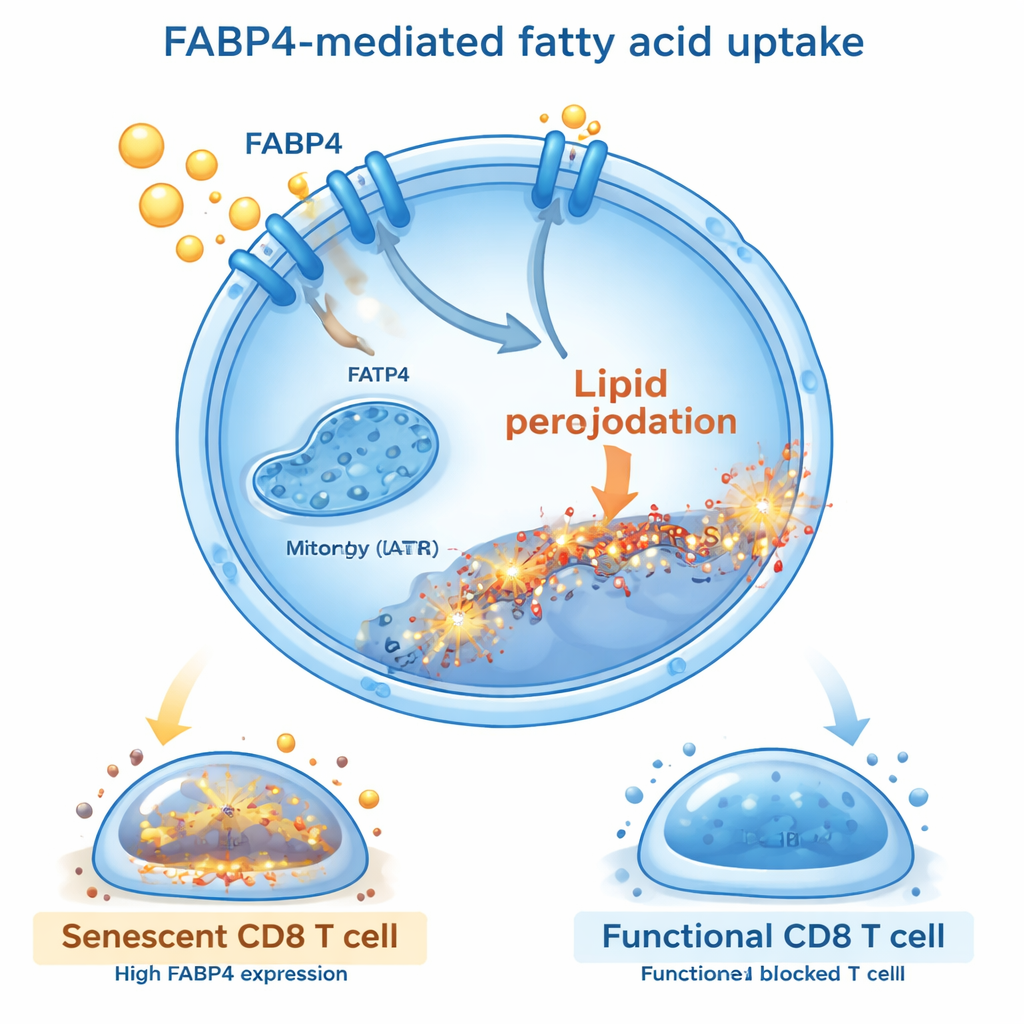
Транспортёр жиров FABP4 как ключевой регулятор
Углубляясь, исследователи выяснили, какие молекулы контролируют этот вредоносный приток жиров. Они обнаружили, что белок-транспортёр FABP4 сильно активировался в CD8 T-клетках после воздействия жировых экстрактов или олеиновой кислоты. FABP4 действует как «шаттл», перенося длинноцепочечные жирные кислоты в клетку. При блокировании FABP4 либо малым молекулой (BMS309403), либо генетическим подавлением T-клетки поглощали меньше жира, демонстрировали меньше перекисного окисления липидов и реже переходили в состояние сенесценции. Такие защищённые T-клетки лучше делились, вырабатывали больше противоопухолевых молекул, таких как интерферон-гамма и гранзим B, и выделяли меньше супрессивных и провоспалительных сигналов. Восстановление уровня FABP4 возвращало отрицательные эффекты, что подтверждает роль этого транспортёра как центрального переключателя, связывающего захват жира с старением T-клеток.
От экспериментов на мышах к потенциальной стратегии лечения
Далее команда протестировала блокаду FABP4 на живых мышах с раком яичников, распространившимся в брюшную полость. Лечение ингибитором FABP4 снижало захват жира и липидное повреждение в CD8 T-клетках, извлечённых из брюшной жидкости, уменьшало долю сенесцентных T-клеток и повышало уровни ключевых эффекторных молекул. Комбинация ингибитора FABP4 со стандартной химиотерапией приводила к меньшему числу видимых опухолевых узелков, более сильным T-клеточным ответам в селезёнке, лимфоузлах и асците, а также к увеличению выживаемости по сравнению с применением одной только химиотерапии. Эти результаты предполагают, что нацеливание на жировой метаболизм может повысить эффективность существующих терапий, возрождая «передовых» бойцов иммунной системы.
Что это означает для пациентов
Для неспециалистов главный вывод таков: при раке яичников важно не только сама опухоль, но и «жирный» район, в котором она живёт. Молекулы, происходящие из жира, особенно определённые жирные кислоты, могут преждевременно старить киллерные T-клетки, лишая их способности атаковать рак. В этом исследовании идентифицирован транспортёр жиров FABP4 как ключевой виновник этого процесса. Блокируя FABP4, по крайней мере в мышиных моделях, исследователи смогли уменьшить старение T-клеток, восстановить их функцию и повысить эффективность химиотерапии. Хотя прежде чем превратить это в клиническую терапию потребуется дополнительная работа, исследование открывает новую перспективу: лечить не только сам рак, но и метаболические «ловушки» в его окружении, которые обезоруживают иммунную систему.
Цитирование: Yu, C., Li, X., Qian, X. et al. Fatty acid uptake mediated by FABP4 promotes the formation of CD8+T cell senescence through lipid peroxidation in the adipocyte-rich microenvironment of Ovarian Cancer. Oncogenesis 15, 9 (2026). https://doi.org/10.1038/s41389-026-00600-w
Ключевые слова: рак яичников, клеточное старение T-лимфоцитов, метаболизм жирных кислот, опухолевая микросреда, FABP4