Clear Sky Science · ru
Реорганизация цитоскелета, вызванная новым слиянием кератинов K6-K14, способствует стволовости рака и клеточной пластичности через отбор по пути cGAS-STING
Как меняющие форму раковые клетки перехитряют окружающую среду
Раковые клетки не просто бесконтрольно делятся; они также учатся изменять и искажать собственный «внутренний скелет», чтобы выжить, скрыться и распространяться. В этом исследовании показано, как конкретный структурный дефект в клетках рака головы и шеи способен разрушать их ядра, включать встроенную систему обнаружения опасности, переводить клетки в состояние дремоты и в конечном итоге способствовать их возврату в более агрессивные, инвазивные, похожие на стволовые клетки формы. Понимание этого механического пути эволюции рака может открыть новые возможности для блокирования рецидивов и метастазирования.
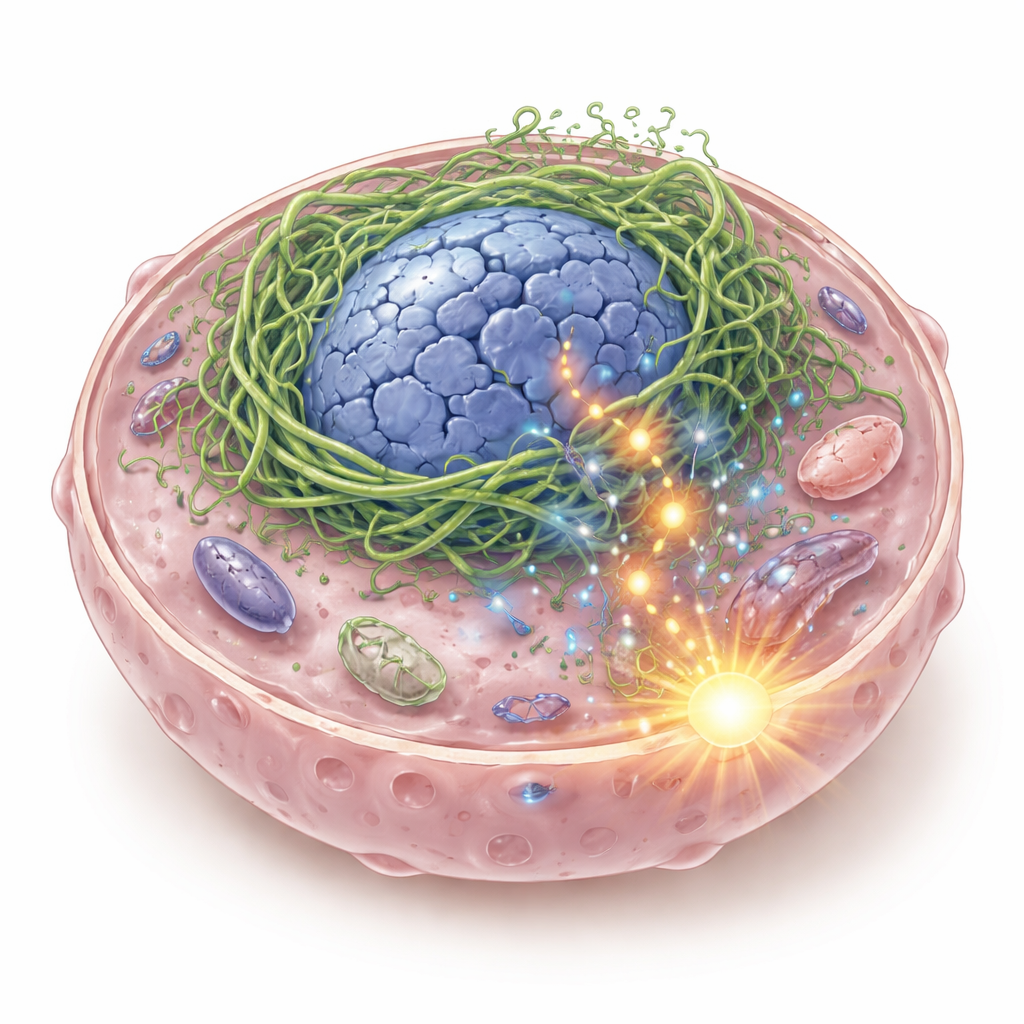
Разрушенный внутренний каркас и его опасные последствия
Внутри каждой клетки есть гибкий каркас из белковых филаментов, который поддерживает форму клетки и её ядра и помогает ей чувствовать физические силы. Авторы сосредоточились на кератинах — семействе каркасных белков, характерных для эпителиальных тканей, в том числе выстилающих ротоглотку. В некоторых плоскоклеточных карциномах головы и шеи они обнаружили гибридный кератин K6-K14/V5, образующийся при слиянии двух генов кератинов. При включении этого белка-слияния в раковых клетках он не формирует ровной поддерживающей сети. Вместо этого он туго сжимается вокруг ядра, деформируя его в полые, уродливые структуры и приводя к разрывам ДНК. Фрагменты ДНК попадают в цитоплазму, где их обнаруживает система иммунного распознавания cGAS–STING, которая обычно даёт сигнал тревоги при наличии вирусной ДНК.
От давления гибели к сокрытому выживанию
Немедленный эффект от этого повреждения ядра вреден для раковых клеток: их рост замедляется, и многие погибают. Однако часть клеток удаётся выжить. Эти выжившие сильно зависят от физических условий среды. На стандартных плоских пластиковых чашках они постепенно исчезают, но при выращивании в мягком коллагеновом геле — ближе по текстуре к настоящей ткани — они сохраняются и вновь появляются как новая популяция, названная 3D-V5. Анализ активности генов показывает, что эти клетки реагируют на продолжающийся сигнал о повреждении ДНК включением аутопhagии — программы самочистки, перерабатывающей повреждённые компоненты, особенно неисправные митохондрии. Эта реакция помогает им перейти в состояние дремоты с низкой активностью, что позволяет выдерживать стресс вместо уничтожения.
Дремлющие клетки перенастраиваются и готовятся к перемещению
Находясь в состоянии дремоты, выжившие клетки незаметно переписывают свои внутренние программы. Они меняют соотношение кератиновых белков и принимают «частичный» эпителиально-мезенхимальный переход (pEMT) — промежуточную идентичность, сохраняющую некоторые эпителиальные черты, но обретающую гибкость и подвижность. Они значительно лучше формируют сферы и посевы новых клеточных колоний — признак стволовости рака. Со временем их механические свойства восстанавливаются: ядра снова уплотняются, восстанавливаются сильные актиновые волокна, и появляются длинные выросты, которые исследуют и захватывают окружающий матрикс. Они также увеличивают выработку матриксных металлопротеиназ (MMP), которые разрушают внеклеточную сеть и прокладывают пути для инвазии.
Общение с соседями для создания поддерживающей ниши
Эти перепрограммированные раковые клетки не действуют в одиночку. Исследователи наблюдали, что 3D-V5 клетки выделяют большое количество крошечных упаковок — внеклеточных везикул — в окружение. Когда эти везикулы контактируют с ближайшими оральными фибробластами (клетками соединительной ткани), фибробласты меняют свою экспрессию генов и становятся похожими на раково-ассоциированные фибробласты, поддерживающие рост опухоли. Многие передаваемые сигналы связаны с осью FGF–FGFR — семейством факторов роста и их рецепторов, известными как драйверы пролиферации, пластичности и резистентности. В культуре и в опухолях у мышей блокирование активности FGFR уменьшало это преимущество роста. В животных опухоли, образованные 3D-V5 клетками, были слабо дифференцированы, более инвазивны, богаты маркерами стволовых клеток и с большей вероятностью распространялись за пределы места инъекции.
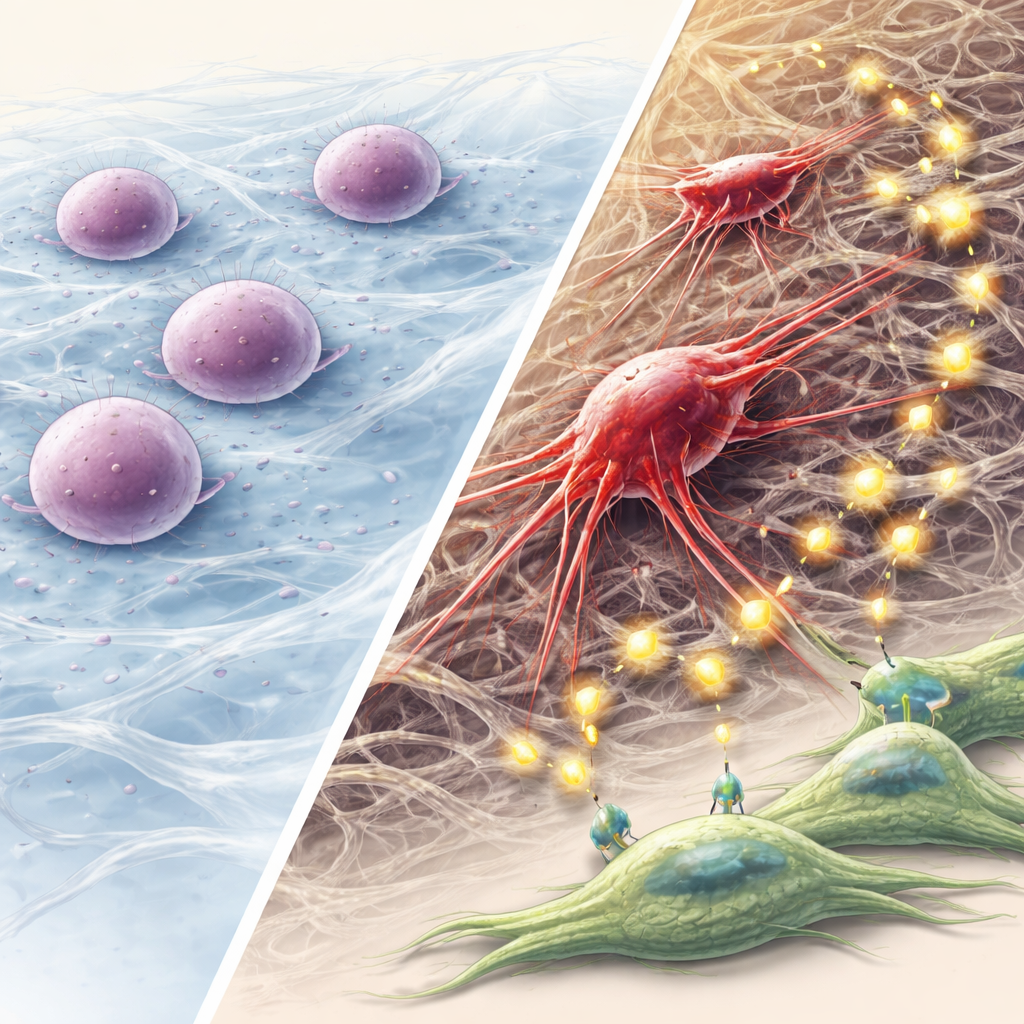
Почему этот механический путь к агрессивному раку имеет значение
Работа предлагает пошаговую модель: слияние кератинов нарушает внутренний каркас клетки, сдавливает ядро и запускает сигнал о повреждении ДНК; аутопhagия затем позволяет немногим клеткам войти в состояние дремоты вместо гибели; со временем эти выжившие реорганизуют свой скелет, приобретают стволоподобные и инвазивные свойства и перестраивают окружение через везикулы и FGF-сигнализацию. Для неспециалистов ключевое послание в том, что физические силы и структурные белки внутри клеток могут быть так же важны, как гены и химические сигналы, в движении эволюции рака. Ориентирование на этот путь «механическое напряжение — аутопhagия — FGF», особенно при раках головы и шеи со слияниями кератинов, может предложить новые стратегии предотвращения пробуждения и распространения дремлющих опухолевых клеток.
Цитирование: Chen, IH., Ravichandran, S., Lai, MT. et al. Cytoskeleton reorganization induced by a novel K6-K14 keratin fusion promotes cancer stemness and cellular plasticity via cGAS-STING selection. Oncogenesis 15, 5 (2026). https://doi.org/10.1038/s41389-026-00598-1
Ключевые слова: стволовость рака, цитоскелет клеток, опухолевая дремота, рак головы и шеи, механотрансдукция