Clear Sky Science · ru
Роль деметилазы гистонов PHF2 как опухолевого супрессора при гепатоцеллюлярной карциноме через регуляцию SRXN1
Почему это исследование рака печени важно
Рак печени — один из самых смертельных видов рака в мире, и существующие лекарства продлевают жизнь лишь незначительно для многих пациентов. В этом исследовании поставлен иной вопрос: вместо того чтобы нацеливаться на известные гены-инициаторы рака, можно ли использовать особенности упаковки ДНК и её химических меток в клетках печени, чтобы найти новые, более точные варианты лечения? Учёные сосредоточились на малоизученном белке PHF2 и выяснили, как он может помогать предотвращать превращение печёночных клеток в раковые.
Поиск уязвимостей в системе контроля рака
Рак обусловлен не только повреждёнными генами; он также подпитывается нарушениями «эпигенетического» контроля — химических меток и белковых комплексов, которые определяют, какие гены включаются и выключаются. При гепатоцеллюлярной карциноме, наиболее распространённой форме рака печени, многие такие регуляторы нарушены. Команда систематически протестировала 497 эпигенетических регуляторов в шести линиях клеток рака печени, используя РНК-инструменты для временного снижения активности каждого регулятора по очереди и затем измеряя выживаемость раковых клеток. Этот большой экран был нацелен на выявление регуляторов, от которых зависят опухоли для роста, и тех, которые обычно действуют как тормоза опухолеобразования.
Поиск новых «ускорителей» и «тормозов» рака
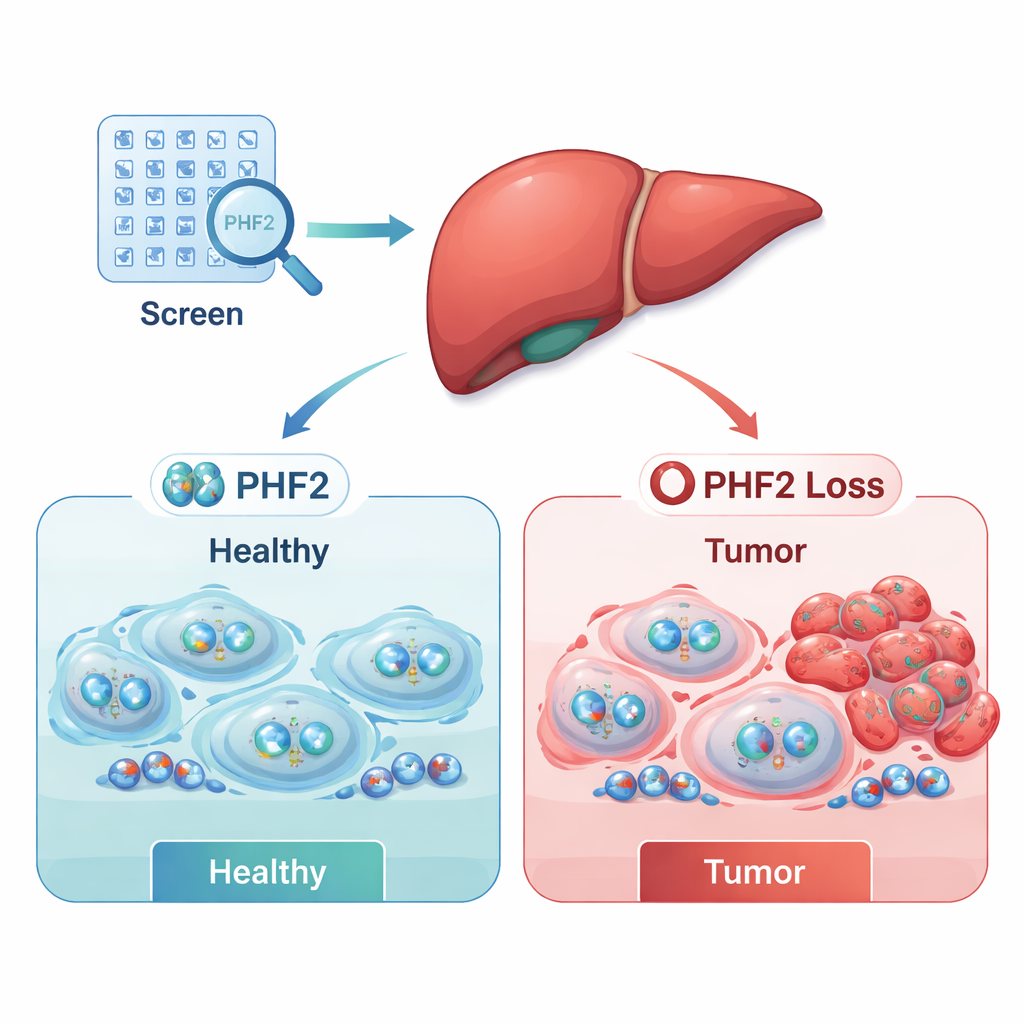
Экран выявил две широкие группы: потенциальные «ускорители» рака (онкогены), потеря которых ухудшала выживание раковых клеток, и потенциальные «тормоза» (опухолевые супрессоры), потеря которых улучшала рост раковых клеток. Сочетая собственные лабораторные данные с крупными публичными клиническими наборами данных, исследователи сузили список до нескольких клинически значимых кандидатов. Два регулятора, SUPT7L и SMARCC1, как правило, были более активны в опухолях и ассоциировались с худшей выживаемостью. Напротив, один регулятор — PHF2 — часто снижался в печёночных опухолях, и у пациентов, чьи опухоли сохраняли более высокий уровень PHF2, обычно наблюдалась более длительная выживаемость. Эти закономерности указывали на то, что PHF2 может действовать как опухолевый супрессор при раке печени у человека.
Как потеря PHF2 меняет поведение печёночных раковых клеток
Чтобы глубже исследовать PHF2, команда создала линии раковых клеток печени с устойчивым снижением этого белка и отслеживала их поведение со временем. Клетки с пониженным уровнем PHF2 росли быстрее и демонстрировали повышенный уровень Ki-67, маркера активного деления клеток, что указывает на то, что PHF2 обычно помогает сдерживать пролиферацию. Эти эффекты были наиболее выражены в уже агрессивных линиях клеток рака печени, что подразумевает: простая потеря PHF2, вероятно, не инициирует рак сама по себе, но может ускорять рост злокачественных клеток после формирования опухоли.
Неожиданная связь с защитой от клеточного стресса
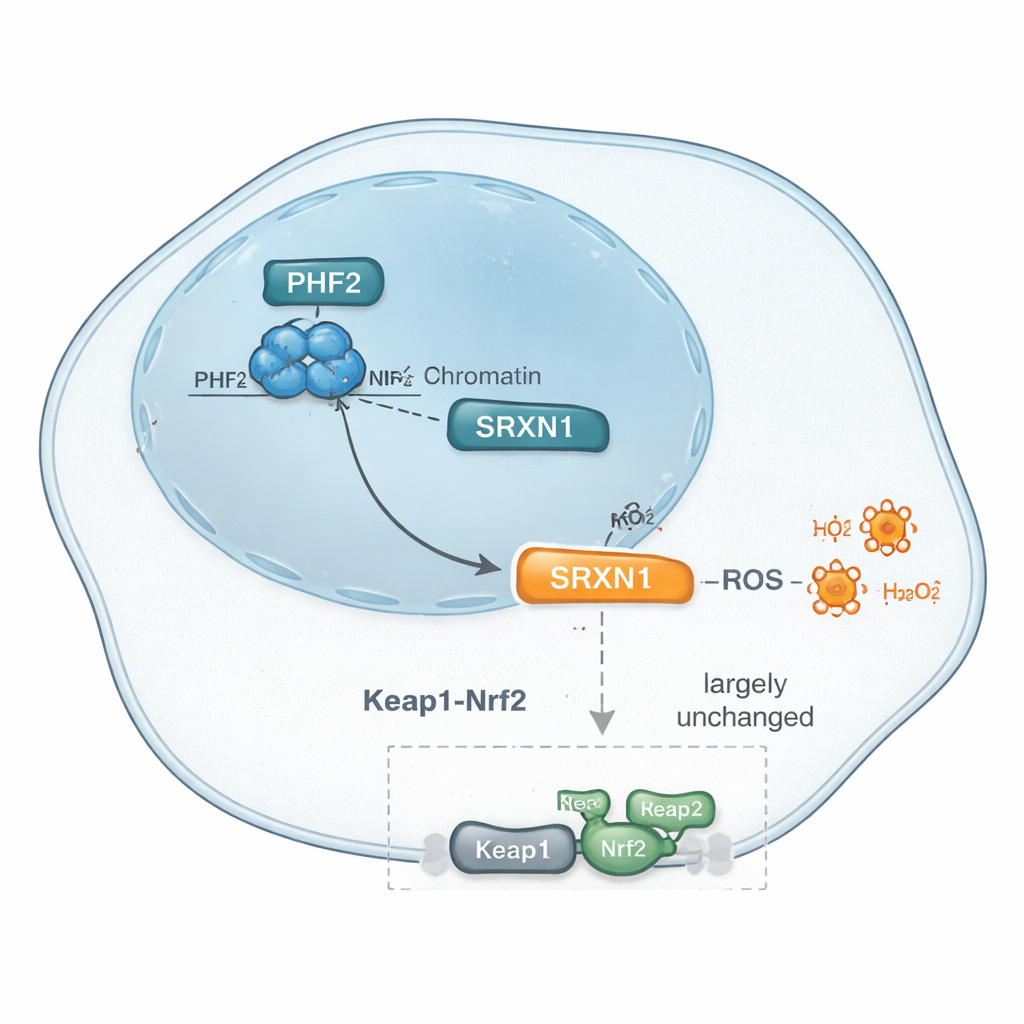
Далее исследователи использовали современные методы протеомного анализа, чтобы каталогизировать тысячи белков, уровни которых менялись при снижении PHF2. Среди многих тонких сдвигов выделялся один паттерн: уровень защищающего от стресса белка SRXN1 последовательно падал при потере PHF2. SRXN1 помогает клеткам справляться с реактивными формами кислорода — химически реактивными побочными продуктами, которые могут повреждать ДНК и белки, но также заставляют раковые клетки адаптироваться. Данные указывали на то, что PHF2 способствует поддержанию уровня SRXN1, и что нарушение этого баланса может влиять на то, как клетки рака печени реагируют на внутренний стресс и, в конечном счёте, как быстро они растут.
Действие в обход известного стрессового пути
Обычно SRXN1 контролируется «мастер-переключателем» ответа на стресс Nrf2, который включает множество антиоксидантных генов при окислительном стрессе. Поскольку SRXN1 снижался при подавлении PHF2, команда проверила, не действует ли PHF2 просто через путь Nrf2. Они исследовали ключевые гены и белки, связанные с Nrf2, обрабатывали клетки препаратами, активирующими Nrf2 путём блокирования его ингибитора Keap1, и использовали генетические инструменты для прямого уменьшения Keap1. Во всех этих тестах ответ клеток с дефицитом PHF2 был похож на ответ нормальных клеток, а анализы путей и факторов транскрипции не выделили Nrf2 как основного участника. Вместо этого в качестве кандидатов всплыли другие факторы, включая ZNF384 и Nrf1 — оба ранее связанные с раком печени. В совокупности свидетельства позволяют предположить, что контроль PHF2 над SRXN1 и антиоксидантными ответами может обходить классическую сигнализацию Nrf2, намекая на отдельный путь регуляции стресса в этих опухолях.
Что это может значить для будущих лечений
Для неспециалиста главное: это исследование выделяет PHF2 как перспективный защитный фактор при раке печени — при наличии и активности PHF2 опухолевые клетки растут медленнее; при его уменьшении они получают преимущество в росте и меняют способы борьбы с клеточным стрессом. Поскольку сам PHF2 может быть трудно прямо заблокировать или стимулировать традиционными малыми молекулами, авторы указывают на развивающиеся стратегии, такие как РНК-ориентированные терапии или препараты, усиливающие активность PHF2 через его верхнеуровневые сигнальные партнёры. Они также подчёркивают, что эффекты PHF2 зависят от контекста — его влияние может варьироваться в зависимости от других мутаций, например статуса p53 — поэтому любая будущая терапия, вероятно, потребует тщательного отбора пациентов. В целом работа уточняет понимание того, как эпигенетические регуляторы формируют поведение рака печени, и открывает новые пути для разработки методов лечения, восстанавливающих или имитирующих опухолево-супрессивное влияние PHF2.
Цитирование: Thng, D.K.H., Hooi, L., Yong, W.K. et al. The role of histone demethylase PHF2 as a tumour suppressor in hepatocellular carcinoma by regulating SRXN1. Oncogenesis 15, 6 (2026). https://doi.org/10.1038/s41389-026-00597-2
Ключевые слова: гепатоцеллюлярная карцинома, эпигенетическая регуляция, PHF2, SRXN1, терапия рака печени