Clear Sky Science · ru
Деградация HILPDA посредством TRIM21 преодолевает устойчивость к иммунотерапии anti‑PD‑1 при раке молочной железы за счёт ограничения палмитоилирования PD‑L1
Почему некоторые противораковые иммунотерапии перестают работать
Препараты, которые «развязывают» иммунную систему, такие как терапии anti–PD‑1, изменили подход к лечению ряда онкопатологий, в том числе агрессивных форм рака молочной железы. Тем не менее многие опухоли либо изначально не реагируют, либо со временем находят способы уклониться. В этом исследовании изучён один из таких путей уклонения при тройной‑негативной раке молочной железы и показано, как перенастройка липидного обмена опухоли — а также перепрофилированный препарат фенретинид — могут вновь открыть дорогу иммунной системе, когда стандартная иммунотерапия не срабатывает. 
Скрытый помощник, защищающий опухоли
Исследователи сосредоточились на малоизвестном белке HILPDA, ранее связывавшемся с тем, как клетки управляют липидами при стрессе. Сравнив мышечные опухоли молочной железы, сохранявшие чувствительность к терапии anti‑PD‑1, и опухоли, ставшие резистентными, они обнаружили, что уровни HILPDA были значительно выше в резистентных раках. Анализы больших баз данных пациентов и образцов опухолей женщин с раком молочной железы подтвердили, что HILPDA более выражен в опухолях по сравнению с нормальной тканью молочной железы, особенно при тройной‑негативной форме, и что у пациентов с более высоким экспрессированием HILPDA прогноз, как правило, хуже. Опухоли у людей, которые не получили пользы от блокировки PD‑1, также содержали больше HILPDA, что напрямую связывает этот белок с неэффективностью лечения.
Как опухоли обращают иммунный ландшафт против нас
Чтобы понять, что именно делает HILPDA в опухолях, команда модифицировала раковые клетки молочной железы так, чтобы они либо сверхэкспрессировали белок, либо были лишены его, а затем выращивала их вместе с человеческими иммунными клетками или в мышах. При высоком уровне HILPDA опухоли привлекали больше регуляторных Т‑клеток, миелоид‑подавляющих клеток и макрофагов типа M2 — типов иммунных клеток, которые ослабляют атаку и помогают опухолям скрываться. В то же время число и активность киллера CD8 Т‑клеток и естественных киллеров снижались, их способность выделять токсичные молекулы и провоспалительные сигналы была подавлена. Подавление HILPDA обращало эту картину: в опухолях меньше было супрессивных клеток, больше — активных киллеров, замедлялся рост и уменьшалось число метастазов. Критически важно, что при лечении животных с низким уровнем HILPDA терапией anti‑PD‑1 их опухоли сокращались сильнее, а животные жили дольше, что демонстрирует роль HILPDA в контроле эффективности иммунотерапии.
Синтез жиров, молекулярная броня и уклонение от иммунитета
Углубившись, учёные выяснили, как HILPDA перестраивает метаболизм опухоли, чтобы укрепить её иммунную защиту. Внутри раковых клеток HILPDA связывается с шаперонным белком HSP90, стабилизируя транскрипционный фактор KLF5, который стимулирует синтез липидов. Это трио усиливает образование жирных кислот, особенно палмитата, и заполняет клетки опухоли липидными каплями. Один из этих жирных компонентов затем присоединяется к PD‑L1 — контрольному белку на поверхности опухоли, посылающему иммунным клеткам сигнал «не атаковать». Команда показала, что присоединение палмитата к конкретному участку PD‑L1 действует как молекулярный клей: оно помогает PD‑L1 устойчиво локализоваться в мембране клетки и препятствует его разрушению. Мутация этой единственной точки присоединения лишала PD‑L1 устойчивости и ослабляла его способность защищать клетки, даже при высоком уровне HILPDA. Иными словами, HILPDA‑зависимое производство липидов подпитывает химическую модификацию PD‑L1, превращая иммунную защиту опухоли из непрочной в усиленную.
Встроенный тормоз, который можно задействовать
У каждого ускорителя есть и тормоз, и здесь им выступает другой белок — TRIM21. Авторы обнаружили, что TRIM21 распознаёт HILPDA и помечает его молекулярными «флажками», отправляющими его в механизмы утилизации клетки. В опухолях молочной железы у пациентов уровни TRIM21, как правило, были низкими при высоком HILPDA, и низкий TRIM21 связывался с плохим прогнозом, что указывает на ослабление этой природной системы торможения при раке. Команда затем искала препараты, способные усилить TRIM21, и выявила фенретинид — ретиноид, уже испытанный на людях. В клеточных и животных моделях тройной‑негативной рака молочной железы фенретинид усиливал активность TRIM21, ускорял разрушение HILPDA, снижал синтез липидов и защитную модификацию PD‑L1, а также замедлял рост и распространение опухоли. Наиболее впечатляюще, сочетание фенретинида с терапией anti‑PD‑1 делало опухоли более уязвимыми для иммунной атаки, увеличивая число киллер‑Т и естественных киллеров и снижая количество супрессивных клеток в микросреде опухоли. 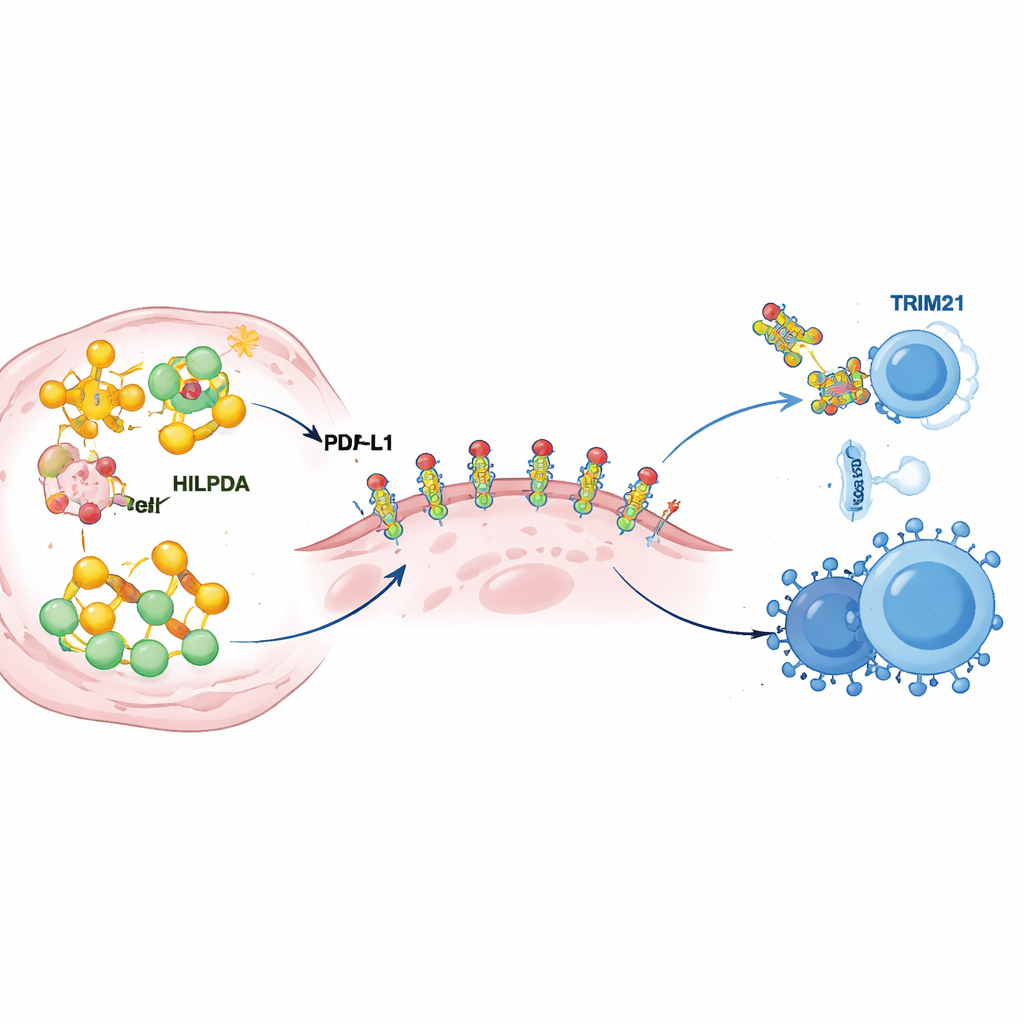
Что это значит для будущего лечения рака
Эта работа выявляет цепочку событий, в которой напряжённые раковые клетки молочной железы повышают HILPDA, усиливают синтез липидов и химически укрепляют PD‑L1 на своей поверхности, что позволяет им продолжать подавлять иммунные клетки даже при наличии блокаторов PD‑1. TRIM21 действует как внутренний предохранитель, способный распускать HILPDA, но в опухолях он часто слишком слаб. Открытие того, что фенретинид может реактивировать этот предохранитель, указывает на практический подход — сочетание метаболического препарата с существующей иммунотерапией для преодоления резистентности. Если эти результаты подтвердят клинические испытания, нацеливание на ось TRIM21–HILPDA–PD‑L1 может дать пациентам с трудноизлечимой тройной‑негативной раком молочной железы второй шанс на пользу от иммунных методов лечения.
Цитирование: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
Ключевые слова: тройная‑негативная рак молочной железы, устойчивость к иммунотерапии, палмитоилирование PD‑L1, липообмен опухоли, фенретинид