Clear Sky Science · ru
L1TD1 способствует прогрессированию муцинозной аденокарциномы толстой кишки за счёт повышения стабильности мРНК ABCC3
Почему этот слизистый тип рака важен
Рак толстой кишки является одной из ведущих причин смерти от рака в мире. В составе этого заболевания выделяется особый подтип — муцинозная аденокарцинома, опухоли при котором заполнены густой слизью, составляющей более половины массы опухоли. Этот скользкий барьер может помогать канцерогенным клеткам уклоняться от химиотерапии и иммунной защиты организма. В работе поставлен фундаментальный, но важный вопрос: что контролирует образование этой слизи, и можно ли подавить этот процесс, чтобы замедлить рост опухоли и повысить эффективность лечения?
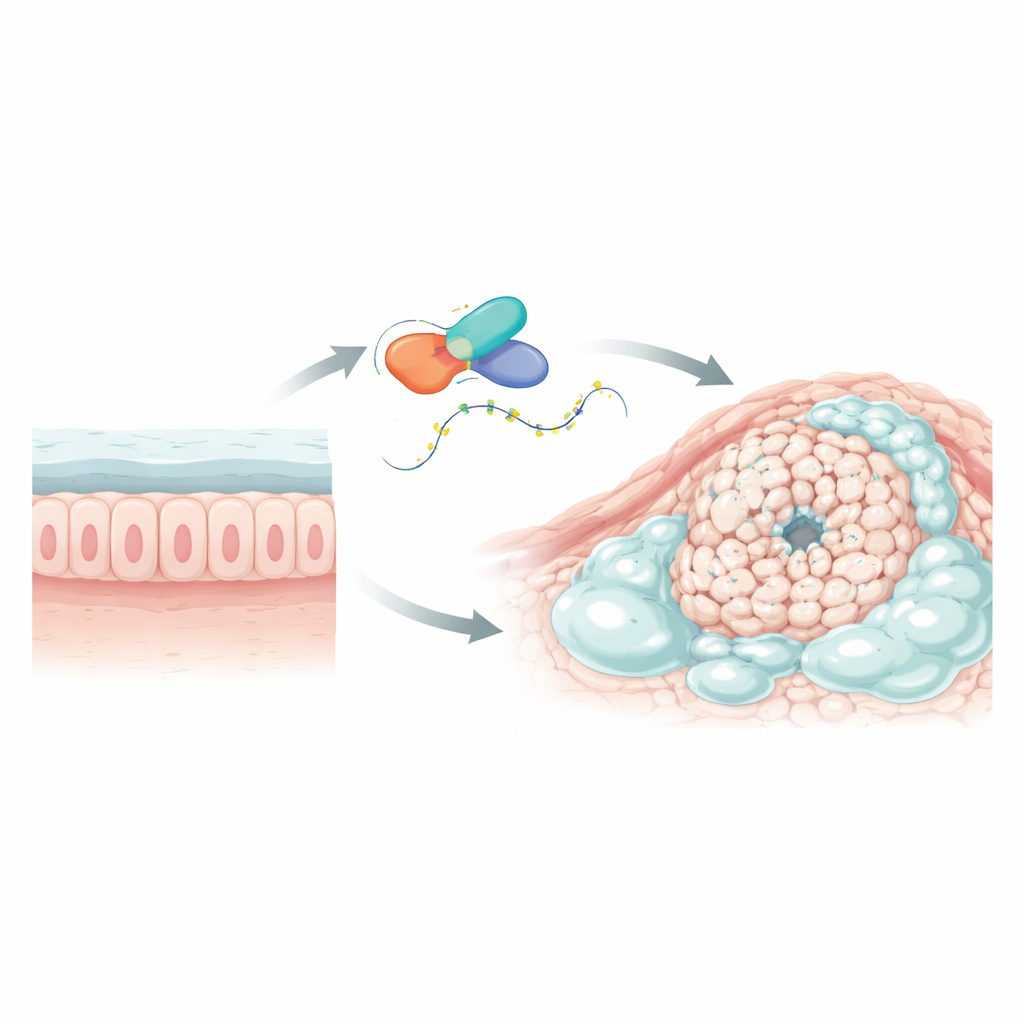
Поиск ключевого проблемного гена
Исследователи сначала проанализировали крупные онкологические базы данных и данные одиночноклеточного секвенирования, чтобы выделить гены, экспрессия которых отличается в слизистых опухолях толстой кишки по сравнению с обычными колоректальными карциномами и прилегающей нормальной тканью. Один ген, обозначенный L1TD1, явно выделялся. Его экспрессия была заметно повышена в муцинозных опухолях, но не в обычных, и выше в опухолевой ткани по сравнению с окружающей нормальной слизистой. L1TD1 кодирует белок, связывающийся с РНК — молекулой, которая переносит генетические инструкции от ДНК к аппарату синтеза белка. Поскольку РНК-связывающие белки могут тонко регулировать продолжительность жизни сообщений и силу их считывания, L1TD1 выглядел сильным кандидатом на роль ключевого регулятора в этих слизистых опухолях.
Как L1TD1 стимулирует рост и метастазирование
Чтобы проверить эффект L1TD1, команда использовала клеточные линии рака толстой кишки и модели на мышах. При повышении уровня L1TD1 клетки делились активнее, лучше мигрировали и агрессивнее пронизывали барьеры, имитирующие ткань. Понижение экспрессии L1TD1 оказывало противоположный эффект: рост замедлялся, инвазия снижалась. У мышей, которым вводили клетки с высоким уровнем L1TD1, опухоли росли крупнее и чаще давали метастазы в печень и брюшную полость. В клинических образцах повышенная экспрессия L1TD1 ассоциировалась с более крупными опухолями, худшей дифференцировкой и более поздними стадиями заболевания, связывая этот ген с более агрессивным течением болезни.
Включение слизи и лекарственной устойчивости
Слизь оказалась ключевым звеном в действии L1TD1. Клетки с повышенным L1TD1 продуцировали больше основных муцинов, особенно MUC2 и MUC5AC, и проявляли признаки бокаловидных клеток — нормальных секреторных клеток кишечника. Трёхмерные культуры и окрашивание тканей у пациентов и мышей подтвердили, что высокий L1TD1 сопровождается более густой и обильной слизью. Важно, что слизь не была просто сопутствующим явлением: при селективном снижении MUC2 дополнительные эффект роста, инвазии и устойчивости к химиотерапии, вызванные L1TD1, в значительной степени исчезали. Клетки с высоким L1TD1 было сложнее уничтожить распространённым препаратом оксалиплатином, а опухоли с такими клетками меньше сокращались у леченных мышей — что подчёркивает роль слизи как защитного щита, который способствует созданию L1TD1.
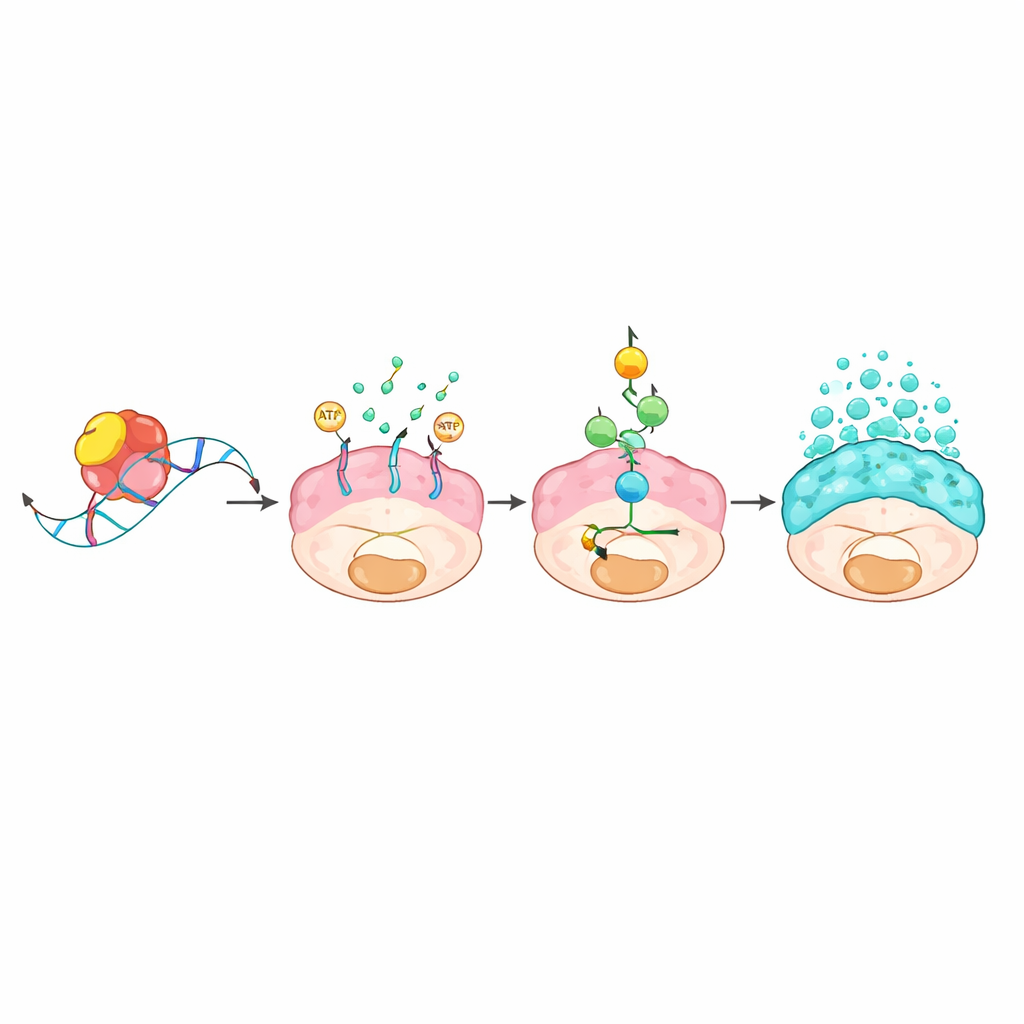
Молекулярная цепочка от контроля РНК к слизе
Далее команда выясняла, как РНК-связывающий белок может вызывать такие выраженные изменения. Путём «выловливания» РНК, физически связанных с L1TD1, и сравнения активности генов при наличии и отсутствии L1TD1 они выделили ген транспортёра ABCC3 как главный мишень. L1TD1 связывался с коротким мотивом «GUGU» в хвостовой части мРНК ABCC3, стабилизируя её и увеличивая синтез белка ABCC3, известного как MRP3. Этот транспортёр находится в клеточной мембране и использует энергию для выкачивания веществ из клетки. Вызванный этим расход энергии активировал метаболический сигнальный сенсор AMPK, который в свою очередь включал классический путь роста и стрессового ответа MAPK. Активация этой каскадной цепочки усиливала производство и секрецию муцинов и укрепляла способность раковых клеток к росту, миграции и лекарственной устойчивости. Генетическое подавление ABCC3 или его блокада экспериментальным соединением, а также ингибирование пути MAPK ослабляли продукцию слизи и снижали агрессивность опухолей.
Что это значит для пациентов
В целом исследование выявляет пошаговую систему контроля для слизистых форм рака толстой кишки: L1TD1 стабилизирует мРНК ABCC3, ABCC3 истощает клеточную энергию, активируется путь AMPK–MAPK, и опухоль отвечает сверхпродукцией слизи с усилением агрессии и лекарственной устойчивости. Для пациентов это открывает несколько перспективных направлений. Уровни L1TD1 и ABCC3 могут помочь идентифицировать опухоли с худшим прогнозом или склонные к резистентности к стандартной химиотерапии. Ещё важнее, что препараты, прерывающие взаимодействие L1TD1 и ABCC3, блокирующие насосную активность MRP3 или нацеленные на гормональную/сигнальную каскаду MAPK, потенциально могут истончить слизистый барьер, замедлить рост опухоли и повысить эффективность существующих терапий при этой трудной форме колоректального рака.
Цитирование: He, H., Yuan, J., Wang, H. et al. L1TD1 promotes colorectal mucinous adenocarcinoma progression by enhancing ABCC3 mRNA stability. Oncogene 45, 1071–1086 (2026). https://doi.org/10.1038/s41388-026-03716-w
Ключевые слова: муцинозный рак толстой кишки, L1TD1, ABCC3 MRP3, продукция слизи, химиоретистентность