Clear Sky Science · ru
Многофункциональная РНК-хеликаза DDX39A стимулирует прогрессирование глиобластомы, модулируя альтернативный сплайсинг WISP1, что индуцирует иммуносупрессивную поляризацию макрофагов
Почему это исследование рака мозга важно
Глиобластома — один из самых смертельных видов рака мозга, известный своими рецидивами после лечения и устойчивостью к лекарствам. В этом исследовании показано, как один молекулярный «переключатель» в опухолевых клетках не только способствует росту опухоли, но и убеждает соседние иммунные клетки прекратить борьбу и начать защищать опухоль. Проследив эту цепочку событий, авторы также выявили уже существующий антипсихотический препарат, который можно было бы перепрофилировать, чтобы разорвать эту вредную сеть.
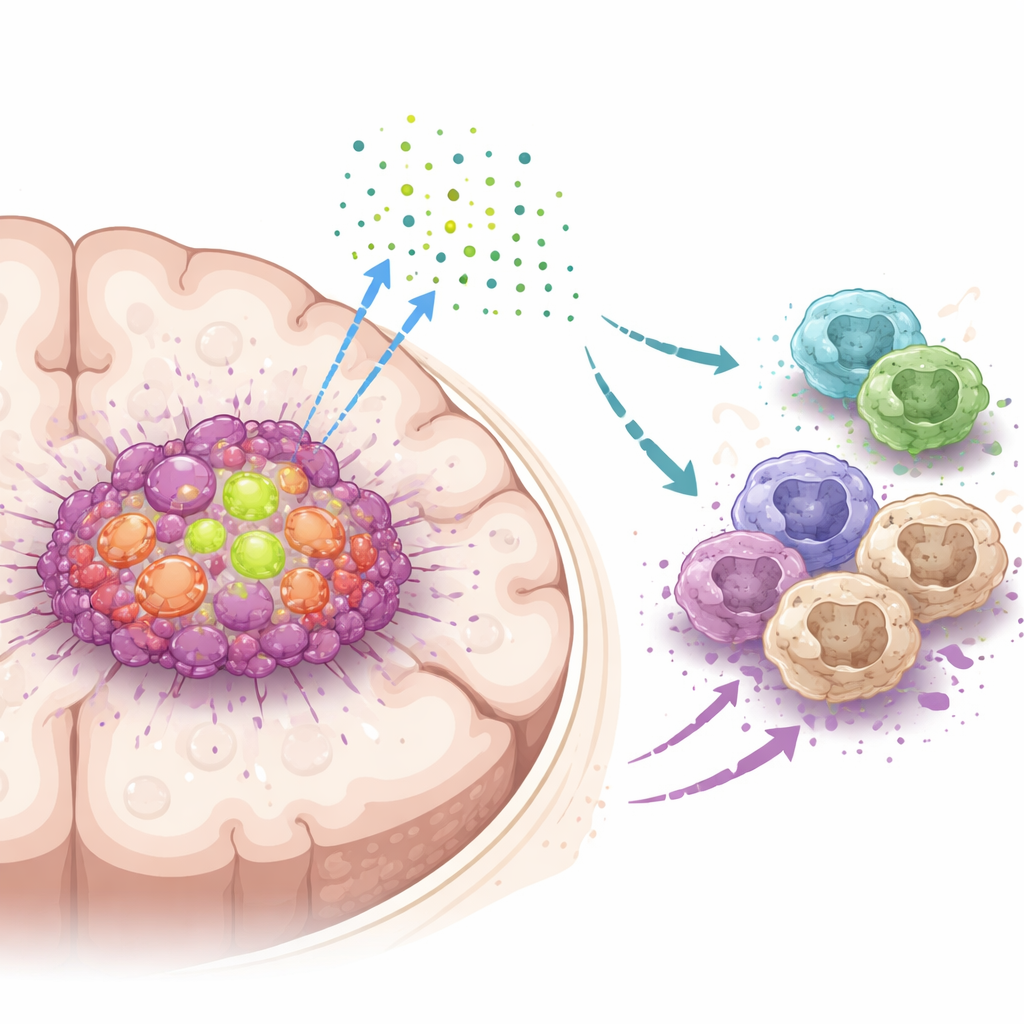
Ключевой помощник внутри клеток опухоли мозга
Команда сосредоточилась на белке DDX39A — молекулярной машине, помогающей клеткам обрабатывать РНК, рабочую копию генетической информации. Анализ больших наборов данных пациентов и образцов опухолей показал, что DDX39A гораздо активнее в глиобластоме по сравнению с нормальной мозговой тканью, а его уровни повышаются с увеличением степени злокачественности. Одноклеточные анализы продемонстрировали, что DDX39A особенно обилен в быстро делящихся опухолевых клетках и в определённых иммунных клетках — макрофагах — внутри опухолевой массы. У пациентов с более высоким содержанием DDX39A в опухолях наблюдались худшие прогнозы, что указывает на тесную связь этого белка с агрессивным течением болезни.
Как этот помощник подпитывает рост и распространение
Чтобы проверить, что именно делает DDX39A, исследователи использовали генетические инструменты для его подавления в стволоподобных клетках глиобластомы, выращенных в лаборатории, и в моделях опухоли мозга у мышей. При снижении DDX39A клетки опухоли росли медленнее, реже прорастали в окружающие ткани и чаще проходили программируемую клеточную гибель. Стволоподобные опухолевые клетки также утратили значительную часть способности формировать новые опухолевые сферы — признак нарушенного самообновления. У мышей опухоли с пониженным уровнем DDX39A были меньше, а животные жили дольше, что подтверждает, что этот белок активно стимулирует прогрессирование опухоли, а не только является её маркером.
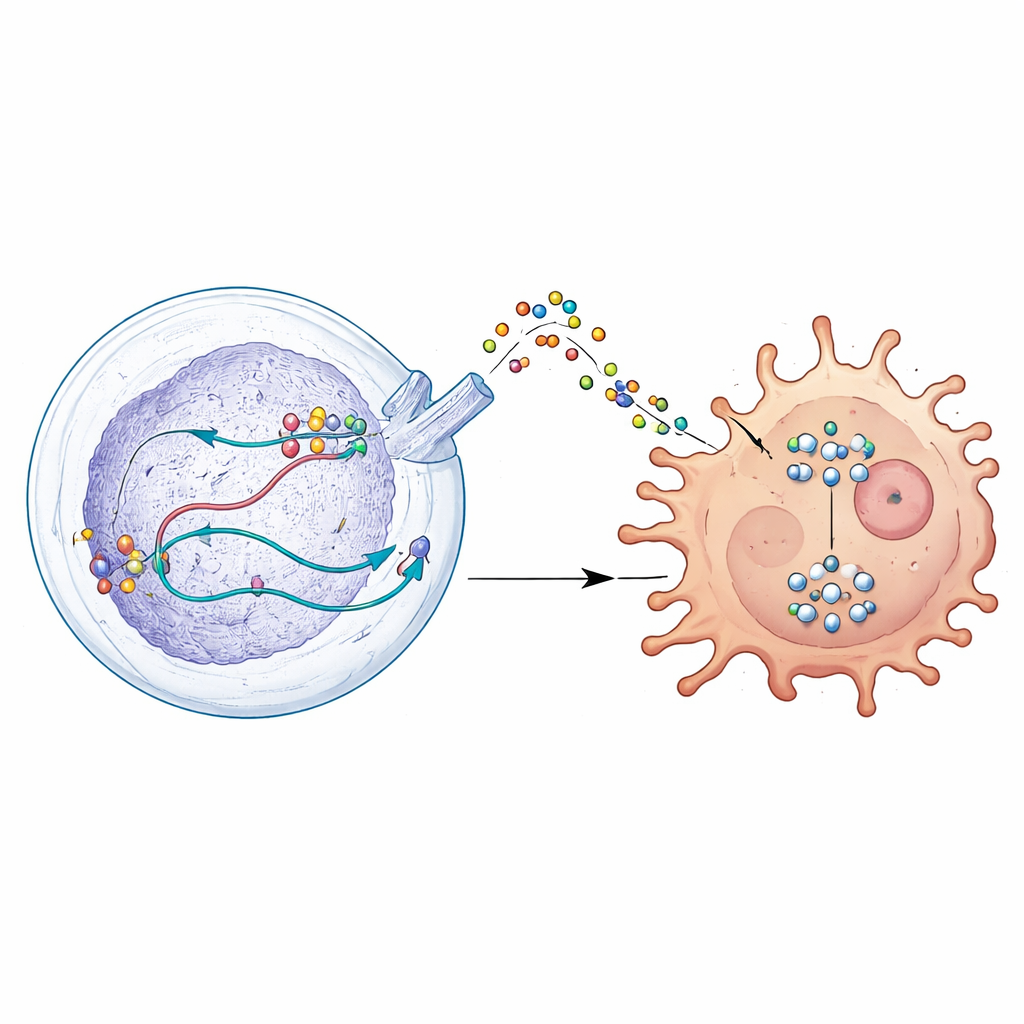
Секретный сигнал, обезоруживающий иммунных защитников
Углубившись дальше, учёные обнаружили, что DDX39A меняет обработку гена WISP1. Вместо простого включения или выключения WISP1, DDX39A формирует его РНК так, что сообщение стабилизируется и повышается синтез белка WISP1. Затем опухолевые клетки выделяют WISP1 в окружение, где он действует как обманчивый маяк. Ближайшие макрофаги, которые могут как атаковать опухоль, так и поддерживать её, реагируют на этот сигнал переходом в иммуносупрессивное состояние, помогающее опухоли. Этот сдвиг опосредуется активацией внутриклеточного пути контроля роста, известного как AKT. При снижении DDX39A или WISP1 активность этого пути уменьшалась, опухолевые клетки становились менее агрессивными, а макрофаги возвращались к более противоопухолевому фенотипу.
Превращение психиатрического препарата в оружие против рака
Имея карту этого пути, исследователи искали в базах данных препараты, которые могли бы помешать активности DDX39A. Они сосредоточились на флуфеназине — давно применяемом антипсихотике, который проникает в мозг. Компьютерное моделирование и тесты связывания показали, что флуфеназин может непосредственно связываться с DDX39A. В опухолевых клетках препарат ослаблял связывание DDX39A с РНК WISP1, снижал уровни WISP1 и уменьшал сигналы по пути AKT. Обработанные клетки росли меньше, реже инвазивно прорастали, образовывали меньше опухолевых сфер и были более склонны к гибели. В модельных животных флуфеназин замедлял рост опухоли мозга, уменьшал число макрофагов, поддерживающих опухоль, и увеличивал выживаемость — при этом применялся в дозах, сопоставимых с уже используемыми у людей для других показаний.
Что это означает для будущего лечения
Проще говоря, исследование показывает, что клетки глиобластомы используют DDX39A, чтобы тонко настроить сообщение (WISP1), которое одновременно повышает их живучесть и перепрограммирует соседние иммунные клетки в телохранителей, а не бойцов. Блокирование этого помощника — генетически или с помощью препарата вроде флуфеназина — ослабляет рак по двум направлениям: поражает сами опухолевые клетки и разрушает защитный щит из иммуносупрессивных макрофагов. Хотя до клинического применения этой стратегии необходимо значительно больше проверок, работа открывает перспективный путь для перепрофилирования известного лекарства против недавно выявленной уязвимости в одном из самых упорных раков мозга.
Цитирование: Zhang, Y., Xue, Z., Zhang, N. et al. The multifunctional RNA helicase DDX39A drives glioblastoma progression by modulating WISP1 alternative splicing that induces an immunosuppressive macrophage polarization. Oncogene 45, 1026–1041 (2026). https://doi.org/10.1038/s41388-026-03715-x
Ключевые слова: глиобластома, РНК-сплайсинг, опухолевый микроокружение, поляризация макрофагов, повторное применение лекарств