Clear Sky Science · ru
PMM2 взаимодействует с TRIM28 для привлечения E2F4 и стимулирования KIFC3-опосредованного опухолевого гликолиза и прогрессии колоректального рака
Почему эта история о раке важна
Колоректальный рак — один из самых смертоносных видов рака в мире, отчасти потому, что многие опухоли учатся перехватывать энергетические системы организма, чтобы подпитывать бесконтрольный рост. В этом исследовании показано, как малоизвестный фермент PMM2 помогает колоректальным опухолям активнее «сжигать» сахар и распространяться, и почему это делает его перспективной новой мишенью для будущих препаратов и диагностических тестов.
Опухолевый двигатель, жаждущий сахара
Клетки рака часто перенастраивают способ использования глюкозы, отдавая предпочтение высокоскоростному, но малоэффективному способу ее «сжигания», известному как гликолиз. Исследователи начали с сравнения тысяч генов в образцах колоректальных опухолей и прилежащих здоровых тканей. PMM2, фермент, обычно участвующий в присоединении сахарных цепочек к белкам, выделялся как один из самых значительно повышенных генов в раке. Клетки опухоли с повышенным уровнем PMM2 росли быстрее, формировали больше колоний и легче распространялись в лабораторных условиях, тогда как клетки с выключенным PMM2 замедляли рост, меньше мигрировали и были более склонны к гибели.
Как опухолевые клетки форсируют потребление сахара
Когда команда уменьшала уровни PMM2 в клетках колоректального рака, клетки поглощали меньше глюкозы, вырабатывали меньше АТФ (их основной энергетический «валюты») и выделяли меньше лактата — побочного продукта гликолиза. Чувствительные метаболические измерения подтвердили, что общая закисление окружающей среды снизилось, в то время как потребление кислорода возросло, что означает сдвиг от ускоренного гликолиза в сторону более нормального дыхания. Ключевые белки-помощники гликолиза, PKM2 и LDHA, также уменьшились. Удивительно, но даже каталитически «мертвая» версия PMM2 могла поддерживать такое «сахарное» поведение, что показывает: роль PMM2 в раке зависит не от его обычной химической активности, а от того, с кем он взаимодействует внутри клетки.
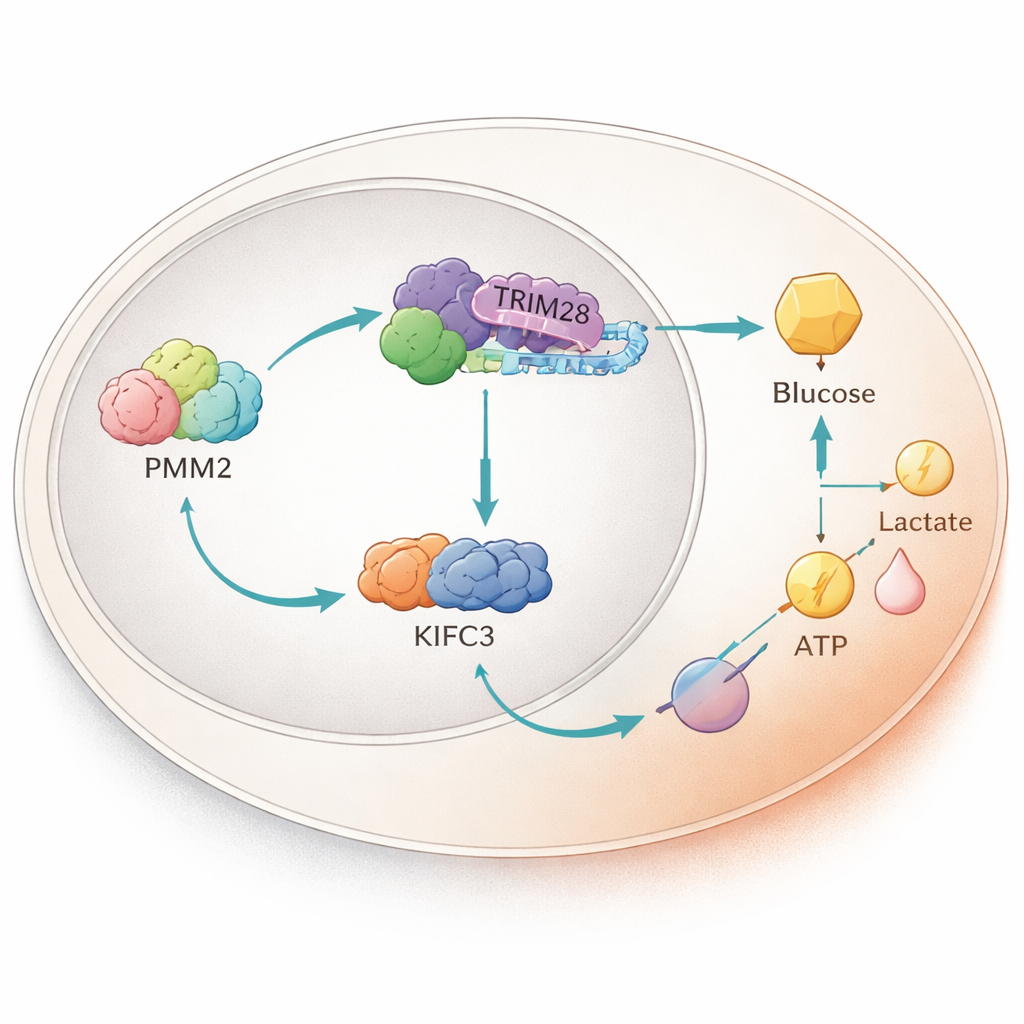
Белковая эстафета в ядре
При дальнейшем изучении ученые обнаружили, что PMM2 физически связывается с другим белком — TRIM28, который способен перемещаться в клеточное ядро и влиять на активность генов. PMM2 способствует накоплению TRIM28 в ядре, где TRIM28 объединяется с транскрипционным фактором E2F4. Вместе эта троица усиливает продукцию моторного белка KIFC3, связываясь с определенным участком его регуляторной ДНК. Эксперименты с удалением участка PMM2, необходимого для связывания с TRIM28, лишали PMM2 способности усиливать гликолиз и рост клеток, что подчеркивает: именно это белковое партнерство — а не классическая ферментная функция PMM2 — дает опухоли преимущество.
Включение ключевого метаболического переключателя
KIFC3, более известный по роли в транспортировке «груза» вдоль внутреннего каркаса клетки, оказался критическим метаболическим переключателем. При понижении уровней KIFC3 клетки колоректального рака потребляли меньше глюкозы, вырабатывали меньше АТФ и лактата и демонстрировали сниженную гликолитическую активность, тогда как потребление кислорода увеличивалось. Важно, что подавление KIFC3 частично нейтрализовало усиление гликолиза и преимущества в росте, вызываемые PMM2. У мышей, трансплантированных человеческими клетками колоректального рака, опухоли с повышенным PMM2 росли быстрее, но этот эффект был ослаблен при снижении KIFC3. Образцы опухолей от этих животных показывали повышенные уровни PMM2, KIFC3 и маркеров гликолиза, связывая всю цепочку событий в живой ткани.
От лабораторных моделей к образцам пациентов
Чтобы приблизить работу к клинике, команда создала миниатюрные трехмерные опухоли — органоиды — из образцов колоректального рака пациентов. Органоиды с более высокими уровнями PMM2 и KIFC3 росли быстрее и вырабатывали больше АТФ и лактата, чем органоиды с низкими уровнями. Принудительная экспрессия PMM2 в органоидах усиливала KIFC3 и гликолиз, тогда как снижение PMM2 давало противоположный эффект. Анализ массивов опухолей пациентов дополнительно показал, что высокий уровень PMM2 коррелирует с более продвинутой стадией заболевания, поражением лимфоузлов и более короткой общей выживаемостью, что делает PMM2 сильным кандидатом на роль биомаркера.
Что это значит для будущего лечения
Проще говоря, исследование показывает, что многие колоректальные опухоли, по-видимому, подключают PMM2 к ядерной белковой «эстафете» — через TRIM28 и E2F4 — чтобы усилить KIFC3 и, как следствие, свою систему «сжигания» сахара. Этот метаболический всплеск помогает раку расти и метастазировать. Поскольку этот путь опирается на белковые взаимодействия, а не на классическую ферментную функцию PMM2, он открывает новые возможности для терапии: малые молекулы, пептиды или препараты-дегрейдеры, нарушающие связывание PMM2 с TRIM28, блокирующие доступ E2F4 к ДНК или подавляющие активность KIFC3, теоретически могут лишить опухоли предпочитаемого топлива. Хотя такие методы лечения пока недоступны, цепочка PMM2–TRIM28–E2F4–KIFC3 теперь выделяется как перспективная дорожная карта для более точечных и ориентированных на метаболизм стратегий борьбы с колоректальным раком.
Цитирование: Peng, Z., Ma, B., Song, Z. et al. PMM2 interacts with TRIM28 to recruit E2F4 and promote KIFC3-mediated tumor glycolysis and colorectal cancer progression. Oncogene 45, 1145–1160 (2026). https://doi.org/10.1038/s41388-026-03707-x
Ключевые слова: колоректальный рак, метаболизм опухоли, гликолиз, онкогенный сигнальный путь, биомаркер