Clear Sky Science · ru
ULK1 способствует прогрессированию метастазов в экспериментальных моделях эпителиального рака яичника
Почему это исследование важно
Эпителиальный рак яичников часто обнаруживают лишь после того, как он незаметно распространился по брюшной полости, что делает его одним из самых смертельных онкологических заболеваний у женщин. Ключевой этап этого распространения — образование крошечных скоплений опухолевых клеток, называемых сфероидами, которые плавают в брюшной жидкости, выдерживают химиотерапию и дают начало новым опухолям. В работе поставлен конкретный, но важный вопрос: помогает ли клеточный «выключатель выживания» ULK1 этим кластерам выживать и распространяться, и может ли его подавление открыть новые подходы к лечению распространённого рака яичников?
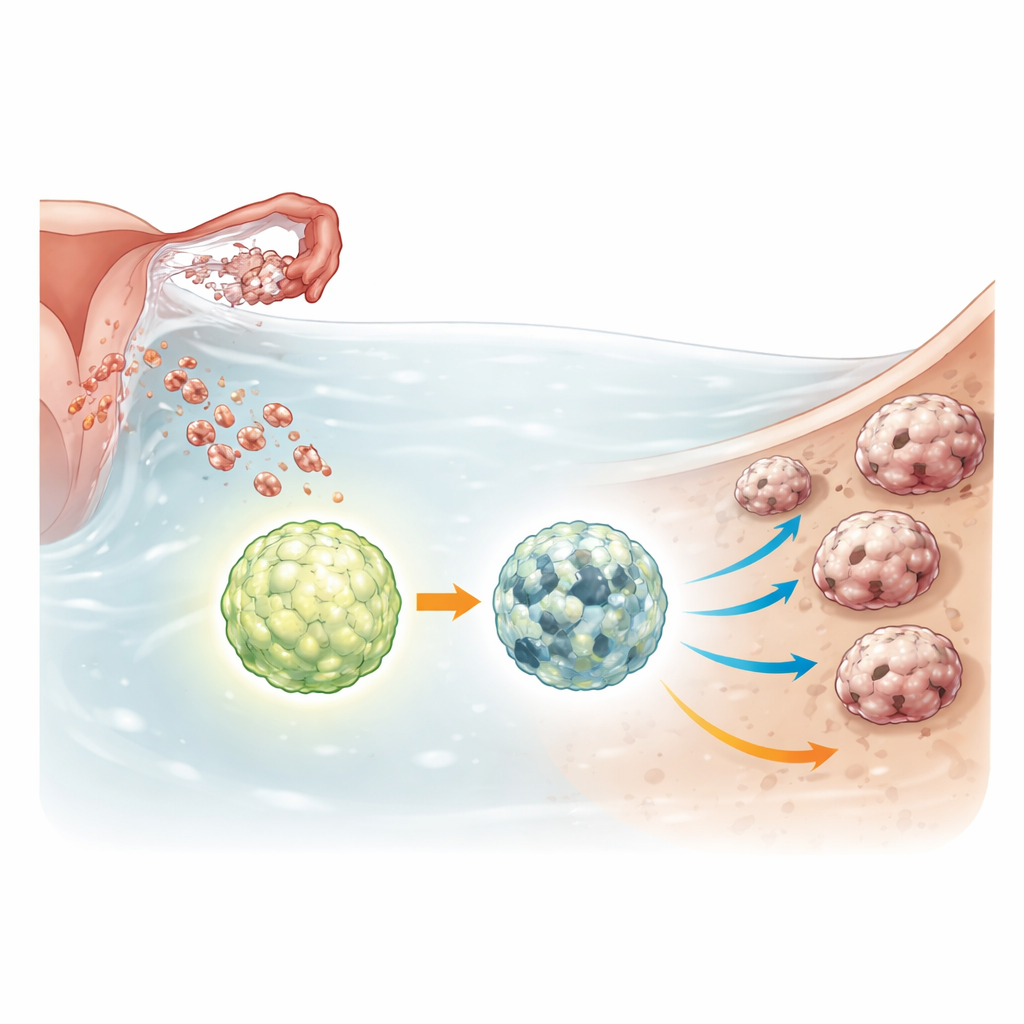
Выключатель выживания внутри опухолевых кластеров
Сфероиды рака яичников переносят неблагоприятные условия: бедность питательными веществами, отсутствие прикрепления и воздействие химиотерапии. Чтобы справляться с этим, они усиливают процесс утилизации и переработки внутренних компонентов — аутофагию, которая поддерживает клетки в стрессовых условиях. ULK1 — главный регулятор, запускающий эту систему переработки. Исследователи с помощью инструментов редактирования генов полностью удалили ULK1 из нескольких линий раковых клеток яичников и из незлокачественной линии клеток фаллопиевой трубы, представляющей ранние предраковые стадии. Затем они сравнили, как ведут себя нормальные и лишённые ULK1 клетки при росте в виде свободно плавающих сфероидов или в виде трёхмерных мини-опухолей — органоидов.
Что происходит при выключении переключателя
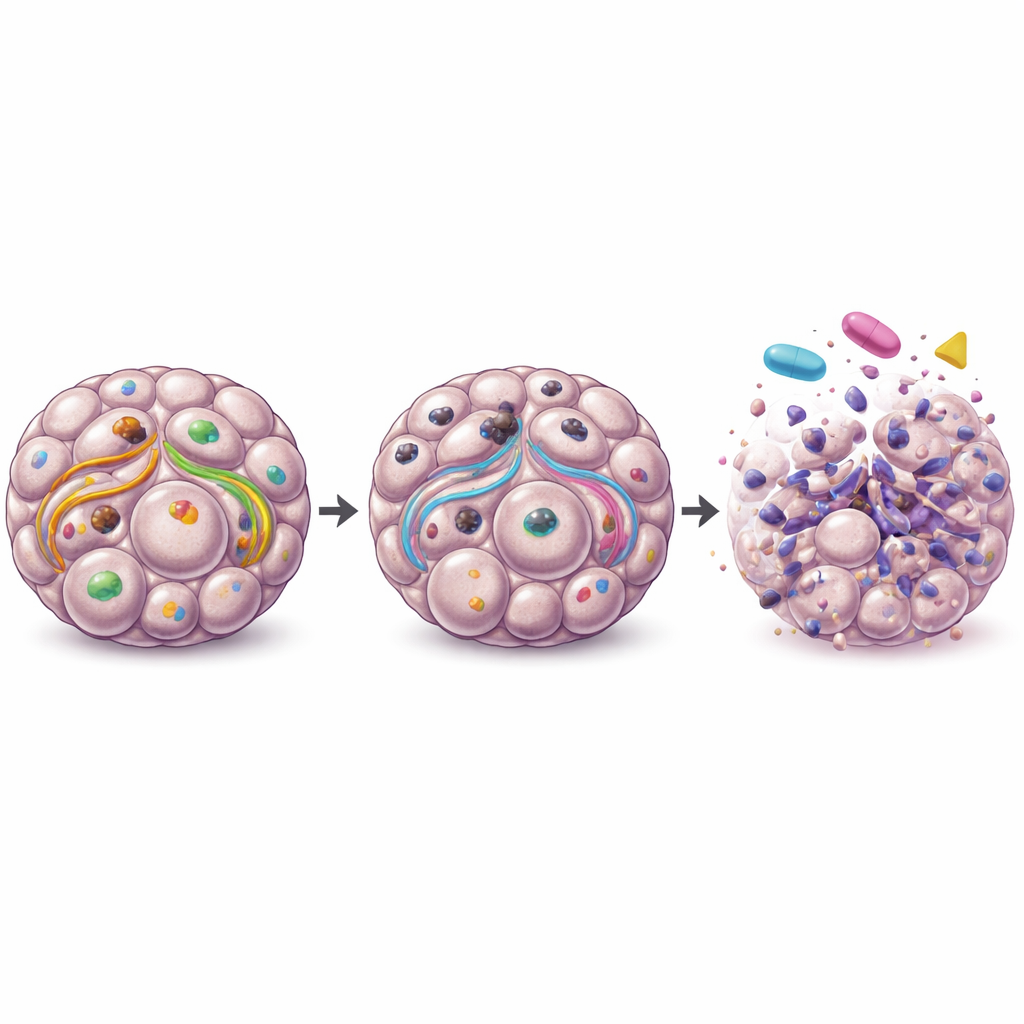
При удалении ULK1 в раковых клетках яичников их способность проводить аутофагию в сфероидах была резко нарушена, о чём свидетельствовали изменения ключевых белков переработки. В таких сфероидах с дефицитом ULK1 оказалось меньше живых клеток и наблюдались повышенные признаки программируемой гибели, что указывает на неспособность кластеров эффективно переносить стрессовые условия. Любопытно, что удаление ULK1 из незлокачественных предшественников не подавляло их систему утилизации в той же степени, что предполагает большую зависимость раковых клеток от ULK1 по сравнению со здоровыми. Эта специфичная для рака зависимость делает ULK1 привлекательной целью для терапии.
Замедление распространения и ослабление опухолевых очагов
Помимо выживания в подвесе, сфероиды должны прикрепиться и прорасти в гладкую оболочку брюшной полости, чтобы образовать новые опухоли. В лабораторных моделях, имитирующих этот ранний этап метастазирования, команда показала, что сфероиды без ULK1 значительно хуже оттесняли и прорастали слой мезотелиальных клеток, который обычно покрывает органы брюшной полости. В органоидах, встроенных в гелеобразную матрицу, раковые клетки без ULK1 формировали также меньшие и менее устойчивые опухолевые структуры. В моделях на мышах, куда человеческие клетки рака яичников вводили в брюшную полость, потеря ULK1 приводила к меньшему числу опухолевых вкраплений и меньшему накоплению жидкости — маркерам продвинутого заболевания, хотя общая выживаемость животных при этом не улучшалась.
Ослабление ключевых сигналов и усиление действия таргетных препаратов
Чтобы понять, как ULK1 поддерживает рак помимо роли в аутофагии, исследователи проанализировали изменения белков в сфероидах без ULK1. Они обнаружили нарушение основных маршрутов роста и выживания в клетке — особенно путей MEK–MAPK и PI3K–AKT–mTOR. Эти пути обычно помогают раковым клеткам противостоять гибели и продолжать деление. Когда командa обработала сфероиды без ULK1 препаратами, блокирующими MEK или mTOR, раковые кластеры стали значительно уязвимее: выживаемость и способность повторно прикрепляться резко снизились. Напротив, удаление ULK1 не повышало чувствительность к стандартным химиопрепаратам, таким как карбоплатин, паклитаксел, или к ингибитору PARP олапарибу, и в некоторых условиях даже, по-видимому, снижало их эффективность.
Подсказки из образцов пациентов и миниатюрных моделей пациента
Анализ больших общедоступных наборов данных по опухолям яичников показал, что более высокая активность гена ULK1 связана с худшей долгосрочной выживаемостью и особенно повышена в метастатических образцах по сравнению с первичными опухолями и нормальной тканью. Чтобы приблизиться к клинике, исследователи протестировали клиническую таблетированную форму ингибитора ULK1 DCC-3116 на органоидах, полученных от метастатических образцов пациентов. В подмножестве этих моделей блокада ULK1 в одиночку или применение препаратов против MEK или mTOR снижали выживаемость органоидов, хотя сочетание агентов не давало стабильного дополнительного эффекта. Другие органоиды пациентов оказались устойчивы ко всем испытанным лечениям, что подчёркивает разнообразие рака яичников и необходимость маркеров для выявления пациентов, которые могут получить пользу.
Что это значит для будущего лечения
В совокупности результаты изображают ULK1 как центрального помощника при распространении рака яичников: он поддерживает внутреннюю переработку, которая сохраняет сфероидные кластеры живыми, способствует их способности внедряться в новые очаги и помогает поддерживать мощные сигнальные маршруты роста. Отключение ULK1 ослабляет эти процессы, уменьшает экспериментальные опухоли и делает кластеры раковых клеток более чувствительными к определённым таргетным препаратам, хотя не к стандартной химиотерапии. Для пациентов это исследование предполагает, что ULK1 может стать частью стратегии медицины точности — особенно для тех с ULK1-высокой метастатической болезнью — где ингибиторы ULK1 комбинируют с блокаторами MEK или mTOR, чтобы ограничить рост и распространение опухоли при условии тщательной диагностики, позволяющей определить, какие опухоли с наибольшей вероятностью отреагируют.
Цитирование: Webb, J.D., Buensuceso, A., Tomas, E.J. et al. ULK1 promotes metastatic progression in experimental models of epithelial ovarian cancer. Oncogene 45, 1111–1127 (2026). https://doi.org/10.1038/s41388-026-03702-2
Ключевые слова: рак яичников, метастазирование, аутофагия, ULK1, таргетная терапия