Clear Sky Science · ru
Ассоциация ретиноидов, рецепторов ретиноевой кислоты и эпигенетики при раке молочной железы
Почему витамин А важен при раке молочной железы
Большинство людей знают витамин А как питательное вещество, важное для зрения, но его активная форма в организме — ретиноевую кислоту — также помогает клеткам решать, расти ли, дифференцироваться или самоуничтожаться при повреждении. В этом обзорном материале рассматривается, как ретиноевая кислота и её клеточные «стации-докеры» изменяются при раке молочной железы, почему многообещающие лабораторные результаты ещё не перешли в успешные препараты для пациентов и как новые данные о «программном обеспечении» раковой клетки — её эпигенетическом коде — могут возродить эту стратегию лечения.
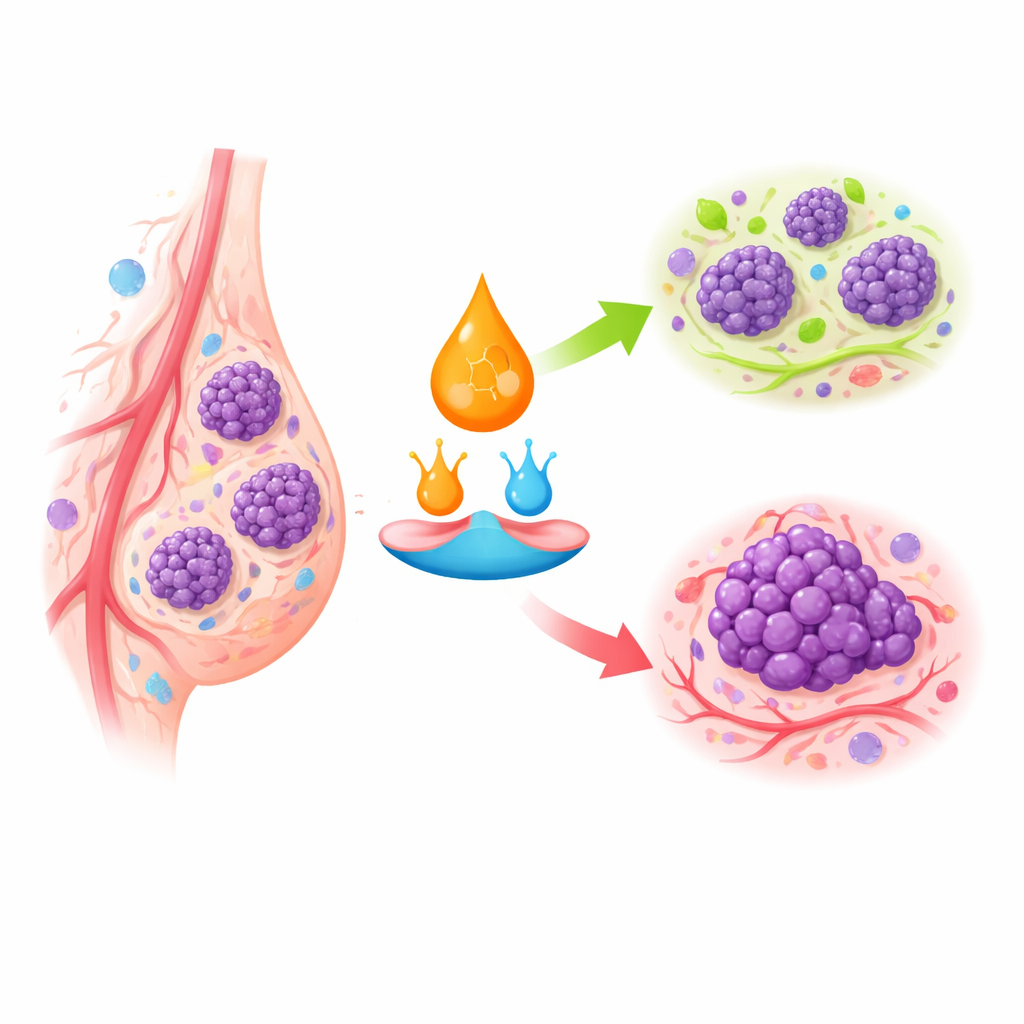
Клеточные светофоры роста и самоуничтожения
Ретиноевая кислота действует, связываясь со специфическими рецепторами внутри клеток, которые затем переключают целые группы генов «включено» или «выключено». В здоровой ткани молочной железы эта система поощряет прекращение деления клеток, их созревание в устойчивые формы или гибель при возникновении аномалий. При раке молочной железы, особенно в более агрессивных подтипах, ключевые рецепторы отсутствуют или заглушены, а внутриклеточный транспорт ретиноевой кислоты перенаправлен. Вместо доставки к рецепторам, замедляющим рост, она может направляться по путям, которые способствуют выживанию и пролиферации. Это помогает объяснить, почему некоторые опухоли молочной железы почти не реагируют на ретиноидные препараты, хотя те же препараты очень эффективны при некоторых злокачественных заболеваниях крови.
Скрытые переключатели в «программном обеспечении» раковой клетки
Авторы сосредотачиваются на эпигенетике — химических «ярлыках» на ДНК и белках-упаковщиках, которые действуют как настройки программного обеспечения генома. Во многих случаях рака молочной железы эти метки запирают важные рецепторы ретиноевой кислоты, особенно один, называемый RARβ2, в положении «выключено», не меняя при этом основной последовательности ДНК. Дополнительные метильные группы на ДНК и уплотнение белковых «шпулей» закрывают этот рецептор, тогда как другие ферменты перестраивают ландшафт хроматина в пользу роста и миграции. Некодирующие РНК, которые не кодируют белки, но влияют на активность генов, дополнительно смещают сигналы в сторону выживания и против дифференцировки. В совокупности эти изменения дают раковым клеткам гибкость для сопротивления лечению и адаптации к стрессу.
Перенастройка сигнальных путей
Важно, что эти эпигенетические замки обратимы. В лабораторных моделях препараты, удаляющие метилирование ДНК или разрыхляющие хроматин, могут восстанавливать RARβ2 и другие компоненты пути ретиноевой кислоты. В сочетании с самой ретиноевой кислотой и стандартной химиотерапией эти «прайминг»-агенты уменьшают опухоли более эффективно и сокращают пул стволоподобных клеток, считающихся источником рецидива. Также имеет значение, как ретиноевую кислоту транспортируют внутри клетки: один белок‑переносчик направляет её к рецепторам, подавляющим рост, тогда как другой доставляет её в про‑ростовые пути. Регулирование баланса между этими носителями может превратить ретиноевую кислоту из «удобрения» в «тормоз».
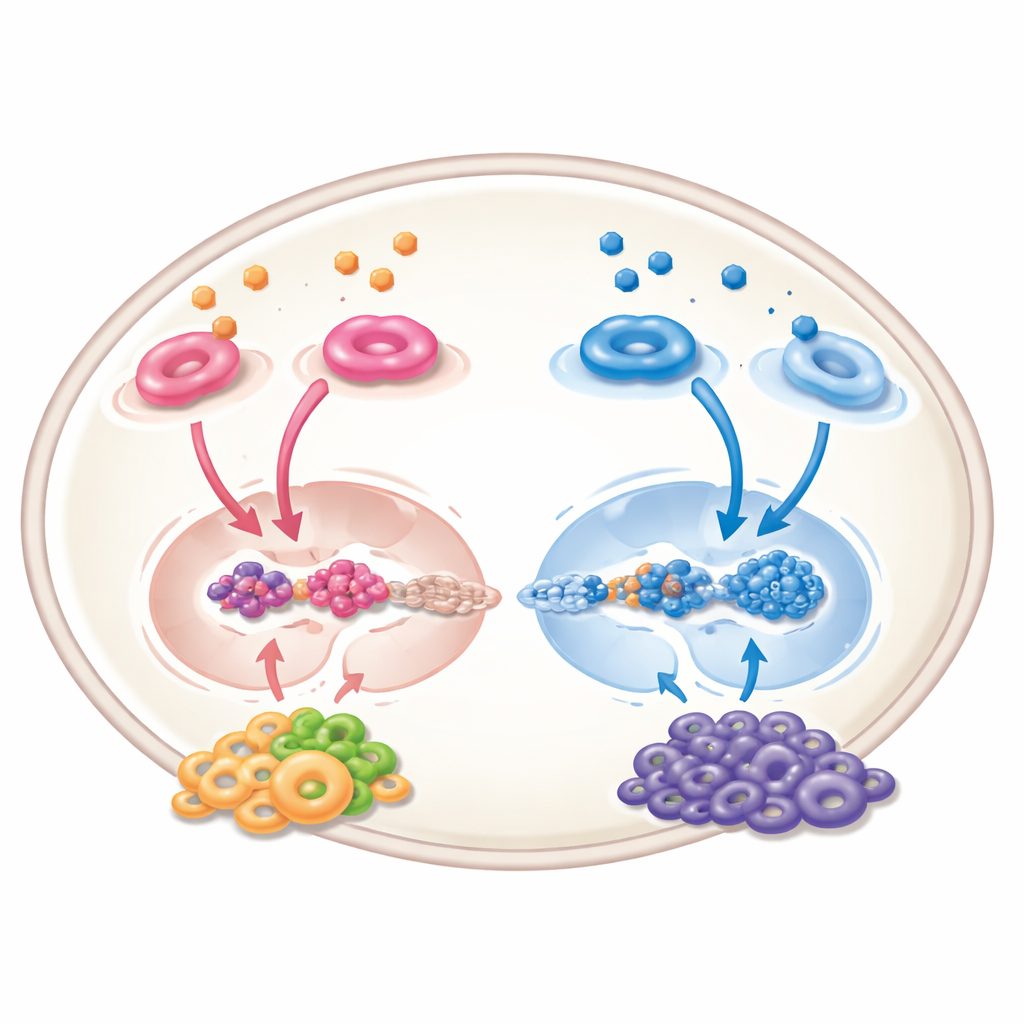
За пределами опухоли: эффект соседства
Ретиноевую кислоту следует рассматривать не только как агент, действующий на раковые клетки; она также перестраивает «окрестности» опухоли — сосуды, иммунные и поддерживающие клетки. В экспериментальных системах она может уменьшать неоваскуляризацию, смещать иммунные клетки в более активное, противоопухолевое состояние и ограничивать супрессивные клетки, которые обычно притупляют защиту организма. Однако картина не полностью однозначна: в некоторых стромальных клетках, окружающих опухоль, активация ретиноевой сигнализации может способствовать росту рака, усиливая химические каналы коммуникации, привлекающие и поддерживающие злокачественные клетки. Эти противоположные эффекты означают, что будущая терапия должна быть тонко настроена, чтобы воздействовать на нужные типы клеток определённым образом.
Проектирование более умных клинических исследований
Ранние клинические испытания ретиноидных препаратов при раке молочной железы в целом не увенчались успехом, но они проводились до появления современного понимания подтипов, биомаркеров и сложной фармакологии. Авторы утверждают, что новые исследования должны отбирать пациентов, чьи опухоли демонстрируют молекулярные признаки чувствительности к ретиноидам — например, сохранённую экспрессию рецепторов или специфические шаблоны метилирования ДНК — и сочетать ретиноиды с препаратами, снимающими эпигенетические блоки, нацеленными на пути роста или усиливающими иммунный ответ. Улучшенные формулы, поддерживающие стабильный уровень препарата в организме, вместе с тщательным контролем как опухоли, так и окружающей ткани будут решающими. Если эти препятствия удастся преодолеть, лечения на основе ретиноевой кислоты могут найти своё место в качестве точных инструментов против избранных форм рака молочной железы.
Цитирование: Szymański, Ł., Schenk, T., Ławiński, M. et al. Association of retinoids, retinoic acid receptors and epigenetics in breast cancer. Oncogene 45, 961–970 (2026). https://doi.org/10.1038/s41388-026-03699-8
Ключевые слова: ретиноевую кислоту, рак молочной железы, эпигенетика, терапия дифференцировки, микроокружение опухоли