Clear Sky Science · ru
Моделирование взаимосвязи жировой ткани и рака: трёхмерная перспектива
Почему жир и рак ближе, чем кажется
Большинство из нас воспринимает жир в организме как лишнюю прокладку или запас энергии, но исследования показывают: это активный, «разговорчивый» орган, который влияет на здоровье порой неожиданными способами. В этом обзоре рассматривается, как жировая ткань и раковые клетки обмениваются сигналами, и как новые трёхмерные (3D) лабораторные модели помогают учёным точнее воспроизводить этот диалог. Понимание этой скрытой коммуникации может улучшить профилактику рака, тестирование лекарств и терапию, особенно в мире с растущей распространённостью лишнего веса. 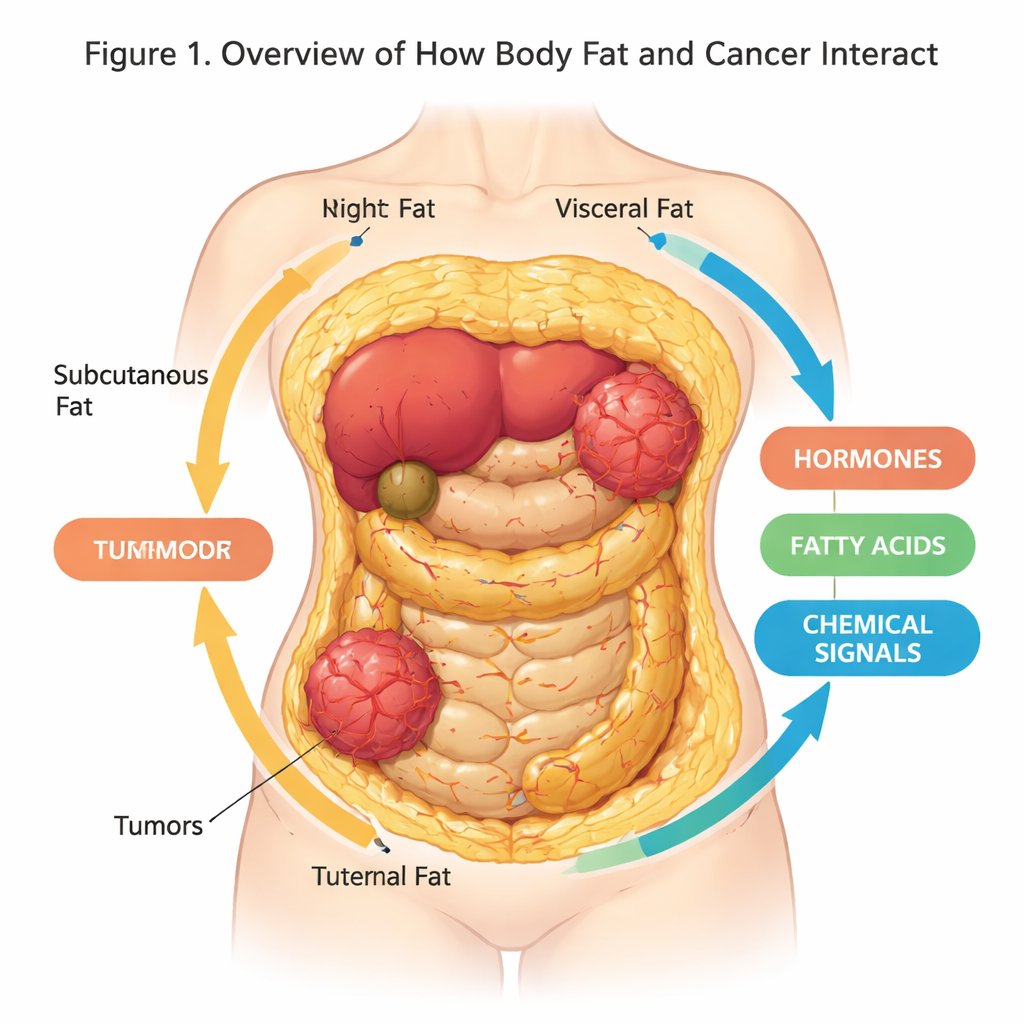
Жир как живой, «говорящий» орган
Жировая ткань — наш корпусной жир — это не просто пассивное хранилище. Это сложный орган, состоящий из адипоцитов, иммунных клеток, кровеносных сосудов и клеток‑поддержки, все они размещены в структурной сети — внеклеточном матриксе. Разные типы жира располагаются в разных местах: подкожный жир под кожей, висцеральный жир вокруг внутренних органов, а также белые, бурые и «бежевые» адипоциты, отличающиеся по способу хранения или сжигания энергии. Эти клетки постоянно выделяют смесь гормонов, жирных кислот и сигнальных белков, влияющих на обмен веществ, воспаление и, как теперь известно, на риск развития и поведение рака.
Ожирение, воспаление и риск рака
Когда мы набираем слишком много веса, белые жировые клетки увеличиваются в размере и количестве, а ткань испытывает стресс и воспаление. Такой «нездоровый» жир выделяет больше провоспалительных молекул и жирных кислот в кровоток при одновременном ухудшении обработки сахара и жиров. Крупные эпидемиологические исследования связывают ожирение с повышенным риском и худшими исходами при многих видах рака, включая рак молочной железы, толстой кишки, поджелудочной железы и матки. В обзоре объясняется, как дисфункциональная жировая ткань может подпитывать опухоли дополнительным топливом, уплотнять окружающие ткани и привлекать другие типы клеток, создавая более благоприятную для рака среду.
Двусторонний диалог между жиром и опухолями
Рак рассматривают теперь как заболевание целой экосистемы, а не только как проблему отдельных «беглых» клеток. Опухолевые клетки используют соседний жир в качестве ресурса, перепрограммируя адипоциты, иммунные клетки и фибробласты, чтобы те помогали росту и распространению. В ответ жировые клетки расщепляют запасённые липиды и выделяют жирные кислоты и гормоны, которые опухолевые клетки легко используют. Такая коммуникация может происходить на расстоянии через циркулирующие сигналы или локально, где опухоль растёт рядом с жиром, как в молочной железе или брюшной полости. Опухолевые клетки могут даже заставлять жировые клетки терять свою исходную идентичность, превращая их в более схожие с клетками, формирующими рубец, или иммуноподобными клетками, которые перестраивают ткань и способствуют инвазии. 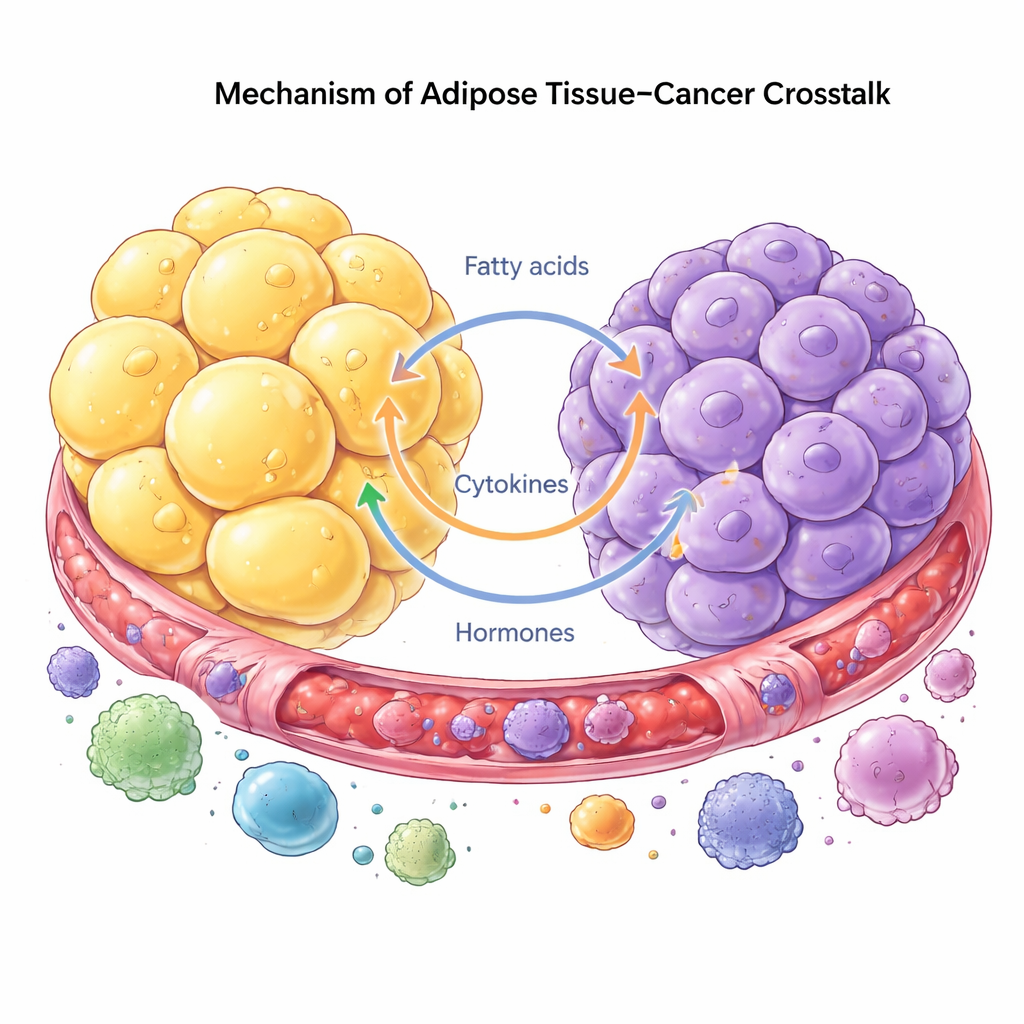
Создание мини-тканей в 3D
Традиционные плоские (2D) культуры клеток и животные модели часто не отражают этих сложных взаимодействий. Авторы описывают новое поколение 3D‑систем, которые ближе к реальной ткани. Сфероиды — это простые кластеры клеток, самоорганизующиеся в крошечные сферы; каркасы (scaffolds) — сконструированные материалы, обеспечивающие трёхмерную опору для роста клеток; органоиды — миниатюрные, самоорганизующиеся версии тканей; а ассемблоиды комбинируют несколько органоидов или сфероидов в составные «мини‑органы». Исследователи используют эти 3D‑подходы для совместного культивирования жировых и раковых клеток, изучения того, как состояния, напоминающие ожирение, меняют их поведение, и проверки, как лекарства могут нарушать вредоносный диалог между ними.
Перспективы и существующие пробелы
Каждая модель имеет свои компромиссы. Сфероиды недороги и подходят для высокопроизводительного скрининга, но относительно просты. Каркасы позволяют точно контролировать физические свойства, такие как жёсткость, что может влиять на распространение рака, но требуют большей технической подготовки. Органоиды и ассемблоиды дают наибольшую реалистичность благодаря множеству взаимодействующих типов клеток, однако они дороги, сложно стандартизируемы и часто лишены полноценных сетей сосудов или иммунных компонентов. В обзоре подчёркивается, что современные системы всё ещё далеки от идеала в точном воспроизведении человеческой жировой и опухолевой ткани, особенно в части полной реконструкции внеклеточного матрикса, зрелых адипоцитов и участия иммунных клеток.
Куда движется это направление исследований
Авторы заключают, что улучшение 3D‑моделей взаимодействия жира и рака необходимо для более точного тестирования лекарств и понимания того, как ожирение способствует развитию рака. По мере того как эти «мини‑ткани» становятся более правдоподобными — сочетая реалистичный жир, опухолевые клетки, кровеносные сосуды и иммунные клетки — они могут помочь учёным прогнозировать, какие терапии сработают у конкретных пациентов, разрабатывать стратегии, блокирующие использование опухолью жировых запасов как топлива, и в конечном счёте направлять лечение, нацеленное не только на опухоли, но и на «нездоровые» микроокружения, способствующие их росту.
Цитирование: Strusi, G., Suelzu, C.M. & Stebbing, J. Modelling adipose tissue-cancer crosstalk: a three-dimensional perspective. Oncogene 45, 905–913 (2026). https://doi.org/10.1038/s41388-026-03697-w
Ключевые слова: жировая ткань, ожирение, микроокружение опухоли, 3D-клеточная культура, метаболизм опухоли