Clear Sky Science · ru
O-гликозилирование POM121 облегчает костные метастазы немелкоклеточного рака лёгкого через усиленный ядерный импорт c‑MYC и перенастройку ВЭМ
Почему это исследование важно
Когда рак лёгкого распространяется в кости, это вызывает сильную боль, переломы и значительно сокращает выживаемость, но врачам по‑прежнему недоступно много способов остановить этот смертельный этап. В этом исследовании авторы изучают внутреннюю «кухню» раковых клеток лёгкого, чтобы понять, как некоторые из них получают преимущество, позволяющее им мигрировать из лёгкого в кость и там процветать. Проследив этот процесс до крошечных изменений на одном белке‑шлюзе в оболочке ядра, исследователи выявляют новую цепочку событий, нацеленную терапевтическими и прогностическими подходами для предотвращения или лечения костных метастазов при немелкоклеточном раке лёгкого.
Сахарная метка, меняющая поведение рака
Исследователи сосредоточились на посттрансляционных модификациях — небольших химических изменениях, которые белки приобретают после синтеза. Одна из таких модификаций, O‑GlcNAcylation, — это присоединение небольшого сахара к определённым участкам белков. На линиях клеток рака лёгкого и в моделях на мышах команда сравнила обычные опухолевые клетки с подпопуляциями, многократно отбираемыми по способности колонизировать кость. Они обнаружили, что у этих «костеориентированных» клеток общий уровень O‑GlcNAcylation был значительно выше, что объяснялось повышенной активностью фермента OGT, устанавливающего эту сахарную метку. Среди сотен модифицированных белков выделялся один: POM121, ключевой компонент ядерной поры — структуры, контролирующей обмен между ядром и цитоплазмой.
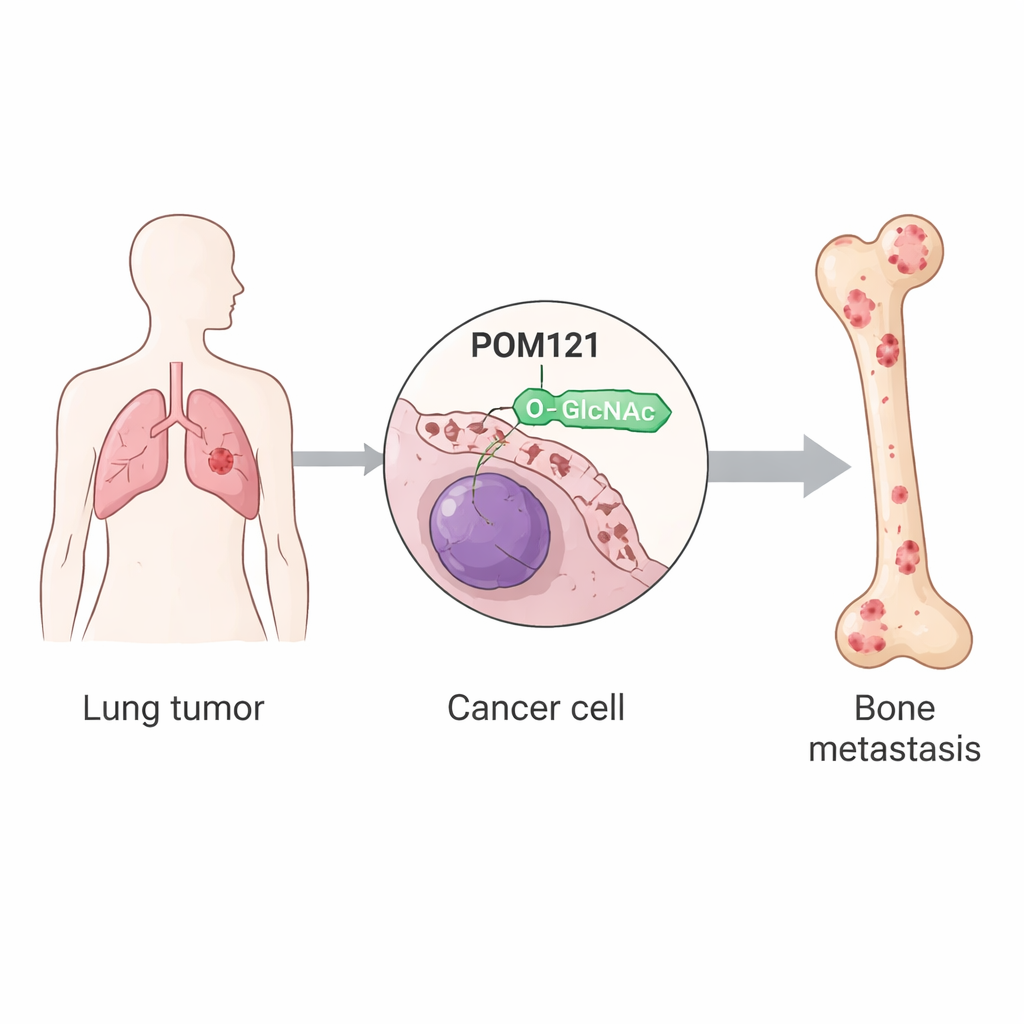
Ядерный «шлюз» POM121 стабилизируется
POM121 размещён в мембране, окружaющей ядро, и входит в состав канала, через который проходит множество сигнальных белков. В клетках рака лёгкого с метастазами в кости POM121 содержал большое количество O‑GlcNAc на одной аминокислоте — серине 199. При замене этой позиции на немодифицируемую белок становился нестабильным и быстро разрушался клеточным «мусороперерабатывающим» механизмом. Работа показывает, что сахарная метка защищает POM121 от пометки на уничтожение ферментом TRIM21, который обычно присоединяет убикуитиновые «метки на утилизацию». В присутствии O‑GlcNAc TRIM21 плохо связывается с белком, уровень убиквитинирования падает, и POM121 накапливается в ядерной поре без сдвига локализации.
Открывая путь для мощного онкогена
Какое значение имеет более стабильный POM121? Ключ к ответу — известный провоспалительный и онкоподдерживающий белок, транскрипционный фактор c‑MYC. c‑MYC должен проникнуть в ядро, чтобы включать гены, но его транспорт зависит от компонентов ядерной поры, таких как POM121. Авторы показали, что при избытке O‑GlcNAc‑модифицированного POM121 в ядре обнаруживалось больше c‑MYC; при снижении уровня POM121 или удалении его сахарной метки импорт c‑MYC в ядро резко падал. У мышей клетки рака лёгкого с немодифицируемым мутантом POM121 давали значительно меньше и меньшие по размеру костные метастазы, тогда как восстановление c‑MYC в клетках с дефицитом POM121 частично возвращало их способность колонизировать кость. Это помещает POM121 выше c‑MYC в критическом метастатическом пути.
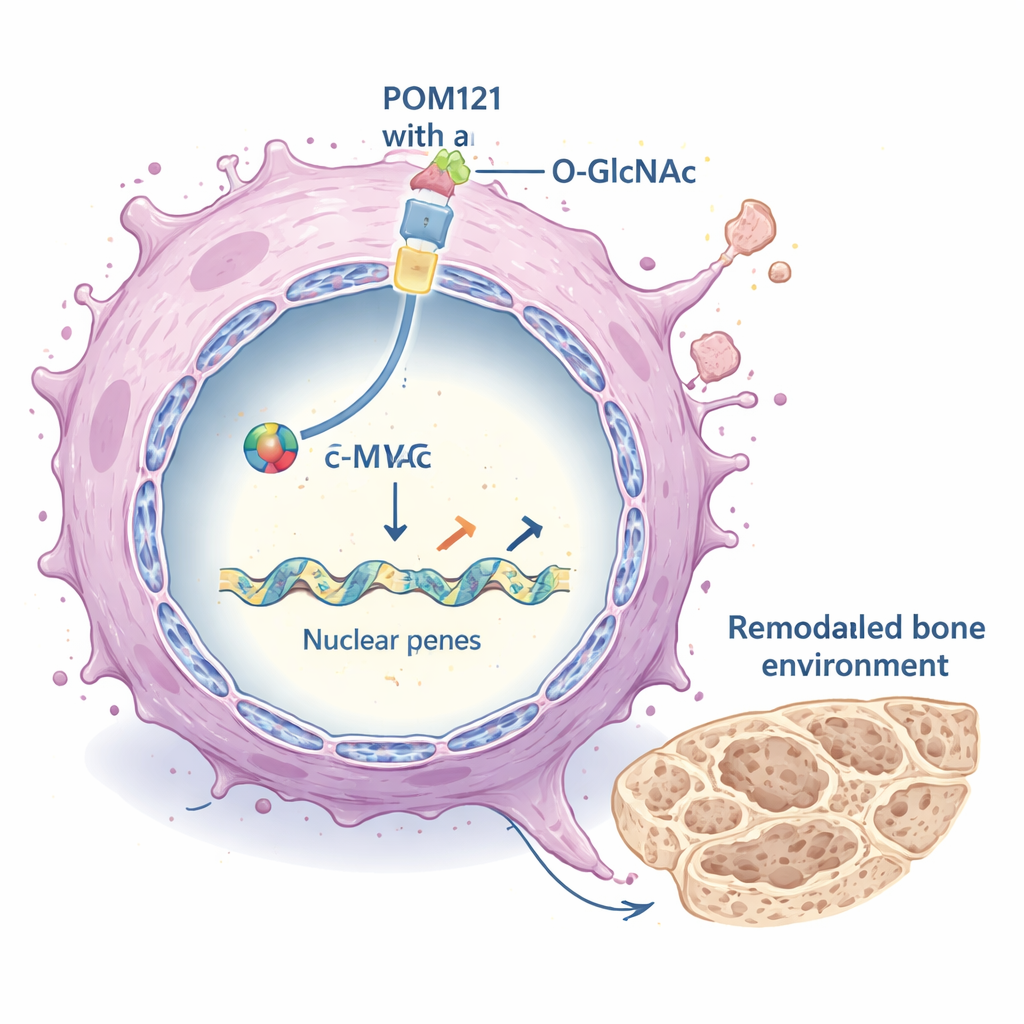
Перенастройка микроокружения опухоли
Оказавшись в ядре, c‑MYC действует как главный переключатель многих генов. Здесь показано, что он сильно активирует набор генов, формирующих внеклеточный матрикс (ВЭМ) — каркас белков вокруг клеток. Эти гены ВЭМ, включающие различные коллагены и ферменты, перестраивающие тканевую архитектуру, были подавлены при блокировании POM121 или c‑MYC и активировались при высоких уровнях O‑GlcNAcylation и POM121. Изменённый ВЭМ, в свою очередь, усиливал основные пути роста внутри раковых клеток, в частности сигнальную каскаду PI3K–AKT–mTOR, поддерживающую выживание, рост и распространение. Схожие изменения наблюдались в нескольких моделях рака лёгкого, что указывает на то, что механизм не ограничен одной клеточной линией.
От лабораторного открытия к клиническому значению
Анализ данных пациентов показал, что высокие уровни OGT, POM121 и c‑MYC, а также регулируемых ими генов ВЭМ коррелировали с худшим прогнозом и с опухолями лёгкого, уже давшими метастазы в кости. В совокупности работа описывает ось OGT–POM121–c‑MYC–ВЭМ: повышенное O‑GlcNAcylation стабилизирует ядерный «шлюз» POM121, который пропускает в ядро больше c‑MYC, что затем перенастраивает тканевой матрикс и сигналы роста в пользу костных метастазов. Для пациентов это предлагает новые типы биомаркеров для выявления риска костного распространения и новые терапевтические подходы — от блокирования OGT или функции POM121 до подавления c‑MYC или ремоделирования ВЭМ — которые в будущем могут помешать раку лёгкого достигнуть скелета.
Цитирование: Ren, YZ., Zhao, MN., Du, FL. et al. POM121 O-GlcNAcylation facilitates bone metastasis in non-small cell lung cancer through enhanced c-MYC nuclear import and ECM reprogramming. Oncogene 45, 728–743 (2026). https://doi.org/10.1038/s41388-026-03687-y
Ключевые слова: метастазы рака лёгкого в кости, POM121, O-GlcNAcylation, c‑MYC, внеклеточный матрикс