Clear Sky Science · ru
Сортиллин проявляет активность, похожую на супрессор опухолей, ограничивая транслокационную функцию EGFR
Почему это важно для лечения рака
Рак легкого — ведущая причина смерти от онкологических заболеваний в мире, и многие современные препараты нацелены на молекулу EGFR, которая стимулирует рост опухоли. Эти лекарства часто хорошо действуют сначала, но опухоли нередко становятся устойчивыми. В этом исследовании обнаружен природный «тормоз» внутри клеток рака легкого — неожиданная роль белка сортиллина, который способен ослаблять раково‑промотирующие сигналы EGFR. Понимание этой связи может помочь объяснить, почему некоторые пациенты лучше отвечают на терапии, нацеленные на EGFR, и подсказать новые подходы, позволяющие продлить эффективность таких лечения.
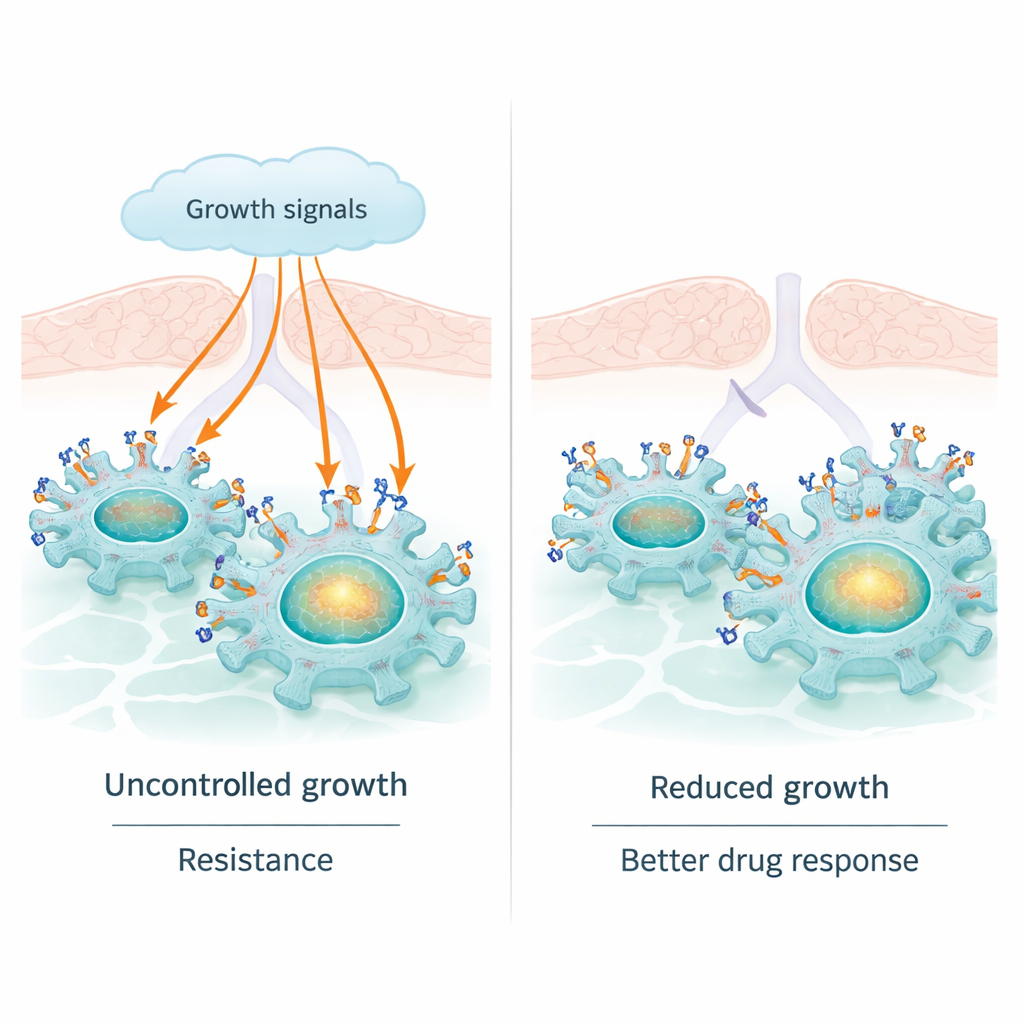
Переключатель роста, работающий на пределе
EGFR — это рецептор на поверхности многих клеток, который улавливает сигналы роста из окружения. У значительной доли аденокарцином легкого EGFR изменён так, что находится в постоянном включённом состоянии. Это подпитывает непрерывный рост и деление клеток и объясняет, почему таблетки‑ингибиторы тирозинкиназ, блокирующие EGFR, могут уменьшать опухоли. Но у EGFR есть и менее замеченная роль: он может перемещаться в ядро клетки и напрямую влиять на ДНК, включая активацию генов, таких как cMYC и CCND1, которые ещё сильнее стимулируют рост, выживание и устойчивость к лечению. Эта ядерная функция EGFR может помогать опухолям ускользать даже когда его поверхностная активность химически подавлена.
Сортиллин входит в ядро
Ранее сортиллин в основном рассматривали как белок сортировки, помогающий интернализовать EGFR с поверхности клетки и направлять его на деградацию, тем самым ослабляя сигналы роста. В этой работе авторы показывают, что сортиллин также следует за EGFR в ядро, когда клетки рака легкого стимулируются. С помощью высокоразрешающей микроскопии и биохимической фракционизации они наблюдали комплексы EGFR и сортиллина, образующиеся внутри ядер вскоре после активации. Важно, что когда EGFR не мог проникнуть в ядро, сортиллин также оставался вне его, что указывает на то, что EGFR служит «пропуском» сортиллина в эту компартмент. Оказавшись в ядре, комплексы EGFR–сортиллин обнаруживались связанными с участками ДНК рядом с сайтами начала транскрипции ключевых генов, контролирующих рост, включая cMYC и CCND1.
Встроенный тормоз для онкогенов
Чтобы понять функцию этих комплексов, исследователи картировали их связывание по всему геному и измеряли изменения в активности генов. Они обнаружили, что сам EGFR склонен продвигать активацию генов, связанных с ростом, тогда как присутствие сортиллина в тех же областях ДНК ослабляет этот эффект. При искусственном снижении уровня сортиллина связывание EGFR в целевых генах увеличивалось, и онкогены, такие как cMYC и CCND1, становились более активными. Напротив, повышение уровня сортиллина давало обратный эффект: связь EGFR с ДНК ослабевала, рекрутирование транскрипционного аппарата снижалось, и экспрессия этих онкогенных генов падала. В модельных мышах опухоли легкого, генетически модифицированные для избыточного синтеза сортиллина, росли медленнее и демонстрировали пониженные уровни cMYC и CCND1.
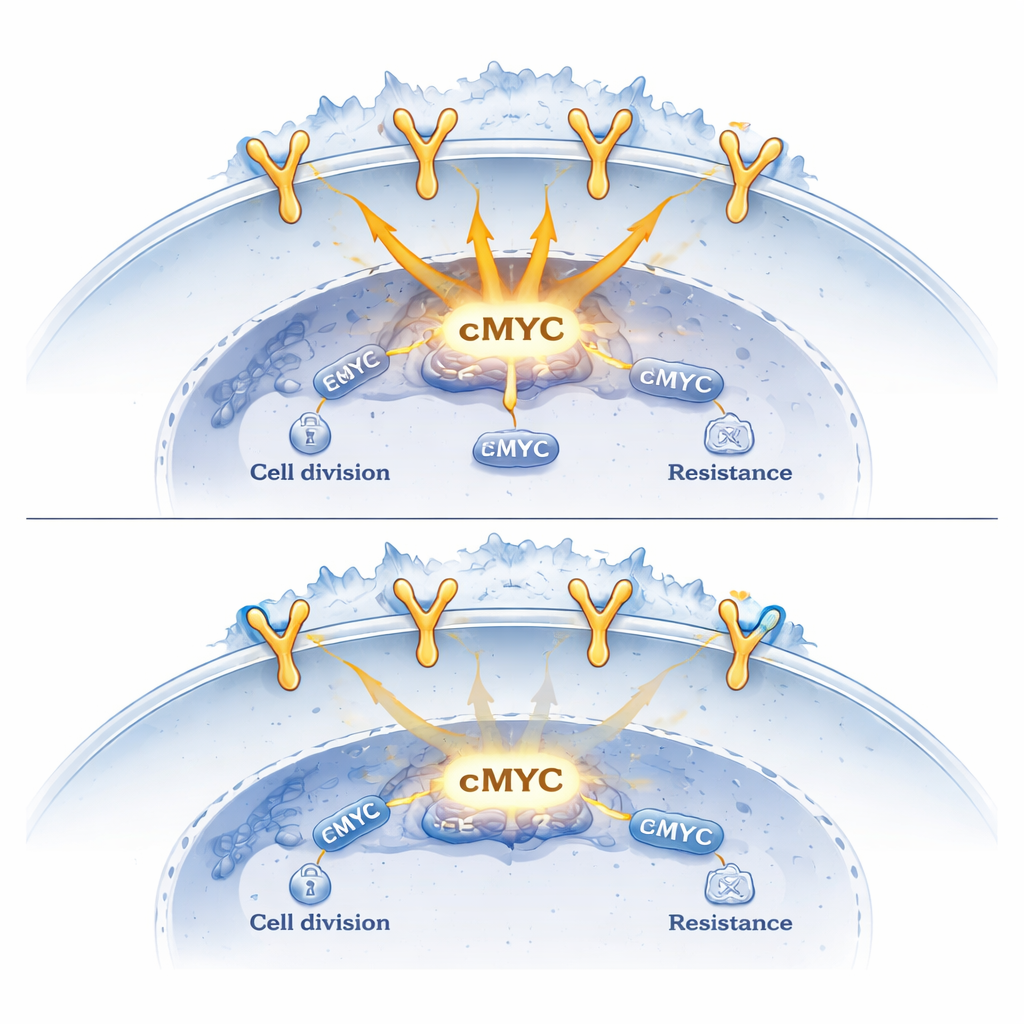
Взаимодействие с препаратами против EGFR
Исследование также рассмотрело, как этот механизм пересекается с действием осимертениба, широко используемого препарата, нацеленного на EGFR и разработанного для блокирования проблемных мутаций EGFR. Удивительно, но даже когда осимертениб подавлял ферментативную активность EGFR, рецептор продолжал перемещаться в ядро. Там он продолжал связываться с ДНК, особенно вблизи гена cMYC. При этом сортиллин также накапливался в ядре в этих условиях. Когда сортиллина было много, уровни cMYC более сильно снижались в ответ на осимертениб, а жизнеспособность раковых клеток падала. Анализ опухолей пациентов и больших публичных онкологических баз данных показал, что уровень сортиллина часто ниже в аденокарциноме легкого по сравнению с нормальной тканью легкого, и что более высокая экспрессия сортиллина стабильно связана с более низкой экспрессией cMYC.
Что это значит для пациентов
В сумме результаты рисуют образ сортиллина как своего рода партнёра с функцией, похожей на супрессор опухолей, который следует за EGFR в ядро и затем его сдерживает. Ограничивая способность EGFR включать мощные гены роста, такие как cMYC, сортиллин может замедлять прогрессирование опухоли и усиливать эффект препаратов, блокирующих EGFR. Поскольку во многих опухолях легкого уровень сортиллина снижен, им может не хватать этого внутреннего тормоза, что частично объясняет, почему некоторые раки особенно агрессивны или быстро приобретают лекарственную устойчивость. Измерение уровня сортиллина в опухоли могло бы помочь предсказать ответ пациента на терапии, нацеленные на EGFR, а стратегии, повышающие активность сортиллина, могут предложить новый способ более длительного контроля над EGFR‑опосредованными раками.
Цитирование: Lapeyronnie, E., Granet, C., Tricard, J. et al. Sortilin exhibits tumor suppressor-like activity by limiting EGFR transduction function. Oncogene 45, 875–888 (2026). https://doi.org/10.1038/s41388-026-03680-5
Ключевые слова: рак легкого, EGFR, сортиллин, cMYC, резистентность к таргетной терапии