Clear Sky Science · ru
Синаптические эффекты интерлейкина-6 на дофаминергические нейроны человека, полученные из iPSC
Почему воспаление важно для настроения
У многих людей с депрессией в крови выявляются признаки низкоуровневого воспаления, и эти иммунные изменения тесно связаны с симптомами, такими как потеря удовольствия, усталость и замедленность движений. В этом исследовании ставится конкретный вопрос: как один ключевой воспалительный сигнал — молекула интерлейкин‑6 — непосредственно влияет на человеческие клетки мозга, использующие дофамин, нейромедиатор, который поддерживает мотивацию и систему вознаграждения? Выращивая в лаборатории человеческие дофамин-продуцирующие нейроны из стволовых клеток, исследователи могли наблюдать, как эти клетки реагируют на воспаление и отличается ли эта реакция у клеток, полученных от женщин и мужчин.
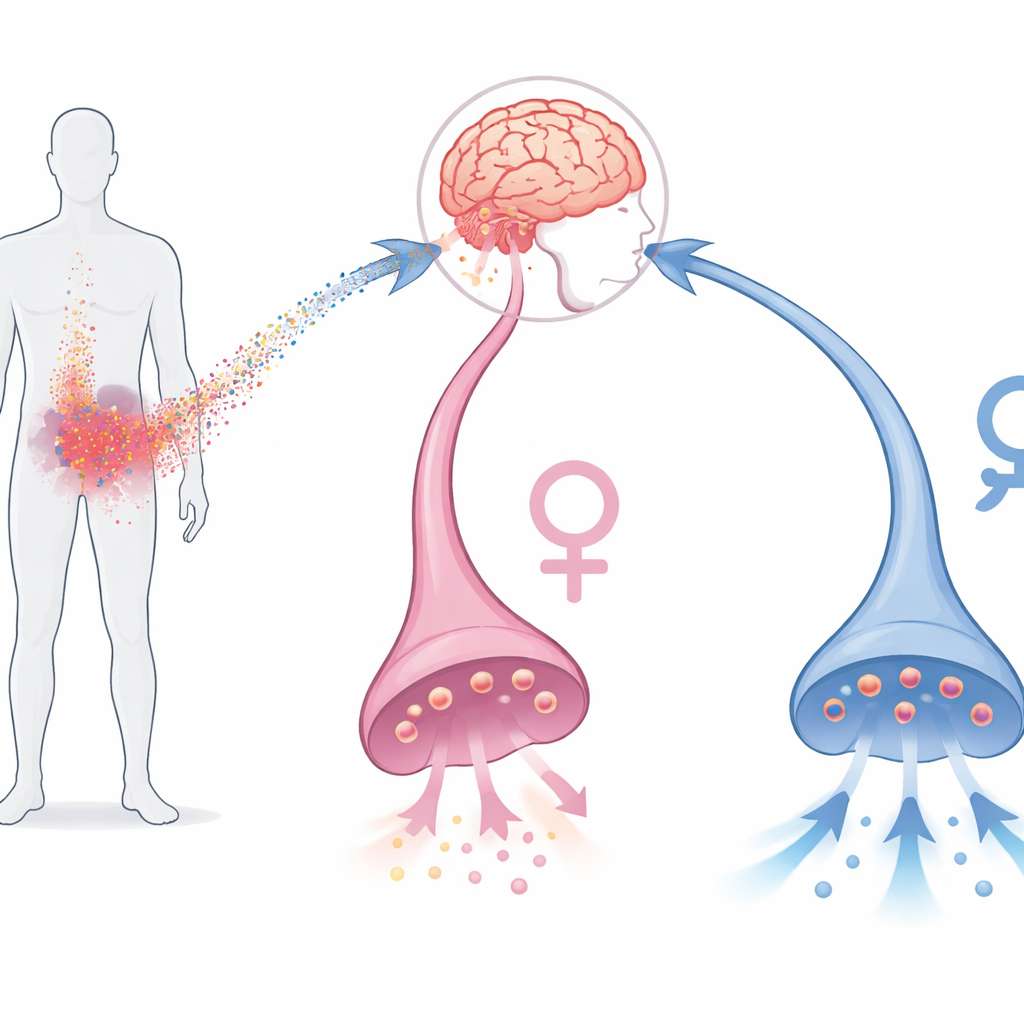
От сигналов крови к мозговой мотивации
Депрессия распространена, вызывает значительную утрату трудоспособности и часто плохо поддаётся стандартным антидепрессантам, особенно у людей с повышенными маркерами воспаления в крови. Предыдущие исследования на людях и животных показали, что воспалительные триггеры могут ослаблять активность системы вознаграждения мозга, в частности вентрального стриатума, который сильно зависит от дофамина. При экспериментальном увеличении уровня воспалительных молекул у людей и животных обычно снижается мотивация добиваться вознаграждения. Интерлейкин‑6 — одна из таких молекул, и при стрессе он может достигать дофаминовых нейронов в мозге. Тем не менее точные механизмы его воздействия на клетки, выделяющие дофамин, оставались неясными, особенно в отношении человеческих нейронов и потенциальных половых различий.
Построение человеческих дофаминовых нейронов в чашке Петри
Чтобы изучить эти механизмы, команда перепрограммировала клетки кожи или крови здоровых мужчин и женщин в индуцированные плюрипотентные стволовые клетки, а затем направила их дифференцировку в дофаминовые нейроны среднего мозга — тот тип, который участвует в мотивации. Примерно через восемь недель созревания эти нейроны проявляли ожидаемые маркёры и электрическую активность. Затем учёные подвергли клетки воздействию интерлейкин‑6 в течение 24 часов и измерили три ключевых показателя: сколько дофамина они выделяли, как часто они генерировали электрические импульсы и насколько эффективно маленькие дофаминовые пузырьки — синаптические везикулы — перемещались и докировались у окончания аксона для высвобождения содержимого.
Разные ответы у клеток от женщин и мужчин
Результаты выявили заметный раскол между нейронами, полученными от женщин, и нейронами, полученными от мужчин. В клетках от женщин интерлейкин‑6 отчётливо ослаблял дофаминергическую систему: выделение дофамина уменьшалось, частота электрической активности снижалась, а синаптические везикулы двигались медленнее и реже оказывались «припаркованными» у терминалей, готовыми к выделению. В клетках от мужчин те же воспалительные сигналы вызывали лишь незначительное замедление, но активировали, по-видимому, компенсаторные механизмы. Везикулы двигались быстрее и стали более многочисленными в терминалях, а число пресинаптических контактов увеличилось — изменения, которые могут помочь сохранить выделение дофамина несмотря на воспаление. Анализ экспрессии генов подтвердил эти функциональные различия, указав, что интерлейкин‑6 включал более выраженные воспалительные программы в нейронах от женщин, чем в нейронах от мужчин.
Длинная некодирующая РНК как скрытый переключатель
Углубившись в механизмы, исследователи сосредоточились на регуляторной молекуле MIAT, длинной некодирующей РНК, которая не кодирует белок, но может тонко регулировать активность генов. Мужские дофаминовые нейроны изначально имели более высокий уровень MIAT, чем женские, а интерлейкин‑6 изменял уровень MIAT в противоположных направлениях у двух полов. Когда команда использовала редактирование генома для удаления MIAT в мужских нейронах, клетки теряли свою защитную, компенсаторную реакцию. После воздействия интерлейкин‑6 дефицитные по MIAT мужские нейроны демонстрировали снижение выделения дофамина, замедление электрической активности и уменьшение числа докированных везикул — очень похоже на картину в женских нейронах. MIAT также влияла на гены, контролирующие рециркуляцию дофамина и чувствительность клеток к интерлейкин‑6, что позволяет предположить, что она действует как молекулярный узел, формирующий реакцию дофаминовых нейронов на воспалительный стресс.
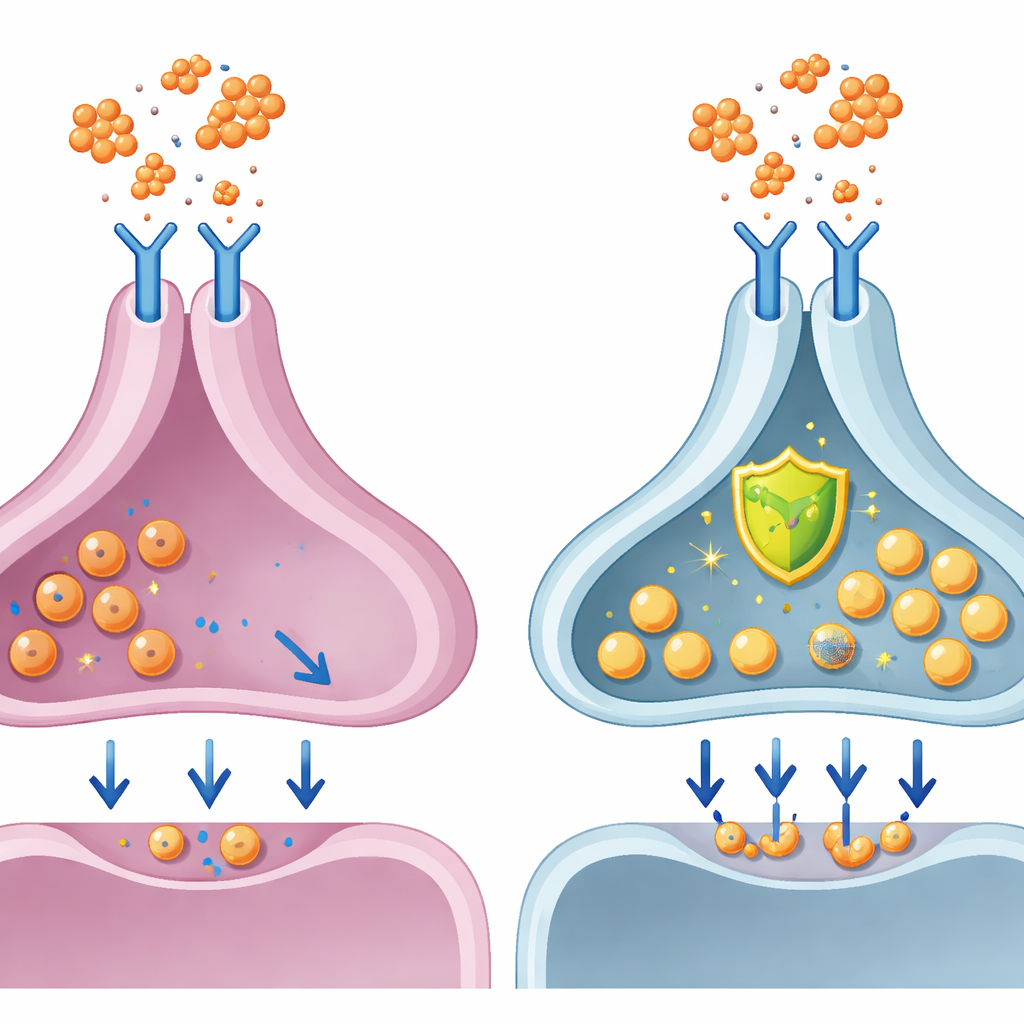
Блокирование вредного пути
Поскольку интерлейкин‑6 сигнализирует через известную цепь белков JAK‑STAT, учёные протестировали, может ли уже существующий препарат, блокирующий этот путь, защитить дофаминовые нейроны. Они добавили барацитиниб, ингибитор JAK, одобренный для лечения воспалительных заболеваний, совместно с интерлейкин‑6. В нейронах, полученных от женщин, барацитиниб в значительной степени обратил снижение выделения дофамина, замедление электрической активности и проблемы с синаптическими везикулами. Это указывает на то, что таргетирование этого пути может напрямую защищать человеческие дофаминовые клетки от дисфункции, вызванной воспалением, по крайней мере в культуре, и может частично объяснять, почему такие препараты у некоторых пациентов ассоциировались с улучшением настроения и мотивации.
Что это значит для людей с депрессией
В совокупности эти результаты показывают, что воспалительные сигналы способны ослаблять человеческие дофаминовые нейроны в половозависимом ключе: у женских нейронов чаще наблюдаются прямые повреждения механизмов выделения дофамина, тогда как мужские нейроны склонны к адаптивным изменениям, помогающим поддерживать функцию. Длинная некодирующая РНК MIAT, по-видимому, является важной частью этого различия, а блокирование сигнальной цепи с помощью барацитиниба может вернуть уязвимые клетки к норме. Для пациентов эти данные поддерживают идею, что терапии, нацеленные на воспаление, могут быть особенно полезны при депрессии с повышенными маркерами воспаления, и что пол и индивидуальные молекулярные профили могут иметь значение при выборе таких подходов лечения.
Цитирование: Huang, Y., Michalski, C., Zhou, Y. et al. Synaptic effects of interleukin-6 on human iPSC-derived dopaminergic neurons. Neuropsychopharmacol. 51, 934–945 (2026). https://doi.org/10.1038/s41386-025-02320-y
Ключевые слова: воспаление и депрессия, дофаминовые нейроны, половые различия, интерлейкин-6, противовоспалительное лечение