Clear Sky Science · ru
RO4938581, негативный аллостерический модулятор GABAA-α5 восстановил поведенческие и ЭЭГ-фенотипы модели мышей синдрома Dup15q
Почему это исследование мозга важно
Синдром Dup15q — редкое генетическое состояние, которое часто вызывает аутизм, приступы и серьёзные трудности в обучении. Для семей доступна главным образом поддерживающая терапия; нет лечения, направленного на коренную биологическую причину. В этом исследовании использовали мышей с тем же дополнительным фрагментом ДНК, что и у людей с Dup15q, чтобы выяснить, что в мозге идёт не так, — и проверить, может ли высокоцелевой экспериментальный препарат ослабить эту проблему. Работа выделяет конкретный тип мозгового рецептора как перспективную и проверяемую мишень для будущих препаратов прецизионной медицины.
Чрезмерное «торможение» в мозге
Наш мозг опирается на тонкий баланс между сигналами «вперёд», которые возбуждают нейроны, и сигналами «стоп», которые их подавляют. При синдроме Dup15q участок 15-й хромосомы дублируется. В этом участке находятся три гена, кодирующие компоненты ключевого «тормозного» рецептора в мозге — GABAA-рецептора, особенно его варианта, содержащего субъединицу альфа-5. Исследователи создали мышей с такой же дупликацией и обнаружили, что у этих животных примерно на 50% больше рецепторов с альфа-5 в областях мозга, важных для памяти, эмоций и движения, включая гиппокамп и кору. Разные методы — от изучения экспрессии генов до визуализации рецепторов — пришли к одному выводу: эта конкретная тормозная система в модели Dup15q чрезмерно развита.
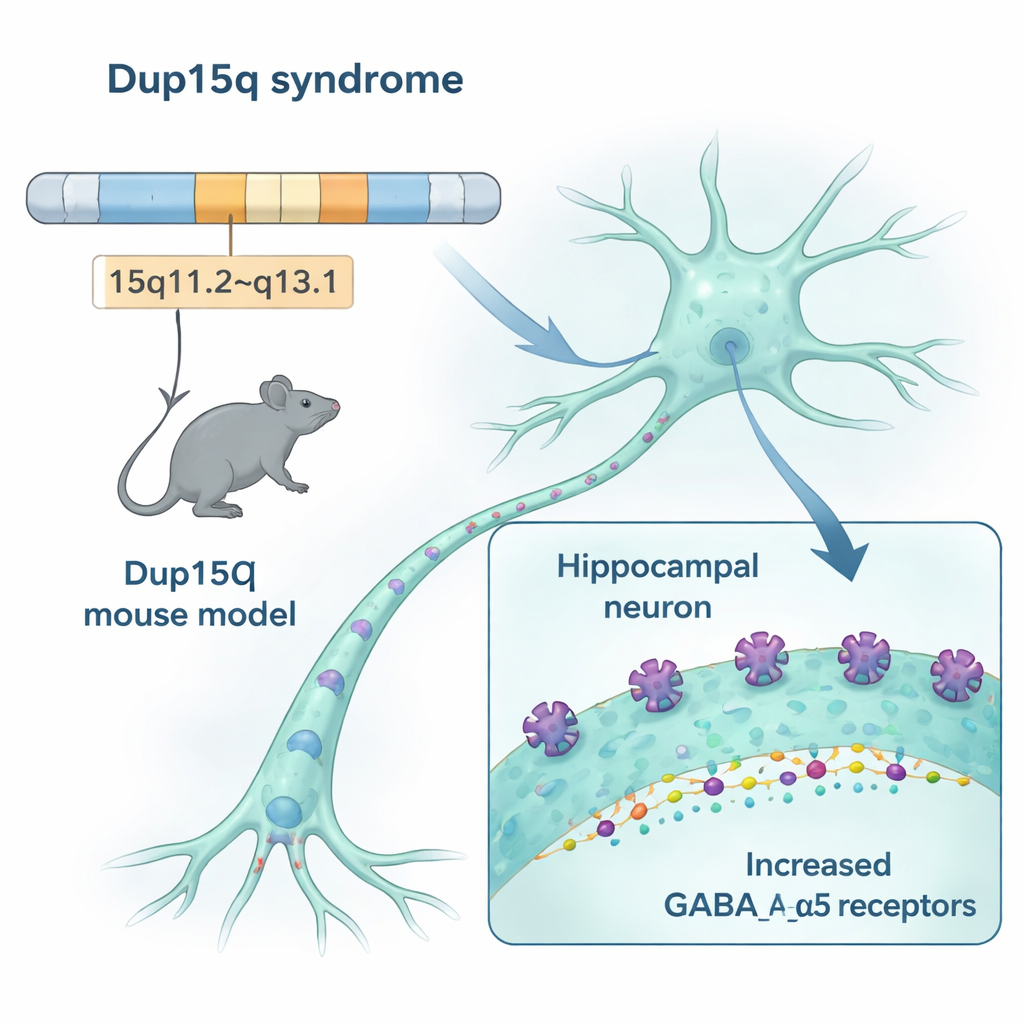
Как избыток рецепторов меняет сигналы мозга
Наличие большего числа тормозных рецепторов имеет значение только если это действительно меняет работу цепей. В тонких срезах гиппокампа команда измеряла крошечные электрические токи, которые тормозные нейроны передают другим клеткам. У мышей с Dup15q эти тормозные токи возникали чаще, что указывает на более сильное фоноподобное торможение, хотя амплитуда каждого отдельного сигнала не изменилась. Отдельный тест поведения цепей — парно‑импульсное ингибирование — также показал, что сети у этих мышей сильнее заглушены, чем у их здоровых сибсов. В сумме данные указывают, что избыток рецепторов делает тормозные цепи доминирующими, смещая баланс в сторону менее гибкой обработки информации.
Поведение и мозговые ритмы у поражённых мышей
Учёные затем спросили, перешло ли это изменённое «проводение» в поведенческие проявления, напоминающие симптомы у людей. В серии тестов мыши Dup15q проявляли намёки на отличия в социализации и коммуникации и, наиболее явно, проблемы с когнитивной гибкостью. В задаче с водным лабиринтом и нормальные, и Dup15q‑мыши выучивали положение скрытой платформы. Но когда платформу перемещали, животные Dup15q медленно бросали старое место и адаптировались к новому — лабораторный параллель жёстких рутин, часто встречающихся при аутизме. Команда также записывала электроэнцефалограмму (ЭЭГ), суммарные ритмы множества нейронов. Как и у людей с Dup15q, у мышей наблюдалась необычно сильная бета‑активность — быстрый ритм, который часто усиливают препараты, усиливающие GABAA‑рецепторы, что подтверждает идею об избыточной активности их тормозной системы.
Целевой препарат, который ослабляет тормоза
Чтобы проверить, можно ли нормализовать это чрезмерное торможение, исследователи использовали RO4938581 — экспериментальное соединение, селективно ослабляющее GABAA‑рецепторы типа альфа-5, не затрагивая другие формы. В срезах гиппокампа препарат снизил величину тормозной передаваемой заряда у нейронов Dup15q, компенсируя избыток торможения. При ежедневном приёме внутрь в течение нескольких недель тот же препарат улучшал работу животных в фазе перестройки водного лабиринта, позволяя им адаптироваться к перемещённой платформе более похоже на здоровых мышей. Он также сблизил их социальное поведение с нормой. В записях ЭЭГ острая доза частично снизила преувеличенную бета‑мощность у мышей Dup15q, подталкивая их мозговые ритмы в сторону типичного паттерна.
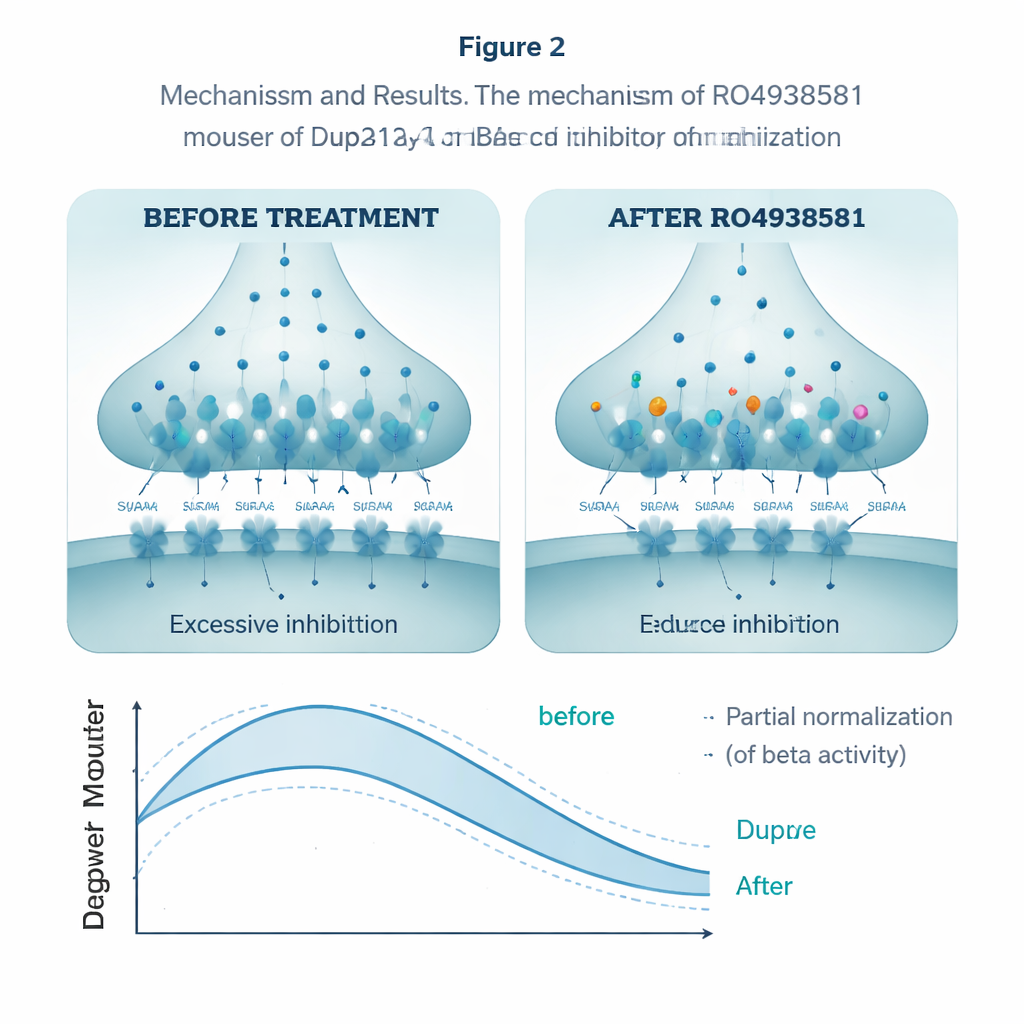
Что это может значить для будущих терапий
Для семей, живущих с синдромом Dup15q, эти результаты не являются немедленным лечением, но они дают конкретную зацепку. Работа указывает на один подтип рецептора — GABAA‑рецепторы, содержащие субъединицу альфа-5 — как на чрезмерно продуцируемый и функционально значимый в релевантной модели на животных. Умеренное снижение активности этого рецептора с помощью негативного модулятора, подобного RO4938581, не устранило все проблемы, но улучшило гибкое обучение, социальное поведение и ключевой ЭЭГ‑биомаркер. Такое сочетание изменений в мозге, поведении и биомаркере усиливает аргументы в пользу тестирования более безопасных, пригодных для людей препаратов, нацеленных на альфа-5, как прецизионных терапий для Dup15q и, возможно, родственных нарушений нейроразвития.
Цитирование: Nakagawa, R., Nani, F., Hipp, J.F. et al. RO4938581, a GABAA-α5 negative allosteric modulator rescued behavioral and EEG phenotypes of a mouse model of Dup15q syndrome. Mol Psychiatry 31, 1351–1360 (2026). https://doi.org/10.1038/s41380-025-03247-y
Ключевые слова: синдром Dup15q, GABAA рецептор альфа-5, нарушение нейроразвития, ЭЭГ бета-мощность, модель на мышах