Clear Sky Science · ru
Каскадная инерционная микрофлюидика для высокопроизводительного, многомасштабного обогащения опухолевых клеток и интактных кластеров в направлении улучшенной диагностики злокачественности
Почему важно сортировать раковые клетки в жидкости
Когда рак распространяется, опухолевые клетки часто попадают в жидкости, окружающие органы. У пациентов с раком легких это может быть жидкость, накапливающаяся вокруг легких — так называемый плевральный выпот. В этой жидкости скрываются редкие одиночные опухолевые клетки и плотные скопления клеток. Считается, что такие кластеры особенно опасны, поскольку они тесно связаны с агрессивным течением болезни и плохим прогнозом. Однако существующие лабораторные методы испытывают трудности с бережным и эффективным извлечением как одиночных клеток, так и кластеров из больших объемов биологической жидкости пациента. В этой работе представлена новая чиповая технология, которая может быстро и аккуратно сортировать эти клетки из плеврального выпота, открывая путь к более надежной диагностике рака и лучшему пониманию механизмов метастазирования.
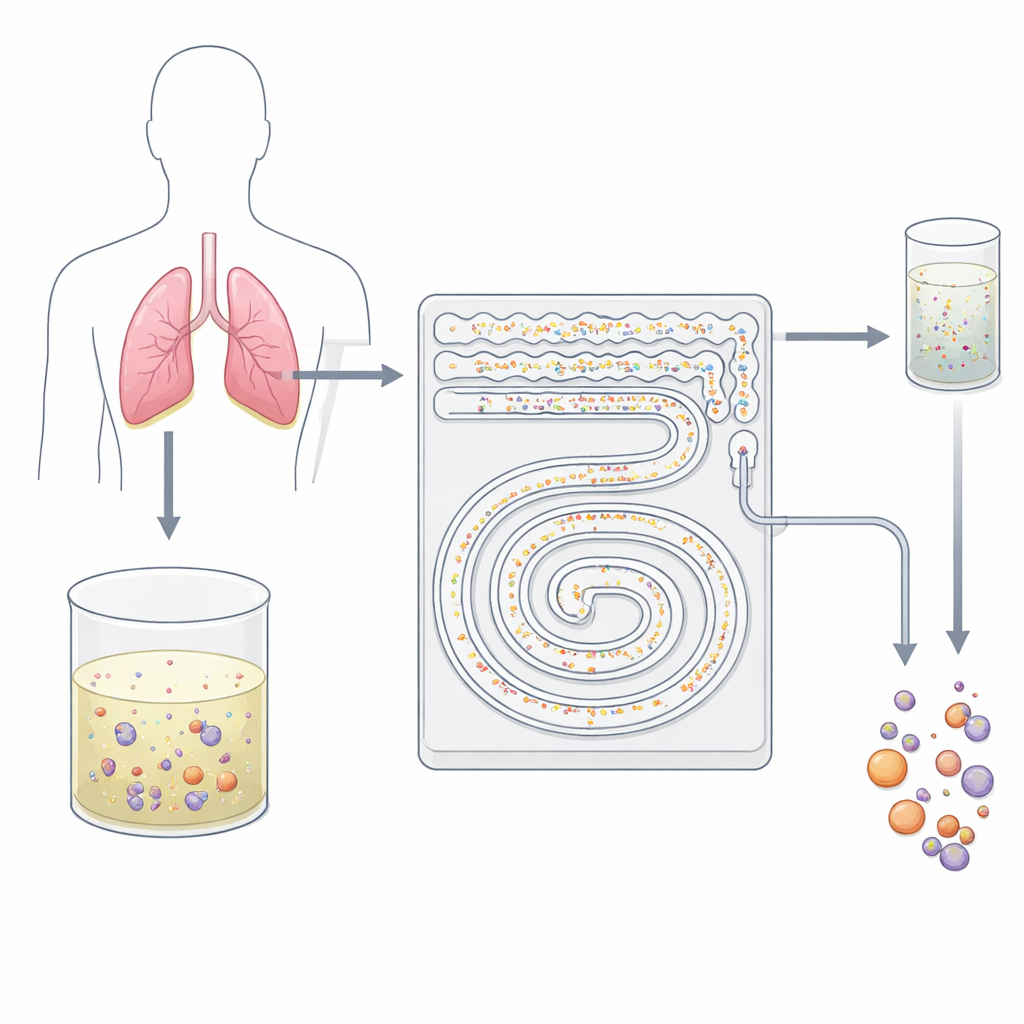
Деликатная «сито» для клеток на чипе
Исследователи разработали пластиковое устройство размером с ладонь с тонкими каналами, действующими как интеллектуальный двухступенчатый фильтр. Вместо использования липких антител или грубой фильтрации чип опирается на поведение клеток в быстротекущей жидкости. Когда поток проходит через изогнутые микроканалы, невидимые силы смещают частицы разного размера в разные струи. Команда использовала этот эффект, широко известный как инерционная микрофлюидика, чтобы отделить мелкие фоновые кровяные клетки от более крупных опухолевых клеток и их кластеров без контакта или маркировки. Поскольку всё происходит в непрерывном закрытом потоке, устройство способно обрабатывать десятки миллилитров жидкости за считанные минуты — то, что традиционная цитология на слайдах выполнить непросто.
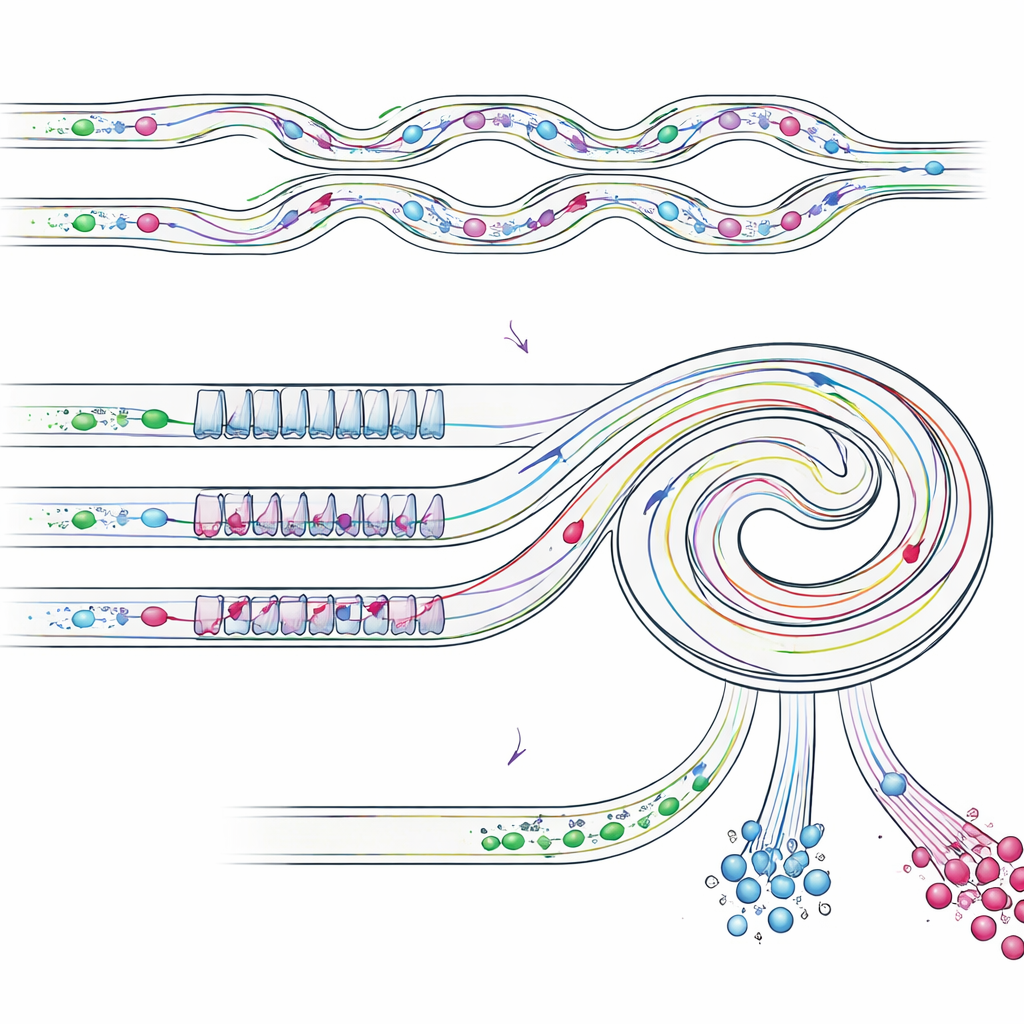
Первый этап: расчистка толпы
На первом этапе устройства плевральный выпот — после удаления лишней жидкости и перевзвешивания клеток — пропускают через массив параллельных змееобразных каналов. Здесь закручивающийся изогнутый поток отталкивает мелкие лейкоциты к стенкам канала, тогда как более крупные опухолевые клетки и кластеры остаются ближе к центру струи. Мелкие клетки направляются в отводы для отходов, что значительно разрежает фон. Этот высокопроизводительный этап может работать примерно на 8 миллилитров в минуту, то есть типичный клинический образец в 50 миллилитров можно обработать примерно за шесть с половиной минут без засорения. На выходе из первого этапа получается намного более чистая смесь, обогащенная потенциально злокачественными клетками и готовая для более тонкого разделения.
Второй этап: разделение одиночных клеток и кластеров
Частично обогащенный образец затем попадает в наклонный спиральный канал с повторяющимся узором узких и широких участков. На этом этапе различные силы потока уравновешиваются по‑разному для объектов разного размера, направляя их в отдельные полосы у внутренней или внешней стенки спирали. Одиночные клетки, которые меньше, выстраиваются в одну боковую позицию, тогда как более крупные кластеры мигрируют в другую позицию ближе к внутренней стенке. Размещая отводы в нужных точках, чип физически разделяет эти потоки: один отвод собирает преимущественно одиночные опухолевые клетки, другой — интактные кластеры, а остальные отводы удаляют оставшиеся мелкие клетки. Важно, что кластеры остаются целыми, избегая повреждений и разрушения, часто наблюдаемых при традиционных методах фильтрации.
Проверка устройства
Чтобы оценить эффективность конструкции, команда сначала использовала пластиковые шарики известных размеров, имитировавшие клетки крови, одиночные опухолевые клетки и кластеры. Они показали, что каскадный чип возвращает более 87% «одиночных» шариков и около 92% «кластерных» шариков, при этом удаляя большинство более мелких «кровяных» шариков. Затем экспериментировали с реальными клетками рака легких (клетки A549), смешанными с лейкоцитами. В этих тестах устройство в целом извлекало около 82% раковых клеток, с примерно 76% чистотой в обогащенной фракции и почти 80% чистотой для фракции кластеров. Наконец, они обработали реальные образцы плеврального выпота от трех пациентов с раком легких. Начиная с жидкости, где опухолевые клетки и кластеры составляли менее 1% всех клеток, чип давал фракции, в которых одиночные злокачественные клетки составляли около 68% всех клеток, а кластеры — около 35% клеток в выделенной струе.
Что это может значить для пациентов
Используя только поток жидкости и геометрию каналов, это устройство может быстро и аккуратно извлекать как одиночные опухолевые клетки, так и интактные кластеры из больших объемов пациентской жидкости без химических меток или сложной аппаратуры. Обогащенные клетки остаются пригодными для стандартных анализов, таких как иммуннофлуоресцентная окраска и микроскопия, что позволяет легко интегрировать процесс в существующие клинические рабочие потоки. Хотя текущее исследование включало небольшое число пациентов и потребует более крупных испытаний для подтверждения влияния на диагностику и прогноз, работа демонстрирует мощную концепцию: быстрый, безметочный «концентратор клеток», раскрывающий и количество, и состояние кластеризации опухолевых клеток в плевральном выпоте. В долгосрочной перспективе такие инструменты могут улучшить оценку злокачественности, помочь в выборе персонализированной терапии и дать более ясное представление о том, как происходят метастазы.
Цитирование: Zhu, Z., Ren, H., Zhang, Z. et al. Cascading inertial microfluidics for high-throughput, multi-scale enrichment of tumor cells and intact clusters towards enhanced malignancy diagnosis. Microsyst Nanoeng 12, 101 (2026). https://doi.org/10.1038/s41378-026-01235-y
Ключевые слова: жидкостная биопсия, микрофлюидная сортировка клеток, кластеры опухолевых клеток, плевральный выпот, диагностика рака