Clear Sky Science · ru
Платформа для меток-независимого биосенсинга с экстремальной чувствительностью на основе топологически нарушающей фазовой нанооптики
Почему важно видеть невидимое
Многие заболевания, включая рак и нейродегенеративные расстройства, выбрасывают в кровь характерные молекулы задолго до появления симптомов. Современные диагностические тесты часто пропускают эти ранние признаки, потому что молекулы слишком малы или их слишком мало для надёжного обнаружения. В этой работе представлен новый оптический сенсор, который способен обнаруживать ничтожно малые количества таких биомолекул без использования флуоресцентных меток или химических бирк. Путём конструирования вещества на масштабе нескольких атомов авторы используют тонкие сдвиги света, превращая крохотные биохимические события в крупные, легко измеримые сигналы.
Превращение света в сверхчувствительный детектор
Обычные плазмонические биосенсоры работают, подсвечивая тонкую металлическую плёнку и наблюдая, как меняется отражённый свет при адсорбции молекул на поверхности. Эти устройства уже чувствительны, но испытывают трудности с очень малыми молекулами или экстремально низкими концентрациями. Вместо отслеживания яркости или цвета новая платформа фокусируется на фазе света — точной синхронизации его волны. При специальных условиях отражённый свет почти исчезает, а его фаза меняется чрезвычайно резко. Эти точки, известные как оптические «тёмные» состояния или фазовые сингулярности, делают систему исключительно отзывчивой даже на незначительные изменения вблизи металлической поверхности.
Создание наноразмерной ловушки для света
Чтобы получить эти сингулярности, команда спроектировала многослойную структуру толщиной всего в несколько десятков нанометров. Стеклянная подложка поддерживает 12-нанометровый слой оксида алюминия с ультра-малыми серебряными наночастицами диаметром менее 3 нанометров, сверху покрытыми гладкой 48-нанометровой золотой плёнкой. Серебряные частицы тщательно формируются и встраиваются так, чтобы они оставались кристаллическими, почти сферическими и равномерно разнесёнными на субнанометрические расстояния. Такая конфигурация позволяет локализованным плазмонным модам частиц сильно взаимодействовать как друг с другом, так и с распространяющимися плазмонными волнами в золотом слое. В результате получается нечто вроде нанооптической полости, в которой энергия света тесно локализуется, а его фаза становится чрезвычайно чувствительной к окружающей среде.
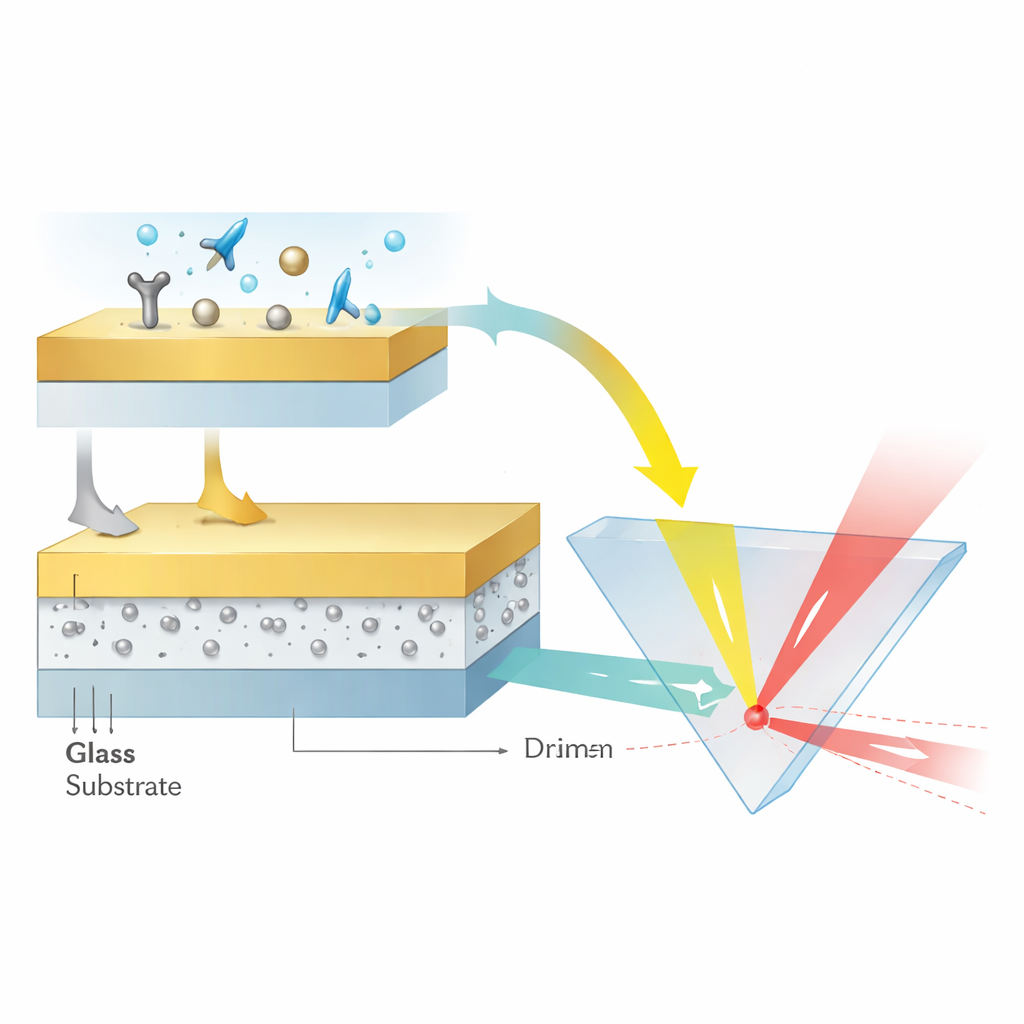
Заставляя свет сдвигаться вбок
Вместо измерения углов или цветов авторы считывали показания сенсора, отслеживая, насколько сильно отражённый лазерный луч смещается боково вдоль поверхности — явление, известное как сдвиг Гооса–Хэншена. Когда лазерный пучок отражается при подходящих условиях, его энергетический максимум может появиться слегка смещённым относительно предсказания простой геометрии. Вблизи фазовой сингулярности это смещение резко увеличивается. Подбирая концентрацию серебряных наночастиц примерно до 16 процентов, команда довела отражательность почти до нуля и заострила фазовый скачок так, что крошечные изменения показателя преломления, вызванные связыванием молекул на золотой поверхности, вызывали боковые сдвиги пучка в сотни микрометров. В калибровочных тестах с разреженными растворами глицерина устройство достигло чувствительности, эквивалентной 3.27 × 10^8 нанометров сдвига пучка на единицу изменения показателя преломления, и разрешало изменения порядка четырёх частей на десять миллионов.
Обнаружение крошечных молекул при ничтожно малых концентрациях
Чтобы продемонстрировать практический биосенсинг, исследователи сначала нацелились на биотин — молекулу размером с витамин с очень малой молекулярной массой. Стандартные поверхностные плазмонные сенсоры не способны надёжно видеть биотин даже при микромолярных концентрациях. Здесь, украсив золотую поверхность стрептавидином, который прочно связывает биотин, новая платформа чётко отслеживала связывание в реальном времени при концентрациях до 1 фемтомоля — примерно одна молекула на 10^15 молекул растворителя. Сигнал устойчиво увеличивался с каждым десятикратным ростом концентрации, что подтверждает предсказуемую зависимость сдвига пучка от покрытия такими крошечными анализируемыми молекулами.
Поиск онкологических маркеров в аттомасштабе
Затем команда переключилась на клинически значимую мишень: фактор некроза опухолей-альфа (TNF-α), цитокин, связанный с воспалением и раком, присутствующий в сыворотке пациентов примерно на уровне 10^−13 моляр. Они функционализировали золотую поверхность короткими цепочками ДНК (аптамерами), которые специфически захватывают TNF-α, и блокировали оставшиеся участки, чтобы подавить неспецифическое связывание. В этих условиях сенсор регистрировал чёткие, стабильные сигналы для TNF-α при концентрациях до 0.1 аттомоля (10^−19 моляр) и давал сдвиг почти 47 микрометров при 10^−13 моляр, что находится в пределах медицински релевантного диапазона. Контрольные тесты с другим цитокином, интерлейкином-6, дали почти отсутствующий длительный сигнал, подтверждая, что отклик был одновременно высокочувствительным и селективным.
Что это означает для будущих медицинских тестов
Проще говоря, эта работа показывает, что тщательно расположенные серебряные наночастицы, скрытые под тонким слоем золота, могут превратить почти неощутимое изменение на поверхности в большое боковое движение света, которое легко измерить. Работая в области фазовых сингулярностей, платформа обходится без флуоресцентных меток и выводит чувствительность в зепто- — до аттомолярного диапазона для реальных биологических мишеней. В случае перевода в надёжные, удобные в использовании устройства такие сенсоры могли бы позволить проводить анализы крови, обнаруживающие маркеры заболеваний задолго до существующих методов, открывая новые возможности для ранней диагностики и мониторинга здоровья в реальном времени.
Цитирование: Du, F., Gireau, M., Youssef, J. et al. Extreme sensitivity label-free biosensing platform based on topologically disruptive phase nano-optics. Microsyst Nanoeng 12, 106 (2026). https://doi.org/10.1038/s41378-026-01222-3
Ключевые слова: биосенсинг без меток, плазмонический датчик, наночастицы, раннее обнаружение заболеваний, онкологические биомаркеры