Clear Sky Science · ru
Пегилированные гибридные нанопластины WS2, легированные медью, для целевой мультимодальной терапии рака
Почему важны более разумные методы лечения рака
У многих людей с раком молочной железы по‑прежнему остаются жесткие методы лечения, которые могут повреждать здоровую ткань и при этом не полностью останавливать опухоль. В этом исследовании описан новый тип крошечных инженерных пластин, слишком малых, чтобы видеть их невооруженным глазом, созданных для перемещения по организму, нацеливания на опухоли молочной железы и одновременного воздействия на них несколькими согласованными способами. Объединив нагрев, химическое воздействие и классический противораковый препарат в одном целевом пакете, исследователи стремятся сделать лечение одновременно более эффективным и менее вредным для остального организма. 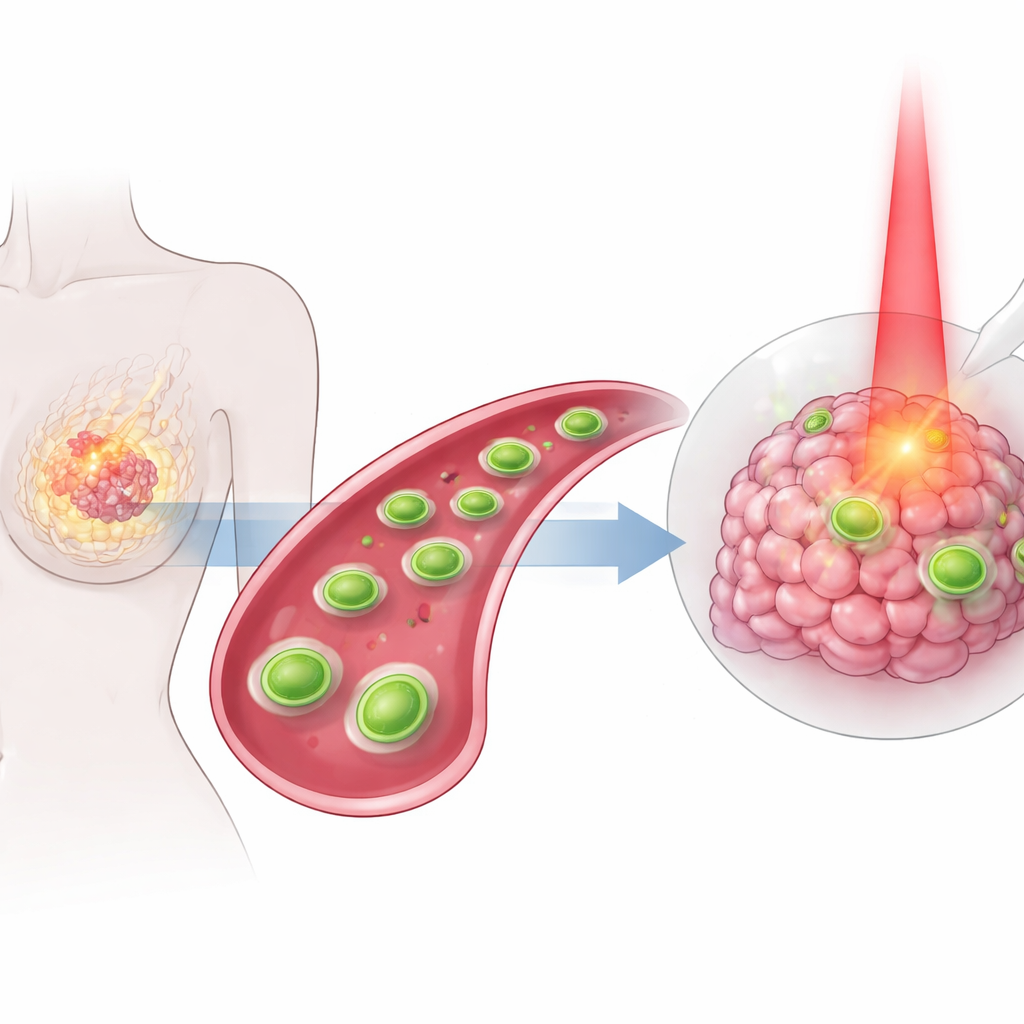
Крошечные пластины, созданные для переноса и доставки лечения
В основе подхода — ультратонкий материал из вольфрама и серы в форме нанопластин. Эти пластины естественным образом поглощают ближний инфракрасный свет и превращают его в тепло. Команда сначала синтезировала эти пластины, а затем аккуратно шероховила их поверхность, чтобы они могли удерживать другие полезные компоненты. Атомы меди были закреплены на пластинах в сильно диспергированном виде, а мягкое, гибкое покрытие, похожее на молекулярный «дождевик», добавили, чтобы частицы лучше смешивались в биологических жидкостях и не образовывали сгустков. Наконец, к поверхности присоединили фолиевую кислоту — витамин, который многие опухолевые клетки активно поглощают, в роли навигационного маркера, и загрузили на поверхность распространенный химиотерапевтический препарат доксорубицин. В результате получилась крошечная многоуровневая платформа, способная циркулировать в крови, распознавать опухолевые клетки и доставлять значительную нагрузку лечения.
Как свет, химия и препарат работают вместе
Когда эти частицы достигают опухоли, происходит несколько согласованных процессов. При облучении области опухоли мягким красным лазером пластины вольфрам–серы эффективно нагреваются, повышая локальную температуру до уровня, который стрессирует и повреждает раковые клетки, не перегревая остальной организм. Одновременно атомы меди на пластинах реагируют с естественными молекулами пероксида, которые присутствуют в опухолях в повышенных концентрациях. Эта реакция превращает пероксид в очень агрессивные короткоживущие окислители, которые повреждают клеточные компоненты изнутри. Опухоли также, как правило, немного более кислые, чем здоровая ткань; в этой более кислой среде и под нагревом лазером связь между пластиной и доксорубицином ослабляется, что позволяет высвобождаться большему количеству препарата непосредственно там, где он нужен. Эти три эффекта — тепло, химическая атака и сфокусированная химиотерапия — заданы так, чтобы усиливать друг друга. 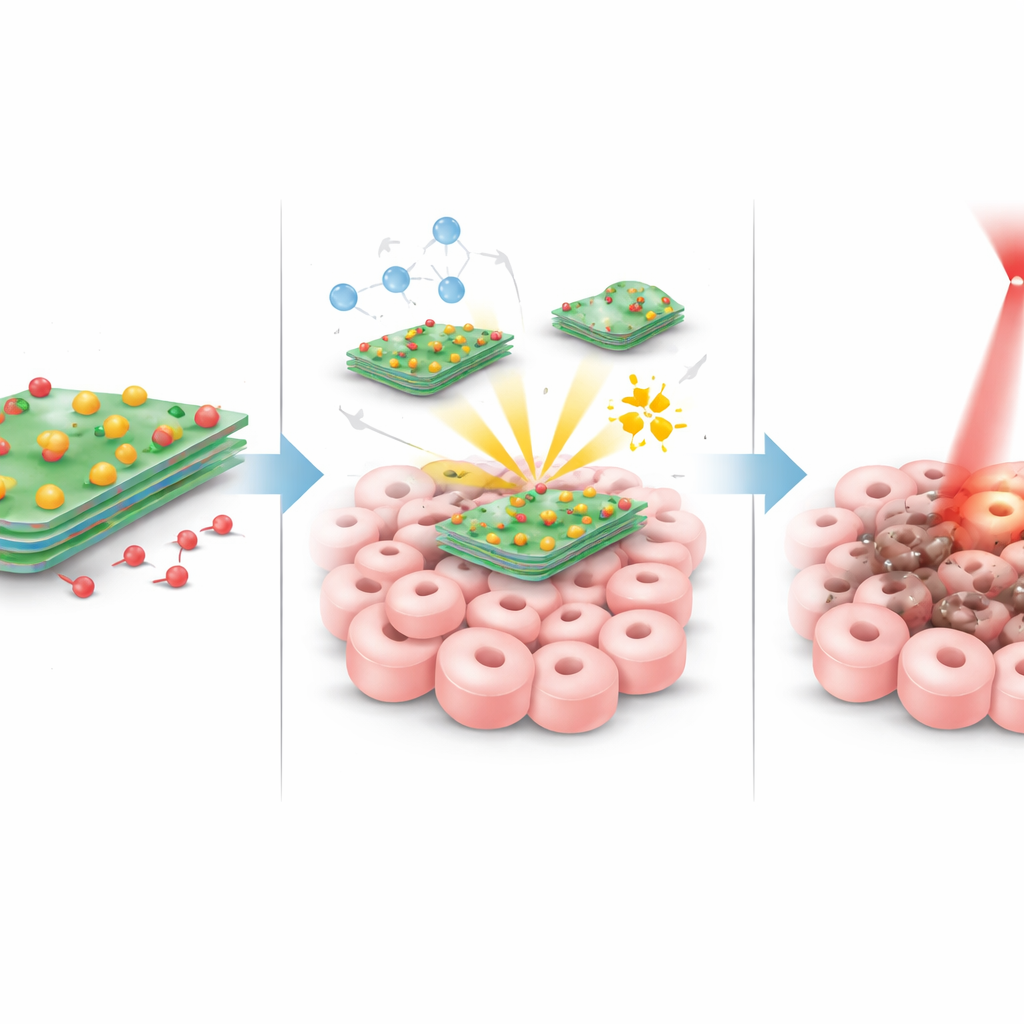
Доказательства из опытов на клетках и мышах с опухолями
В лабораторных культурах покрытые пластины сами по себе почти не вредили нормальным клеткам, что указывает на хорошую начальную безопасность. Но когда пластины были загружены доксорубицином и подвергнуты облучению лазером в присутствии пероксида, они вызывали сильную гибель клеток рака молочной железы, значительно большую, чем любое отдельное лечение. Исследователи также показали, что частицы генерируют всплеск реактивных окислителей внутри опухолевых клеток, подтверждая активность меди‑катализируемой химии. У мышей с опухолями молочной железы частицы с покрытием фолиевой кислотой накапливались в опухолевой ткани значительно сильнее и дольше, чем не нацеленные частицы. Когда мышам вводили полную комбинацию — целевые частицы и облучение красным светом — их опухоли заметно уменьшались, время выживания увеличивалось, а масса тела и здоровье органов в целом оставались нормальными, что указывает на ограниченные побочные эффекты по сравнению со стандартной терапией.
Что это может означать для будущей помощи при раке
В совокупности результаты указывают, что эти инженерные пластины действуют как многофункциональный инструмент для лечения рака: они находят опухоли, нагревают их, отравляют изнутри с помощью реактивной химии и точнее доставляют проверенный препарат, при этом щадя большую часть организма. Работа пока находится на стадии исследований на животных, и остаются важные вопросы о долговременной безопасности, разложении и оптимальном производстве таких частиц для применения у людей. Тем не менее конструкция демонстрирует, как объединение нескольких умеренных лечебных подходов в одном умном пакете, адаптированном к среде самой опухоли, может дать значительно более сильный общий эффект. Если будущие исследования подтвердят их безопасность и эффективность, такие многофункциональные наноплатформы могут сделать терапию рака молочной железы более целенаправленной, эффективной и менее истощающей для пациентов.
Цитирование: Li, D., Wen, C., Wu, H. et al. PEGylated Cu-doped WS2 hybrid nanosheets for targeted multimodal cancer therapy. Microsyst Nanoeng 12, 121 (2026). https://doi.org/10.1038/s41378-026-01218-z
Ключевые слова: терапия рака молочной железы, наномедицина, фототермическое лечение, целевой доставкой лекарств, хемодинамическая терапия