Clear Sky Science · ru
Роботизированная система переноса клеток на основе моделирования сопротивления микропипетки
Перемещение крошечных клеток без микроскопа
Современная биология часто опирается на удивительно простую операцию: подцепить одну клетку стеклянной трубкой и поместить её в другое место. Это необходимо для процедур лечения бесплодия, криоконсервации эмбрионов, клеточных терапий и базовых исследований. Тем не менее сегодня такая работа почти всегда требует громоздкого микроскопа и высококвалифицированного оператора, наблюдающего за каждым движением. В этой статье описана новая роботизированная система, способная перемещать отдельные клетки между каплями жидкости без какого‑либо микроскопического обзора, что открывает путь к полностью закрытым автоматизированным «клеточным фабрикам», работающим быстрее, дешевле и с меньшим вредом для хрупких клеток.
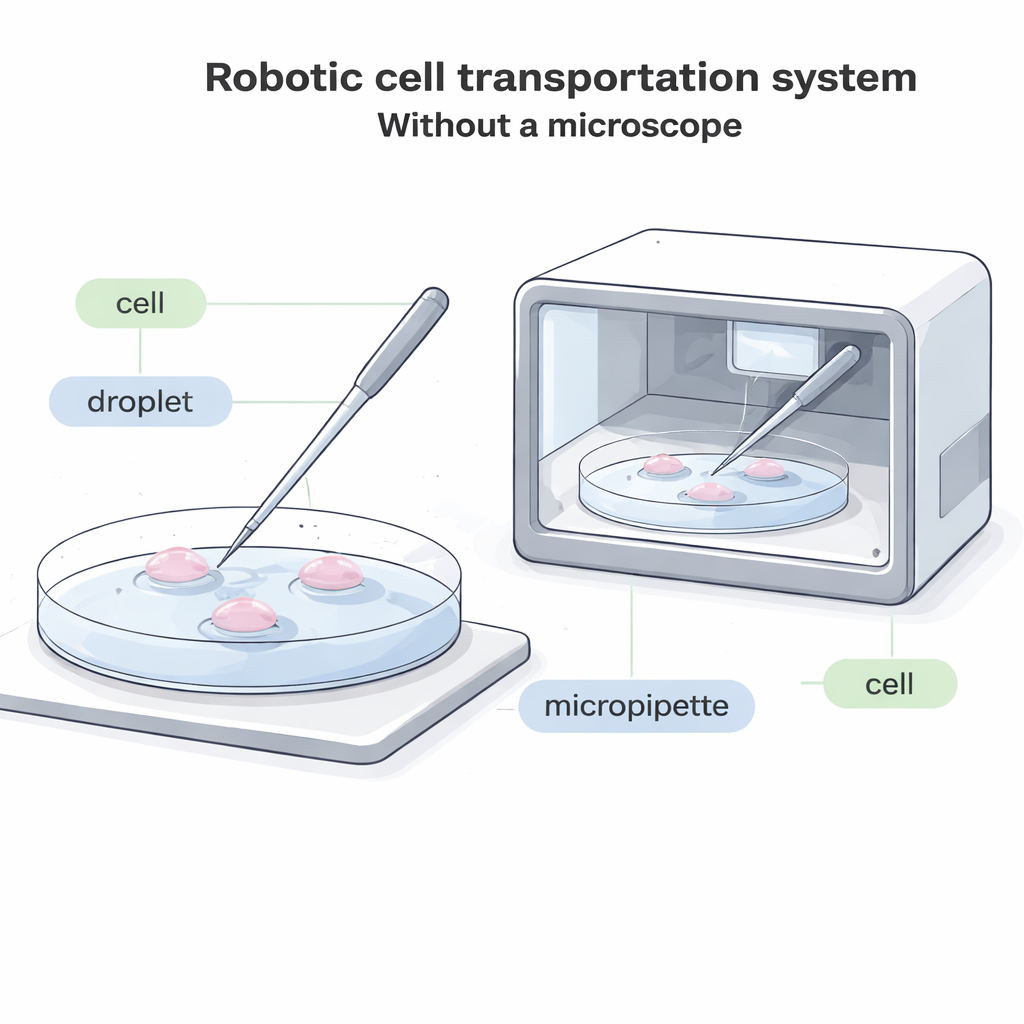
Почему перемещение клеток требует изменений
В современных лабораториях оператор смотрит в микроскоп и с помощью тонкой стеклянной трубки — микропипетки — касается дна чашки, аккуратно всасывает одну клетку, переносит её в новую каплю жидкости и затем выталкивает. Этот процесс медленный, визуально требовательный и трудноавтоматизируемый. В многих будущих системах — например компактных запечатанных устройствах для выращивания эмбрионов или других клеток внутри корпуса — просто не хватает места для традиционного микроскопа. В других случаях клетки метят флуоресцентными красителями, которые могут выцветать или повреждаться светом, поэтому важно минимизировать интенсивное микроскопическое наблюдение. Существующие «слепые» системы, не полагающиеся на изображение, работают только с необычно крупными клетками, оставляя большинство распространённых типов клеток без подходящего автоматического решения.
Особая трубочка с встроенной «пробкой»
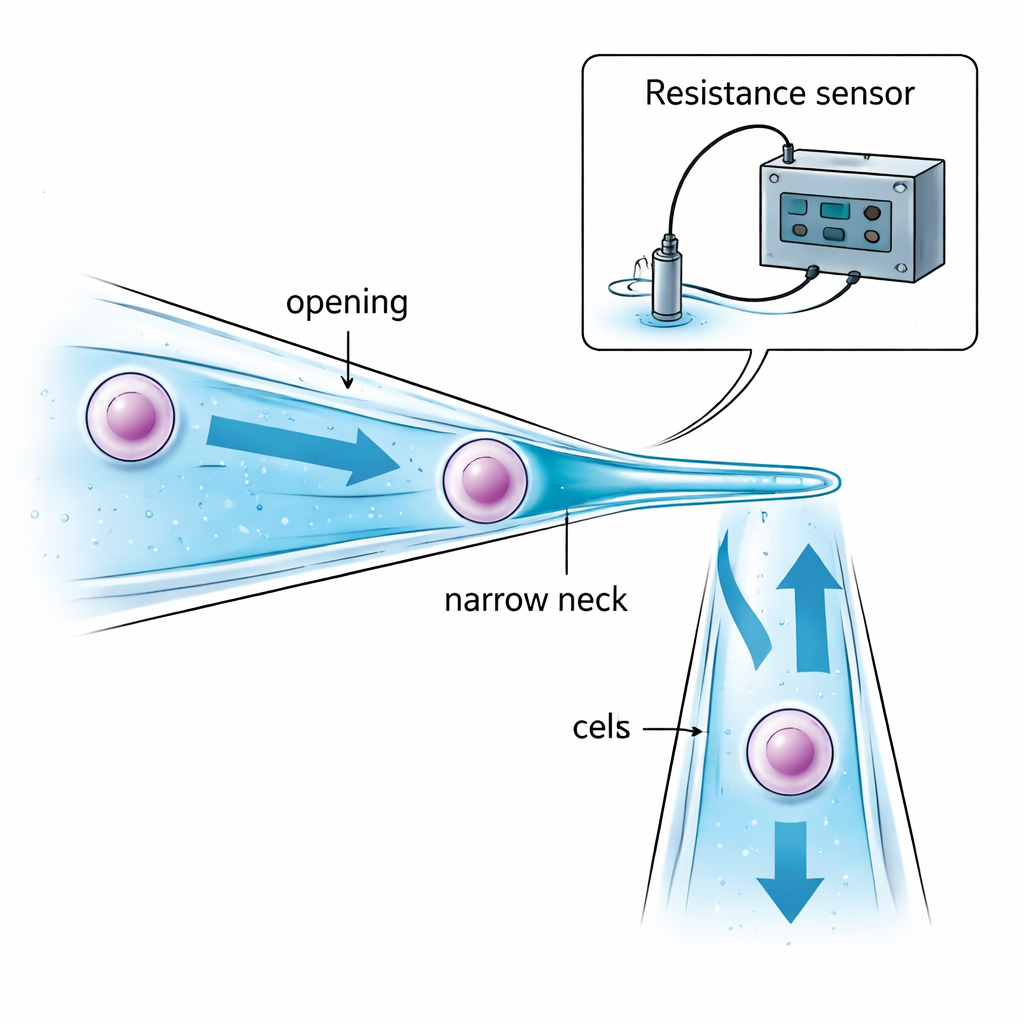
Авторы подходят к проблеме через переработку самой микропипетки. Вместо прямой стеклянной трубки одинакового диаметра по всей длине они создают микропипетку с узкой горловиной. Её отверстие немного шире целевой клетки, чтобы клетку можно было втянуть внутрь. Глубже по трубке диаметр плавно сужается до «горла», размер которого меньше клетки. Когда всасывание тянет клетку к этому сужению, клетка останавливается и удерживается внутри трубки — вместо того чтобы висеть на кончике и подвергаться воздействию масла или воздуха между каплями. Тщательный выбор размеров отверстия, горла и расстояния между ними обеспечивает надёжный захват клетки без чрезмерного сжатия и делает так, чтобы переносилось лишь небольшое количество жидкости из одной капли в другую, уменьшая риск загрязнения.
Слушая электрические сигналы вместо того, чтобы смотреть
Без микроскопа роботу всё равно нужно знать три вещи: когда стеклянный наконечник достаточно близок к дну чашки, когда клетка успешно захвачена в горле, и когда она полностью выпущена в новую каплю. Команда решает это, контролируя крошечные изменения электрического сопротивления в жидкости внутри и вокруг микропипетки. По мере приближения наклонённой пипетки к дну чашки зазор жидкости между ними уменьшается, и сопротивление предсказуемо растёт, сигнализируя о безопасной посадке чуть до контакта. Когда клетка блокирует узкое горло, путь тока через жидкость сужается и сопротивление внезапно скачет; когда клетку выталкивают, сопротивление так же резко падает. Математические модели этих сопротивлений — «зазорного», «аспирационного» и «инъекционного» — позволяют компьютеру интерпретировать сигналы в реальном времени и принимать решения о выключении всасывания или давлении без визуальной обратной связи.
Проверка робота в деле
Чтобы проверить работоспособность подхода на практике, исследователи собрали полноценную роботизированную установку, сочетающую управление движением, контроль давления, измерение сопротивления и хост‑компьютер. Они тестировали систему на небольших раковых клетках HeLa (примерно 10 микрометров в поперечнике) и значительно больших порционных яйцеклетках свиней (около 150 микрометров). Система надёжно обнаруживала посадку, захват и выпуск исключительно по сигналам сопротивления для широкого диапазона размеров пипеток. В прямых сравнениях робот переносил клетки HeLa с 90‑процентной частотой успешных операций — лучше, чем предыдущий автоматизированный метод с визуальным контролем — и транспортировал порционные яйца со 95‑процентным успехом, что выше стандартного микроскопического подхода. Время операции на одну клетку было сопоставимо или быстрее, чем при ручном управлении, главным образом потому, что узкая горловина устраняет необходимость в повторной тонкой настройке всасывания для позиционирования клетки.
Сохранение жизнеспособности и масштабирование
Любой робот‑помощник в лаборатории должен избегать повреждения обрабатываемых клеток. После переноса новой системой и клетки HeLa, и порционные яйцеклетки свиней культивировали в течение дня и окрашивали красителем, светящимся только в живых клетках. Уровни выживаемости при новом методе совпадали или близко подходили к показателям при традиционном переносе под микроскопом и к контрольным, неповреждённым клеткам, что указывает на то, что мягкое механическое сжатие в узкой горловине при правильно выбранных порогах заметного снижения жизнеспособности не вызывает. В перспективе авторы предполагают, что та же сенсорика на основе сопротивления и управление давлением может быть интегрирована в компактные микрофлюидные чипы. Это позволило бы многим каналам работать параллельно, обеспечивая высокопроизводительную, полностью закрытую обработку клеток, пригодную для автоматизированной репродуктивной медицины, клеточных терапий и долгосрочных устройств культивирования клеток, куда микроскопы трудно поместить.
Что это значит для будущей работы с клетками
Для неспециалистов главный вывод таков: перенос одиночных клеток больше не обязательно зависит от человека, смотрящего через микроскоп. За счёт тщательной формы стеклянной трубки и «прослушивания» того, как электричество течёт через окружающую жидкость, робот может почувствовать, когда он сел, схватил клетку и отпустил её — всё в темноте и в тесных пространствах. Это делает более практичным проектирование закрытых автономных систем культивирования клеток, которые защищают хрупкие образцы, упрощают клинические рабочие процессы и приближают лабораторную точность манипуляций клетками к автоматизированной, фабричной модели работы.
Цитирование: Zhao, Q., Liu, M., Zhu, R. et al. Robotic cell transportation system based on micropipette resistance modeling. Microsyst Nanoeng 12, 65 (2026). https://doi.org/10.1038/s41378-026-01193-5
Ключевые слова: манипуляция клетками, микропипетка, робототехника, микрофлюидика, автоматизация