Clear Sky Science · ru
Стратегии контроля пространственной организации клеток в микрофизиологических системах
Создание миниатюрных тканей в лаборатории
Наши органы эффективно работают потому, что их клетки расположены не случайным образом — они тщательно упорядочены в пространстве. В этой статье рассматривается, как учёные учатся воссоздавать этот сложный порядок внутри «органов-на-чипе» и других миниатюрных выращенных в лаборатории тканей. Направляя, где располагаются разные клетки и как они взаимодействуют, исследователи создают более правдоподобные модели сердца, мозга, кишечника, сосудов и даже экосистем «человек–микроорганизмы». Эти продвинутые системы обещают безопасные испытания лекарств, меньше экспериментов на животных и лучшие инструменты для изучения заболеваний и разработки персонализированных методов лечения.
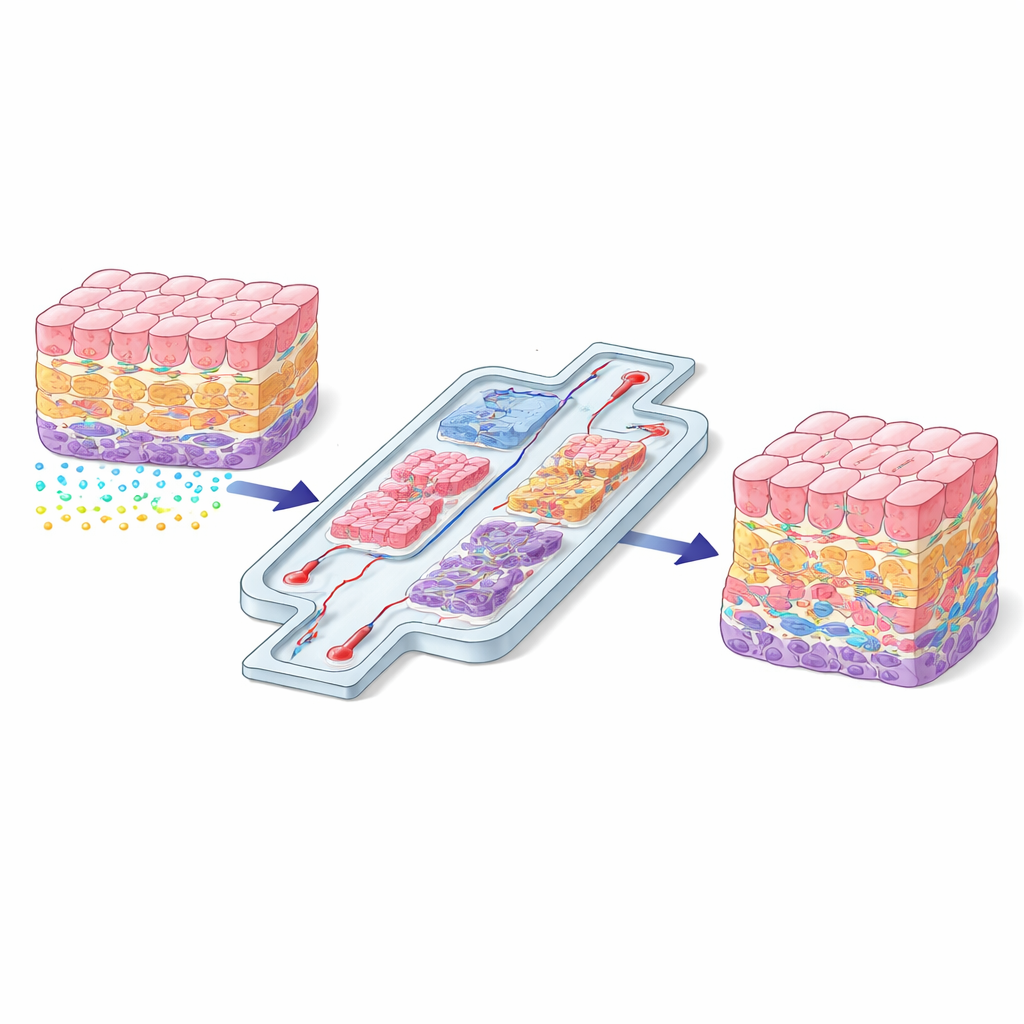
Почему положение клетки имеет значение
Внутри организма каждая клетка живёт в своём «районе» с уникальным сочетанием опорных структур, химических сигналов и физических сил. Клетка печени рядом с кровеносным сосудом ощущает совсем другие сигналы, чем клетка глубоко внутри органа. Эти различия по положению определяют, как клетки растут, во что они дифференцируются и как реагируют на повреждение или лекарства. Когда учёные выращивают клетки на плоских пластиковых чашках, эта пространственная «беседа» во многом теряется, и клетки часто ведут себя неестественно. Авторы утверждают, что воссоздание реалистичной пространственной организации — это не просто улучшение, а базовое требование, если выращенные в лаборатории ткани должны имитировать настоящие органы.
Два основных подхода к размещению клеток
Авторы объединяют существующие стратегии в две широкие группы: прямой и косвенный контроль. Прямые методы физически размещают клетки или отсеки точно там, где это необходимо. К ним относятся 3D биопечать, которая наносит слои клеток и мягких гелей как биологический 3D-принтер; микрофлюидные чипы, формирующие ткани в связанных камерах и каналах; и методы физической фиксации, которые направляют клетки в нужные позиции с помощью света, звука, магнитов или электрических полей. Эти подходы особенно ценны, когда важна точная геометрия — например, при воссоздании гематоэнцефалического барьера, слоистой стенки сосуда или пути течения от кишечника к печени.
Дать клеткам читать своё окружение
Косвенные методы, напротив, изменяют окружающую среду и позволяют клеткам делать остальное самостоятельно. Здесь учёные настраивают «ландшафт», который клетки ощущают: состав окружающего геля, жёсткость и текстуру поверхностей, градиенты растворённых веществ, таких как факторы роста или лекарства. Тщательно расставленные молекулы опоры могут заставлять определённые типы клеток оседать в заданных областях. «Умные» гидрогели, которые размягчаются или высвобождают сигналы по мере ремоделирования клетками, поощряют самоорганизацию структур, например сетей сосудов или крипт и ворсинок кишечника. Микрофлюидные устройства могут создавать стабильные химические градиенты, из-за которых стволовые клетки приобретают разные идентичности вдоль канала, а раковые и иммунные клетки мигрируют в отдельные зоны, раскрывая механизмы распространения заболеваний.
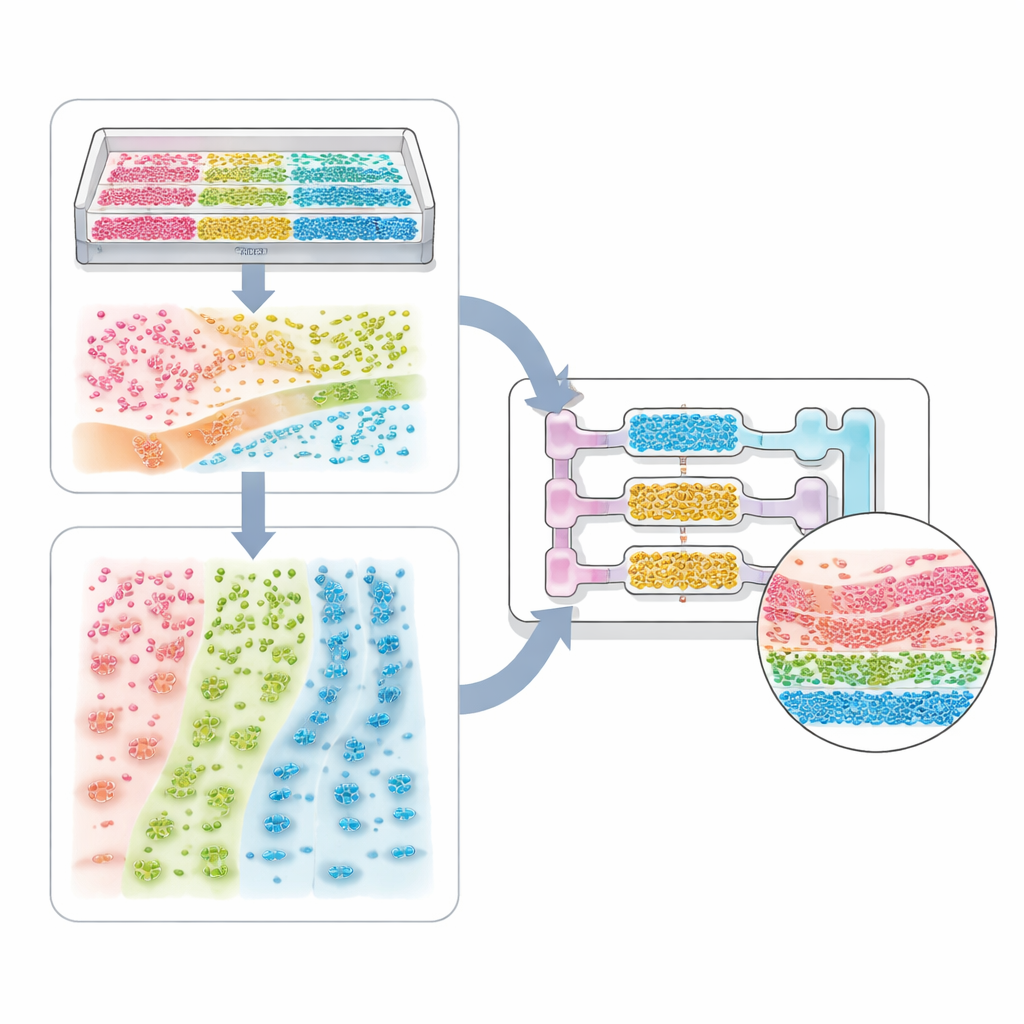
От систем из одного типа клеток до моделей всего организма
Обзор проходит через спектр приложений. На простейшем уровне это системы с одним типом клеток, где структурированные канавки или градиенты жёсткости позволяют кардиомиоцитам сокращаться синхронно или нейронам вытягивать выровненные волокна. Более сложные модели тканей смешивают несколько типов клеток — например, опухолевые клетки, клетки поддержки и сосудистые клетки — чтобы формировать сферы и органоиды с внутренними ядрами и оболочками. Микроканальные чипы и биопечать добавляют границы и поток, позволяя воссоздать альвеолы лёгких, фильтры почек, зоны печени и мультиорганные цепочки, отслеживающие, как лекарство всасывается, трансформируется и выводится. Те же идеи применимы к системам хозяин–микроб, где пространственное расположение бактерий вдоль стенки кишечника или через слой слизи определяет, защищают ли они нас или вызывают болезнь.
Как проверить, что узоры реальны
Поскольку эти системы становятся всё более сложными, учёным нужны надежные способы подтвердить, что клетки оказываются там, где положено, и ведут себя ожидаемо. В статье выделены методы визуализации, которые позволяют наблюдать за живыми клетками в движении и изменении со временем, а также продвинутые методы окрашивания и секвенирования, картирующие, какие гены, белки и метаболиты присутствуют в каждой точке. Датчики, встроенные в чипы, могут отслеживать кислород, питательные вещества, кислотность и механические силы, связывая локальные условия с реакциями клеток. Вместе эти инструменты помогают исследователям убедиться, что дизайн не только визуально правдоподобен, но и функционально соответствует реальной ткани.
Куда движется эта работа
Авторы заключают, что наиболее мощные системы будут сочетать прямые и косвенные стратегии: использовать чипы и биопринтеры для задания общей планировки, а затем вводить настраиваемые гели, текстуры и градиенты, которые позволяют тканям созревать и ремоделироваться со временем. Они также отмечают практические препятствия — такие как масштабирование производства, снижение вариабельности между лабораториями и этические вопросы, связанные со сложными моделями человеческих тканей. Тем не менее посыл ясен: овладение пространственной организацией ключевым образом превратит микрофизиологические системы в надёжные заместители человеческих органов, открывая новые возможности для изучения развития, тестирования терапий и индивидуализации медицины.
Цитирование: Truong, H.D., Ge, Z., Chng, E. et al. Strategies to control cellular spatial organization in microphysiological systems. Microsyst Nanoeng 12, 85 (2026). https://doi.org/10.1038/s41378-025-01141-9
Ключевые слова: organ-on-a-chip, пространственная организация клеток, 3D биопечать, микрофлюидные модельные ткани, микрофизиологические системы