Clear Sky Science · ru
Однотрубочная платформа на основе CRISPR для диагностики на месте с быстрой, специфичной и чувствительной детекцией HPV16 без предварительного амплифицирования
Почему важно распознавать именно один тип вируса
Рак шейки матки часто связан с инфекцией вирусами папилломы человека (ВПЧ), но не все типы ВПЧ несут одинаковый риск. Врачам нужны тесты, которые надежно различают эти очень близкие по последовательности вирусы, особенно высокорисковый тип HPV16. Проблема в том, что существующие генетические тесты иногда путают близких родственников, что приводит к ложным тревогам или пропуску случаев. В этом исследовании представлен новый метод тестирования, который значительно повышает как точность, так и практичность, стремясь внедрить точную субтипацию ВПЧ в клиники и точки оказания помощи.
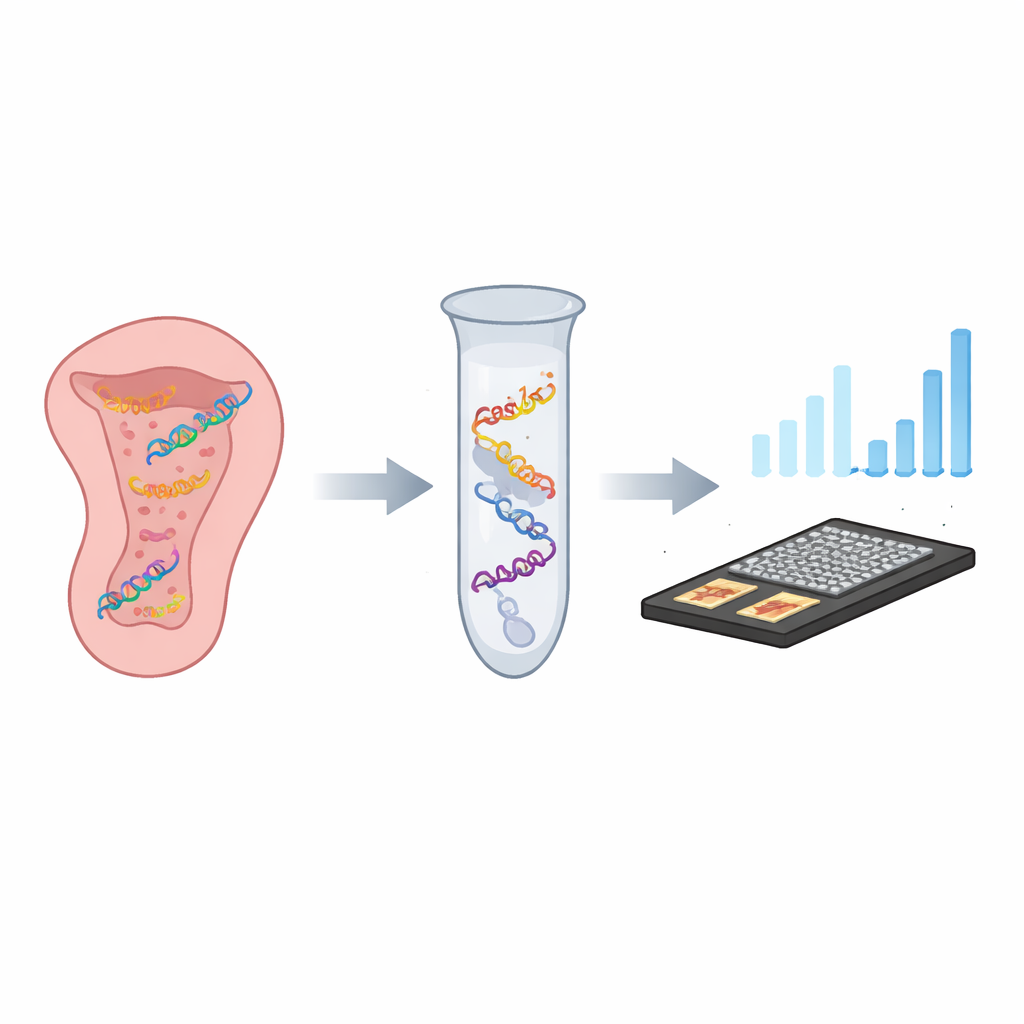
Умный молекулярный замок и ключ
Исследователи создали одноруководочный тест, который они называют CASTSA, объединяющий две мощные идеи: точность CRISPR, системы наведения на генетические участки, заимствованной из бактерий, и усиливающую сигнал способность ПЦР, стандартного метода копирования ДНК. В CASTSA белок CRISPR Cas12a наводится на генетическую последовательность HPV16 короткой направляющей РНК — «ключом». Когда он находит точное совпадение и рядом присутствует короткий узор, необходимый для его активности, Cas12a разрезает вирусную ДНК в предсказуемом месте. Этот разрез создает характерный свободный конец одной цепи ДНК, который служит уникальной отправной точкой для амплификации. Другие типы ВПЧ, даже с очень похожими последовательностями, либо не разрезаются, либо не формируют подходящую отправную точку, поэтому они не амплифицируются.
Преобразование крошечного надреза в сильный сигнал
Чтобы превратить разрез CRISPR в детектируемый сигнал, команда разработала специальный праймер ДНК, называемый терминальным праймером. Этот праймер прикрепляется правильно только к той цепи, которая образовалась после разреза Cas12a, затем складывается сам на себя как «шпилька» (hairpin) и помогает сформировать стабильный матрикс для ПЦР. Дополнительные «универсальные» последовательности праймеров затем присоединяются и запускают обычную количественную ПЦР в реальном времени. Ключевым является то, что амплификация происходит только если Cas12a сначала выполнил свою функцию и если праймер правильно свернулся, создавая два уровня проверки. Такая архитектура резко снижает вероятность непреднамеренной амплификации частично совпадающей, нецелевой ДНК, решая обычную проблему прежних CRISPR‑тестов, которые полагались на отдельный шаг предварительной амплификации.
Все в одной пробирке, с меньшим числом ошибок
Важным практическим достижением является то, что разрезание CRISPR и амплификация ПЦР происходят вместе в одной запаяной пробирке, что исключает необходимость открывать пробирки между этапами — важный источник контаминации в многих лабораторных протоколах. Авторы тщательно подбирали условия реакции, особенно уровни магния, так чтобы и Cas12a, и фермент копирования ДНК эффективно работали, не поощряя спонтанные реакции. Они показали, что их однопродуктовая схема надежно различает HPV16 от нескольких других высокорисковых типов, включая HPV18, 33, 45 и 52, несмотря на то, что эти вирусы имеют сильно консервативные генетические участки. По сравнению со стандартной количественной ПЦР или с CRISPR‑тестами, которые сначала амплифицируют ДНК, а затем проводят CRISPR‑детекцию, CASTSA дала значительно меньше вводящих в заблуждение сигналов от оф‑таргетных типов ВПЧ.
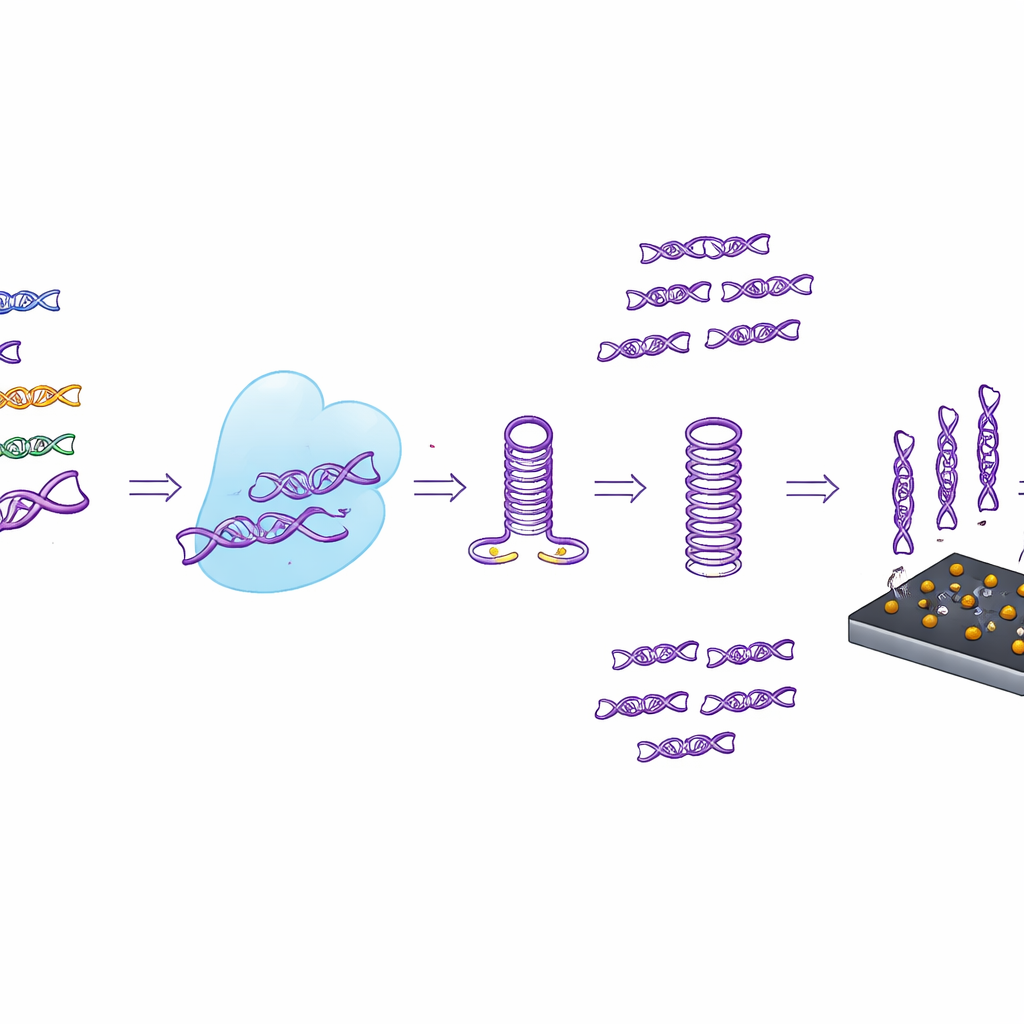
От пробирки к портативному сенсору
Вместо того чтобы полагаться только на флуоресцентные считывания, исследователи также связали CASTSA с компактным электрохимическим сенсором, изготовленным из лазерно‑индуцированного графена. Эта пористая, высокопроводящая углеродная поверхность украшена наночастицами золота, несущими захватные цепи, разработанные так, чтобы связываться только с продуктами амплификации CASTSA для HPV16. Когда эти продукты прилипают, электрический ток через сенсор изменяется измеримым образом. Используя массив из четырех электродов — три измерительные точки и одну встроенную контрольную фоновую — устройство может вычитать шум от неспецифического прилипания. В испытаниях эта интегрированная система обнаруживала всего 18 копий мишени HPV16 на реакцию, превзойдя чувствительность только флуоресцентного считывания и сохранив отличную повторяемость.
Как это может изменить тестирование на ВПЧ
Чтобы оценить работу метода в реальных условиях, команда протестировала 20 клинических образцов, известных наличием HPV16, и 10 образцов от здоровых доноров. CASTSA, как в форме с флуоресценцией, так и в сочетании с графеновым сенсором, полностью совпала с результатами стандартных госпитальных ПЦР‑тестов. При этом метод продемонстрировал превосходную способность игнорировать другие высокорисковые типы ВПЧ, которые часто приводят к путанице. Для пациентов это может означать меньше двусмысленных результатов и более уверенные решения о дальнейшем обследовании и лечении. В более широком смысле, стратегия CASTSA — сначала распознавание CRISPR, затем амплификация, все в одной запечатанной пробирке — предлагает шаблон для высокоспецифичных, с низкой контаминацией генетических тестов, которые могут быть адаптированы для многих патогенов и мутаций, особенно в условиях, где требуются быстрые и надежные ответы.
Цитирование: Chen, Y., Chen, Y., Zhang, C. et al. One-pot CRISPR-based point of care platform for rapid, specific and sensitive detection of HPV 16 without pre-amplification. Microsyst Nanoeng 12, 81 (2026). https://doi.org/10.1038/s41378-025-01130-y
Ключевые слова: обнаружение HPV16, диагностика CRISPR, тестирование на основе ПЦР, электрохимический биосенсор, анализ у постели пациента