Clear Sky Science · ru
JAK2V617F перенастраивает фактор HIF-1, индуцируя неклассический гипоксический регулон при миелопролиферативных неоплазиях
Почему это важно для рака крови
Некоторые медленно прогрессирующие заболевания крови, известные как миелопролиферативные неоплазии, могут годами тихо существовать, а затем внезапно превратиться в агрессивную лейкемию. В этом исследовании поставлен простой, но ключевой вопрос: как распространённая онкогенная мутация захватывает встроенную систему клетки по распознаванию кислорода, и можно ли нацелить это переадресацию специфично, не вредя здоровым клеткам? Ответы могут открыть новый подход к лечению пациентов высокого риска, одновременно щадя нормальные ткани, которые тоже зависят от сигналов кислородного ответа.
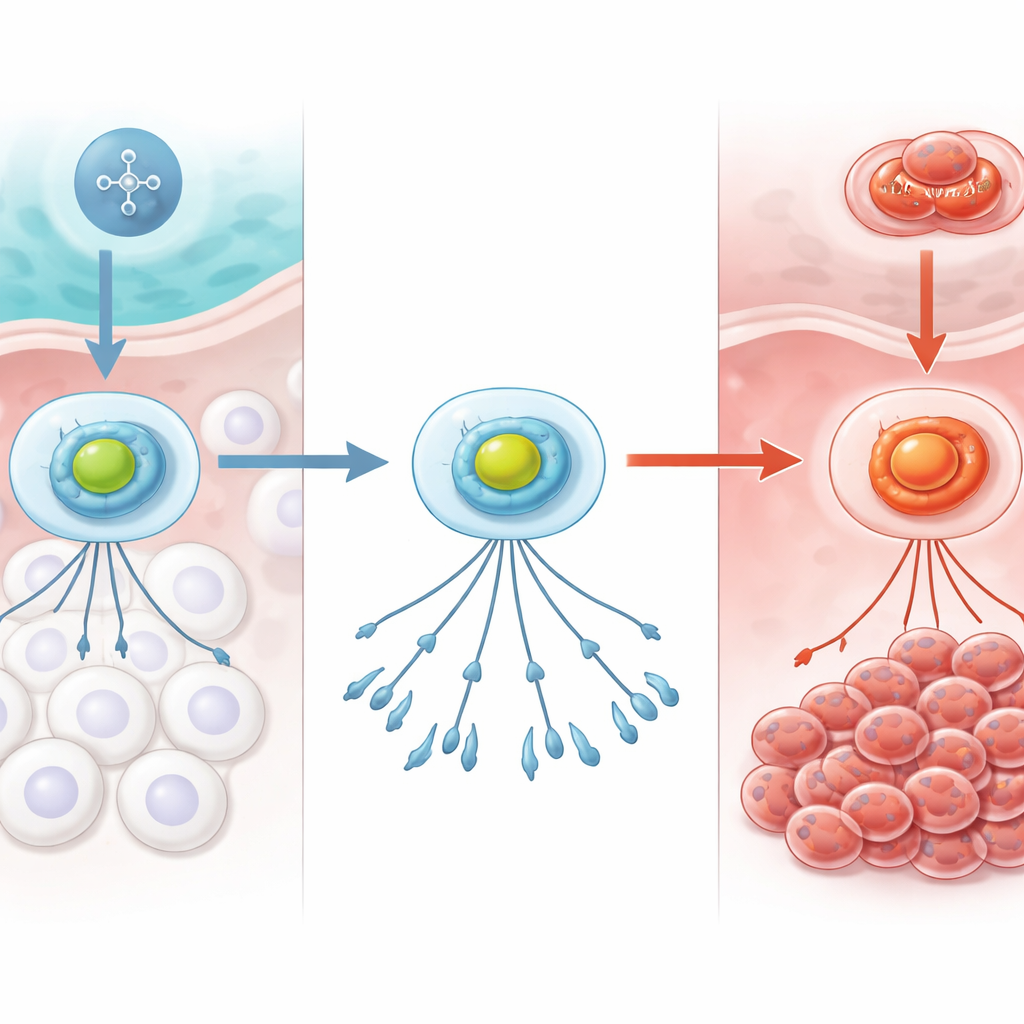
Система тревоги организма по кислороду
Клетки постоянно отслеживают доступность кислорода. В основе этой системы лежит белковый комплекс HIF‑1, который ведёт себя как «сигнализатор» при низком содержании кислорода. При нормальном, хорошо насыщенном кислородом состоянии один из субъединиц HIF‑1 быстро расщепляется, поддерживая сигнал в выключенном состоянии. Когда кислорода становится меньше, это разрушение останавливается, HIF‑1 стабилизируется, перемещается к ДНК клетки и включает гены, помогающие адаптироваться — например, меняя способы получения энергии или стимулируя рост новых сосудов. В раке та же система может работать на пользу опухоли, помогая злокачественным клеткам выживать в стрессовых условиях, таких как гипоксичное костномозговое пространство.
Когда мутация перенастраивает сигнализацию
Исследователи сосредоточились на мутации JAK2V617F, которая очень часто встречается при миелопролиферативных неоплазиях. Ранние работы показали, что эта мутация удерживает сигнал HIF‑1 включённым даже при достатке кислорода. На модельных линиях клеток команда сравнила участки связывания HIF‑1 с ДНК в двух состояниях: при истинной гипоксии и при нормальном содержании кислорода в присутствии мутации JAK2V617F. Они обнаружили, что в мутированных клетках HIF‑1 связывается с меньшим числом регионов генома, менее отзывчив на изменения в уровне кислорода и взаимодействует с другим набором партнёрских белков, многие из которых участвуют в обработке РНК. Иными словами, мутация не просто постоянно «включает» HIF‑1 — она перенастраивает сигнал на другой набор целей.
Рак-специфическая генная программа
На основе этих экспериментов авторы выделили несколько наборов генов, зависимых от HIF‑1, включая так называемый гипоксический сигнатур JAK2V617F. Затем они проверили, насколько сильно эти сигнатуры активированы в клетках крови 172 пациентов с миелопролиферативными неоплазиями, позитивными по JAK2V617F. Удивительно, но привычные гипоксические программы HIF‑1 не предсказывали тяжесть заболевания или продолжительность жизни пациентов. Напротив, мутация‑специфический гипоксический сигнатур чётко разделял пациентов с более тяжёлым течением болезни и был связан с худшей выживаемостью в целом. Многие гены в этом наборе были особенно активны в предшественниках мегакариоцитов — клетках костного мозга, которые чрезмерно разрастаются и приводят к фиброзу при этих расстройствах — и некоторые участвовали в репарации повреждений ДНК, процессе, который может помогать раковым клеткам переживать вредные воздействия.
Подсказки к внезапному ухудшению болезни
Главный страх пациентов — это внезапная трансформация хронического состояния в агрессивную «бластную» лейкемию. Проанализировав сопоставимые образцы пациентов до и после такой трансформации, команда выделила меньший набор из 13 генов, названный сигнатурой HIF1‑MPN‑BP, уровни которого повышались или снижались при переходе в бластную фазу. Этот набор был тесно связан с более высокими баллами риска, худшей выживаемостью и более выраженным фиброзом костного мозга. Что важно, этот профиль, по-видимому, специфичен для болезни, обусловленной JAK2V617F, а не универсальная черта всех лейкемий. Многие гены в этом поднаборе являются правдоподобными мишенями для лекарств, предлагая сфокусированный список кандидатов для будущих терапий, направленных на блокирование прогрессирования.
Поиск скрытого помощника мутации
Как JAK2V617F удерживает HIF‑1 активным независимо от кислорода? С помощью протеохимических подходов авторы обнаружили, что в мутированных клетках HIF‑1 несёт две ранее неизвестные химические метки (фосфорилирования) в участке, который обычно контролирует его распад. Эти изменения они проследили до киназы PIM1 — фермента, включающегося в сигнальном каскаде вниз по потоку от мутированного JAK2. Блокирование PIM1 экспериментальными препаратами приводило к снижению уровней HIF‑1 в мутантных клетках, при этом нормальный ответ на гипоксию оставался в значительной степени нетронутым. Ингибирование PIM1 также селективно уменьшало экспрессию рискованных генов HIF1‑MPN‑BP и сдвигало мутантные клетки в сторону гибели, не затрагивая их немутированные аналоги.
Что это значит для пациентов
Эта работа показывает, что один и тот же белок для распознавания кислорода, HIF‑1, ведёт себя по‑разному в зависимости от способа активации. При миелопролиферативных неоплазиях, вызванных JAK2V617F, сигнальная ось JAK2–PIM1 стабилизирует HIF‑1 таким образом, что он теряет нормальный кислородный контроль и сужает свою активность к набору генов, способствующих заболеванию. Поскольку эта изменённая программа тесно связана с тяжестью болезни и риском трансформации, и её можно подавить блокированием PIM1, она представляет собой перспективный путь для селективного подавления патологической активности HIF‑1 при сохранении его жизненно важной роли в здоровых тканях. Терапии, использующие это различие, в будущем могут помочь предотвратить переход медленно прогрессирующих заболеваний крови в угрожающую жизни лейкемию.
Цитирование: Kealy, D., Ellerington, R., Bansal, S. et al. JAK2V617F reprograms Hypoxia Inducible Factor-1 to induce a non-canonical hypoxia regulon in myeloproliferative neoplasms. Leukemia 40, 609–621 (2026). https://doi.org/10.1038/s41375-025-02843-9
Ключевые слова: миелопролиферативные неоплазии, JAK2V617F, HIF-1, киназа PIM1, трансформация в бластную фазу