Clear Sky Science · ru
Алнуктамаб — двуустный T‑клеточный энгейджер, нацеленный на антиген созревания B‑клеток, для пациентов с рецидивирующей или рефрактерной множественной миеломой: результаты фазы 1, первого исследования на людях
Почему этот новый противораковый препарат важен
Для людей с множественной миеломой — опухолью крови, которая почти всегда рецидивирует после лечения — каждая новая опция может означать больше времени и лучшее качество жизни. В этом исследовании оценивают иммунотерапию следующего поколения под названием алнуктамаб, разработанную чтобы помочь собственным клеткам‑защитникам организма находить и уничтожать миеломные клетки. Вопрос, который ставили исследователи, — практический и важный для пациентов и врачей: можно ли эту мощную терапию вводить простым подкожным уколом, получая при этом сильный противоопухолевый эффект при меньшем риске опасных побочных явлений?
Хитрый способ перенаправить иммунную систему
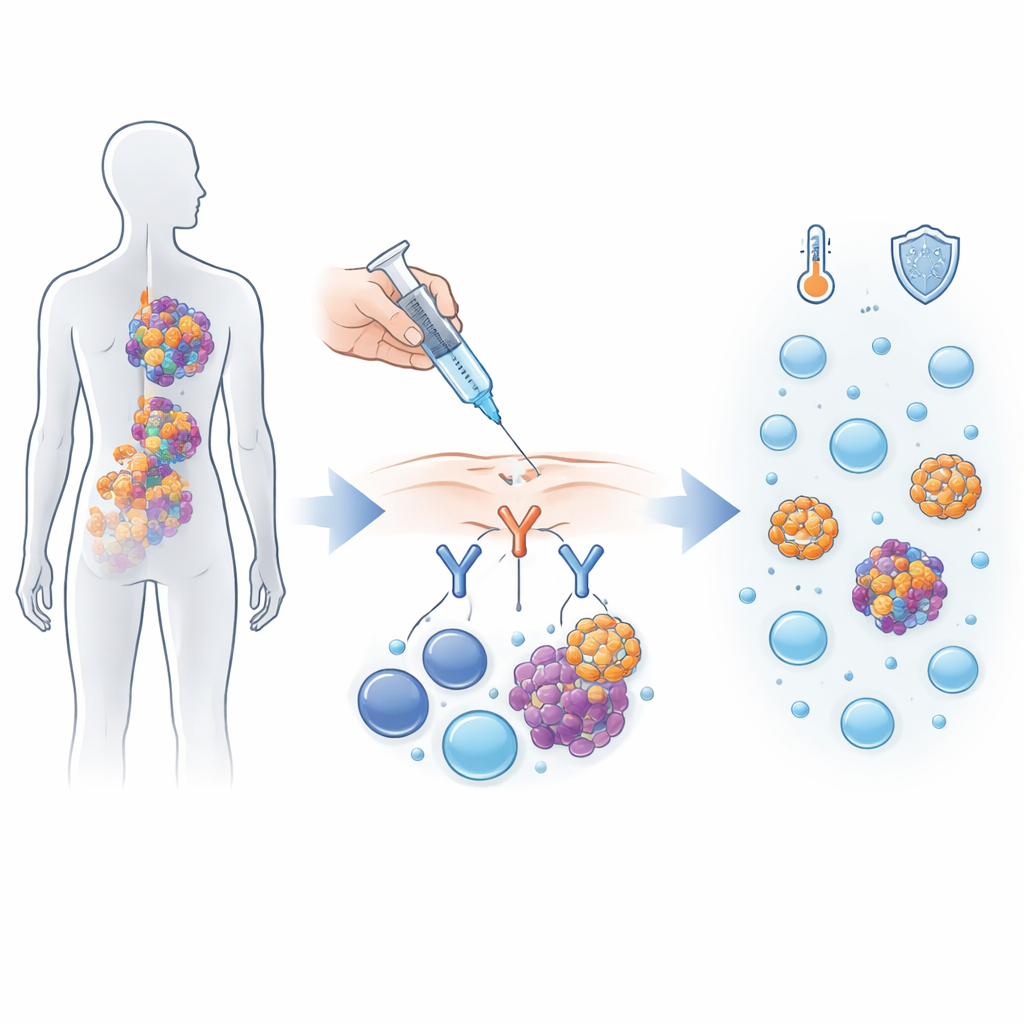
Алнуктамаб относится к новому классу препаратов, которые действуют как молекулярные свахи между раковыми и иммунными клетками. Миеломные клетки несут на поверхности маркер BCMA, а T‑лимфоциты — маркер CD3. Алнуктамаб сконструирован с двумя «руками», цепляющимися за BCMA, и одной «рукой», связывающейся с CD3, что притягивает T‑клетки в непосредственный контакт с миеломными клетками, чтобы те могли их атаковать. В этом первом клиническом исследовании на людях 165 пациентов с миеломой, вернувшейся после как минимум трёх различных видов терапии, получили алнуктамаб либо внутривенно, либо подкожно.
От инфузии к инъекции
Изначально препарат вводили внутривенно, но этот путь вызывал более сильные иммунные реакции, включая угрожающее жизни осложнение — цитокиновый шторм, при котором иммунная система резко выбрасывает большие количества провоспалительных сигналов. Из‑за этих проблем с безопасностью и лишь умеренной эффективностью исследование переключили на подкожное введение, при котором препарат высвобождается более постепенно. Девяносто пять пациентов лечились таким образом по «шаговой» схеме: небольшие стартовые дозы с последующим повышением до целевой, а частота инъекций постепенно снижалась со еженедельного режима до введения раз в четыре недели при продолжении терапии.
Как пациенты реагировали и с чем сталкивались
Среди всех получавших подкожные инъекции примерно 59% наблюдали уменьшение опухоли минимум вдвое, а почти половина достигла состояния «минимальной остаточной болезни отрицательной» (MRD‑отрицательной), то есть при высокочувствительных тестах миеломные клетки в костном мозге не выявлялись. При рекомендованной дозе 30 миллиграмм ответы были ещё лучше: примерно 71% пациентов ответили на лечение и более половины достигли MRD‑отрицательности. Многие пациенты контролировали болезнь почти год и дольше, даже по мере ослабления режима дозирования. Побочные эффекты были частыми, но в основном управляемыми. Лихорадочные иммунные реакции возникали примерно у трёх из пяти пациентов, но все они были лёгкой или средней тяжести. Наблюдалось снижение уровня белых кровяных клеток и инфекции, что отражает и мощь препарата, и уязвимость иммунной системы пациентов, однако серьёзные инфекции встречались реже, чем описано для некоторых похожих препаратов.
Почему подкожный путь оказался безопаснее
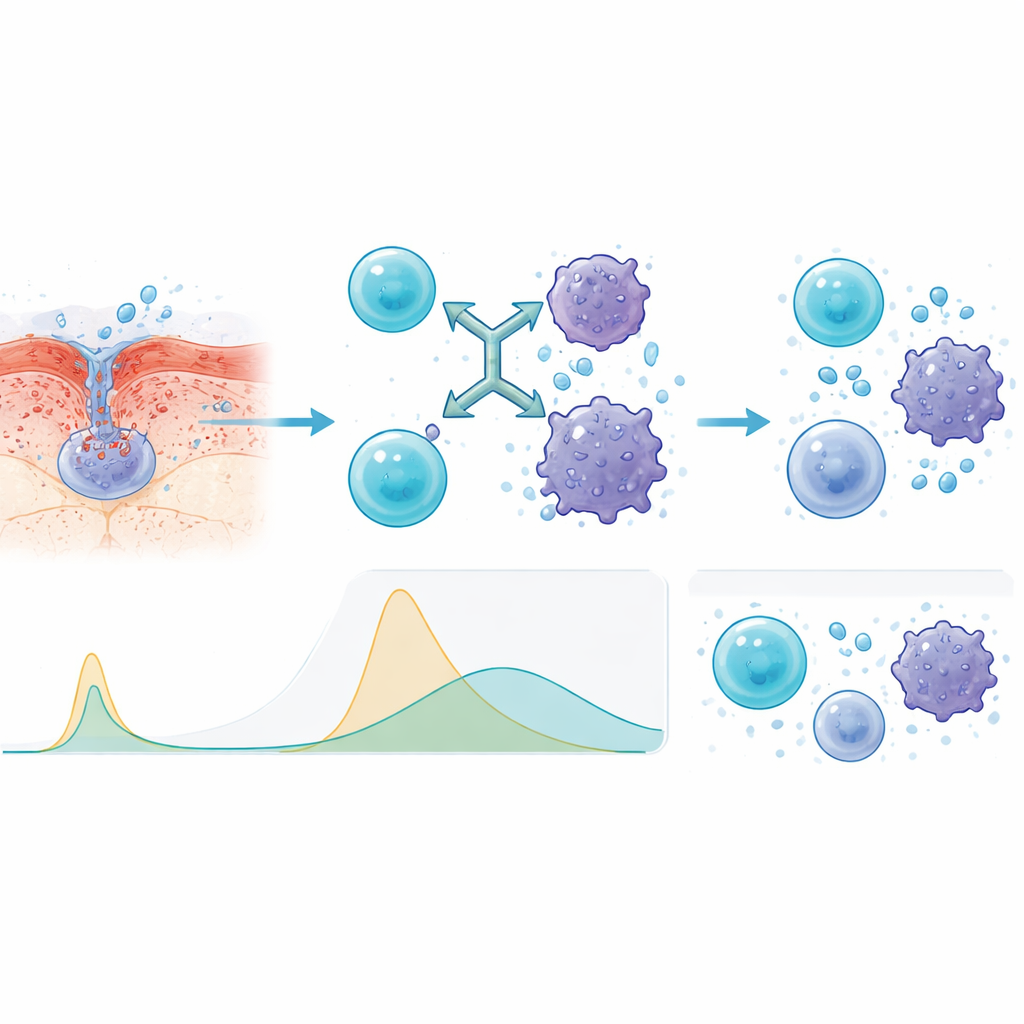
Чтобы понять, почему подкожное введение вело себя лучше, исследователи измеряли в крови сигнальные молекулы иммунного ответа. По сравнению с внутривенной инфузией инъекции вызывали более медленные и более низкие пики ключевых провоспалительных сигналов, таких как интерлейкины и фактор некроза опухоли. Такой более сглаженный профиль означает, что иммунная система остаётся активированной против опухоли, но без того резкого всплеска, который может сделать пациента опасно больным. Кроме того, команда обнаружила, что у пациентов с более низким уровнем циркулирующего «сброшенного» BCMA на старте — признаком менее агрессивного или менее продвинутого заболевания — реакции были лучше, а ремиссии длились дольше.
Что это значит для будущего лечения миеломы
Хотя компания впоследствии решила прекратить разработку алнуктамаба по стратегическим причинам, уроки этого исследования важны. Работа показывает, что грамотно спроектированный иммуноэнгейджер может вводиться простым уколом по схеме, которая со временем становится менее обременительной, при этом обеспечивая глубокие и продолжительные ответы у многих пациентов с трудноизлечимой миеломой. Это также указывает на то, что постепенное наращивание дозы и избегание резких пиков активации иммунитета может ограничивать серьёзные реакции, не снижая противоопухолевой эффективности. Эти выводы, вероятно, помогут при разработке будущих иммунных терапий, давая надежду на то, что у большего числа пациентов с рецидивирующей миеломой появятся эффективные, более безопасные и удобные в применении варианты лечения.
Цитирование: Bar, N., Martin, T., Hofmeister, C.C. et al. Alnuctamab, a bivalent B-cell maturation antigen-targeting T cell engager for patients with relapsed or refractory multiple myeloma: results from a phase 1, first-in-human study. Leukemia 40, 481–490 (2026). https://doi.org/10.1038/s41375-025-02841-x
Ключевые слова: множественная миелома, иммунотерапия, биспецифическое антитело, BCMA, T‑клеточный энгейджер