Clear Sky Science · ru
Гликолитический путь KDM6B/Pdk1, стимулирующий лактиляцию ZEB2, способствует формированию клеточного цемента
Почему важно защищать корни зубов
Заболевание десен, или пародонтит, — одна из ведущих причин потери зубов у взрослых. По мере прогрессирования оно незаметно разъедает ткани, которые фиксируют зубы в челюсти. Одна из самых важных таких структур — цемент, тонкий, напоминающий кость слой, покрывающий корень и обеспечивающий «привязку» зуба к связке и кости. Как только цемент теряется, зубы расшатываются и в конечном счёте могут выпасть. В этом исследовании поставлен простой, но важный вопрос: можно ли понять на молекулярном уровне, как строится цемент, чтобы однажды помочь организму его восстановить и сохранить зубы на всю жизнь?
От клеток, поддерживающих зуб, к терапевтической мишени
Цемент образуется специализированными клетками — цементобластами, которые располагаются на поверхности корня и откладывают новый минерал. Эти клетки во многом похожи на остеобласты, но сигналы, подсказывающие им, когда и как строить цемент, были плохо изучены. Исследователи сосредоточились на молекуле KDM6B — ферменте, который редактирует химические метки на белках, упаковывающих ДНК, и может включать гены. Изучая зубы мышей разных возрастов и цементобласты в культуре, они обнаружили, что уровни KDM6B повышаются в активную фазу формирования цемента и снижаются, когда рост замедляется. При блокировке KDM6B в клетках или у животных активность цементобластов уменьшалась, и «клеточная» часть цемента — более толстая живая область у верхушки корня — истончалась, что указывает на ключевую роль KDM6B в поддержании здорового роста цемента.
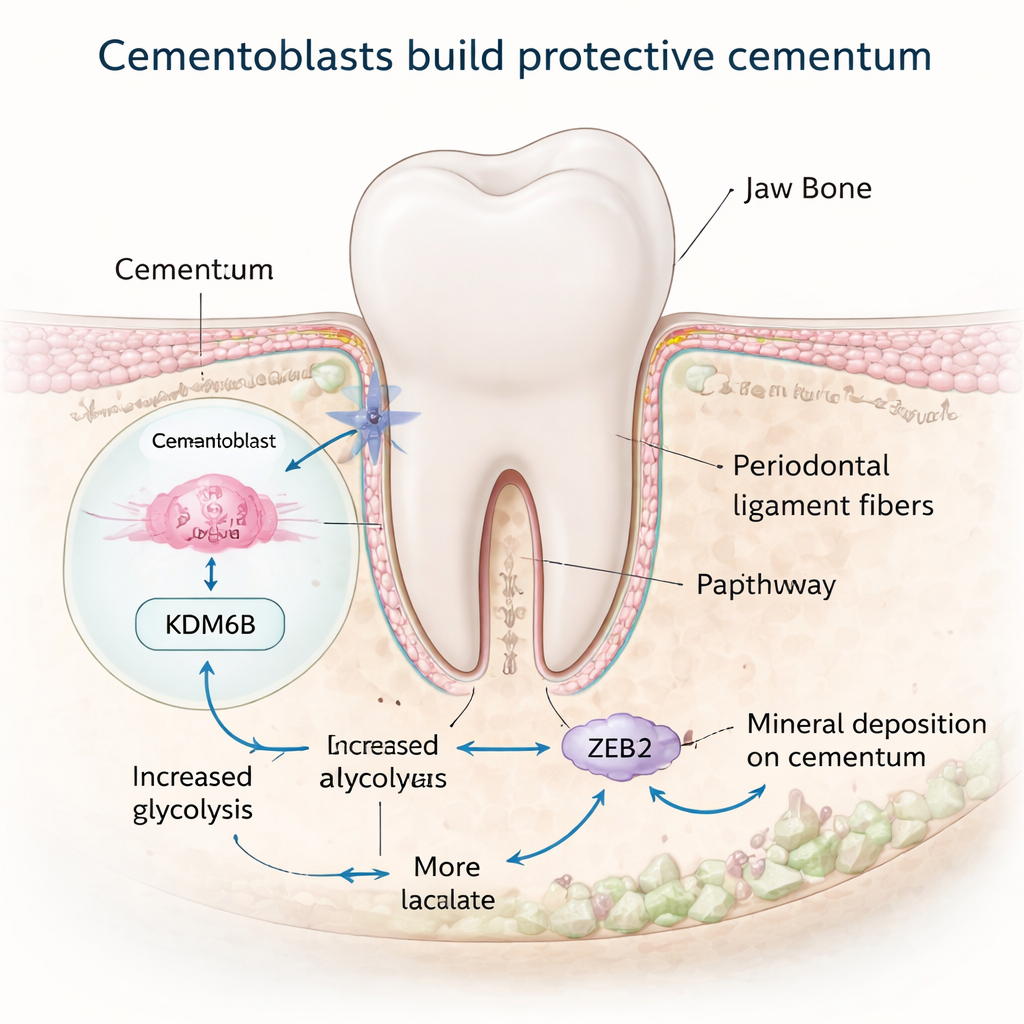
Перенастройка метаболизма клеток для построения минерала
Построение минерализованной ткани требует много энергии, и многие клетки переводят свой обмен веществ в особый высокоактивный режим при выполнении такой работы. Команда обнаружила, что KDM6B помогает цементобластам перенастроить использование сахара. Обычно эти клетки предпочитают путь гликолиза, который быстро расщепляет глюкозу и производит лактат. При снижении KDM6B гены, участвующие в гликолизе, выключались, тогда как те, что связаны с более медленным кислородзависимым энергообеспечением, были смешанными или повышенными, и клетки производили меньше энергии в целом. Центральным игроком в этом переключении оказался фермент PDK1. С помощью картирования генома исследователи показали, что KDM6B физически удаляет репрессирующую метку в области ДНК, контролирующей ген Pdk1, что позволяет уровням PDK1 увеличиваться. Востановление PDK1 в клетках с дефицитом KDM6B возвращало многие маркеры минерализации, выявляя метаболическое переключение KDM6B–PDK1, которое питает цементобласты.
Превращение лактата из отхода в полезный сигнал
Лактат часто считают отходным продуктом интенсивно работающих мышц, но последние исследования показали, что он также может выступать сигналом, модифицирующим белки. В этом исследовании повышенный гликолиз под управлением KDM6B и PDK1 увеличивал продукцию лактата в цементобластах. Затем учёные отслеживали относительно новую модификацию белков — лактиляцию, при которой метки, происходящие от лактата, прикрепляются к определённым участкам белков. Они обнаружили, что уровни лактиляции в цементобластах повышаются в периоды активного формирования цемента и снижаются у старых мышей и в клетках с дефицитом KDM6B. Добавление простого натрия лактата в систему усиливало лактиляцию, возрождало экспрессию генов, связанных с минерализацией, и восстанавливало образование минеральных узелков как в культуре клеток, так и в модели у мышей, даже при блокировке KDM6B. Это указывает на то, что сам лактат способен частично спасать ослабленную цементообразующую активность.
Молекулярный импульс для ключевого регулятора цемента
Затем команда спросила, какие именно белки «украшаются» лактиляцией и имеют значение для цемента. Они сосредоточились на ZEB2 — регуляторе генов, известном своей ролью в продвижении минерализации цементобластов. С помощью методов картирования белков они определили конкретные участки ZEB2, несущие метки лактиляции, и показали, что изменение одного критического сайта ослабляет способность клетки включать гены минерализации. Последующие эксперименты продемонстрировали, что путь KDM6B–PDK1 усиливает лактиляцию ZEB2, и что добавление лишнего лактата может восстановить активность ZEB2 при низком уровне PDK1. По сути, метаболизм и регуляция генов связаны: расщепление сахара питает производство лактата, который затем тонко настраивает ZEB2, поддерживая программы формирования цемента в активном состоянии.
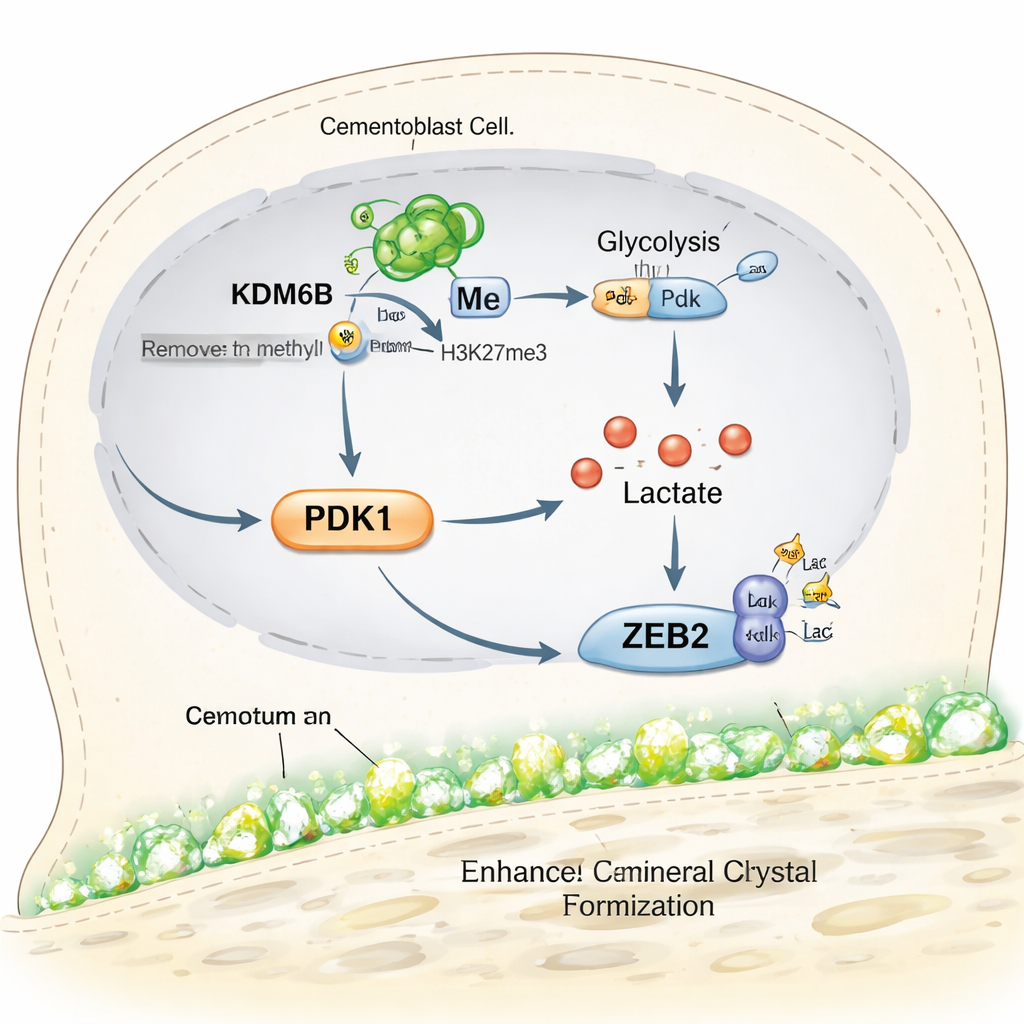
Что это значит для будущих методов сохранения зубов
Проще говоря, исследование выявляет цепочку событий внутри клеток, формирующих цемент: фермент KDM6B открывает ген Pdk1, PDK1 направляет клетки на быстрый путь использования сахара, этот метаболизм генерирует лактат, а лактат химически настраивает белок ZEB2, чтобы стимулировать отложение минерала. Когда любой шаг этой цепи блокируется, рост цемента ослабевает, но внимательное добавление лактата может частично его восстановить. Для пациентов это ещё не клиническое лечение, но работа выделяет новые, точечные мишени для лекарств или биоматериалов, предназначенных для регенерации цемента и стабилизации зубов при тяжёлом заболевании дёсен. Также это предполагает, что аналогичные метаболические «переключатели» можно использовать для стимулирования заживления костей и в других частях тела.
Цитирование: Yang, Z., Wang, H., Xiao, J. et al. KDM6B/Pdk1 glycolytic pathway-driven ZEB2 lactylation promotes cellular cementum formation. Int J Oral Sci 18, 21 (2026). https://doi.org/10.1038/s41368-025-00420-5
Ключевые слова: регенерация цемента, пародонтит, метаболизм цементобластов, гистондеметилаза KDM6B, лактиляция белков