Clear Sky Science · ru
Структурные сведения о мутациях, связанных с заболеваниями, в механизмах обработки микроРНК
Как крошечные РНКовые «ножницы» формируют здоровье и болезнь
Внутри каждой клетки существует скрытая система редактирования, которая подрезает генетические сообщения до того, как они будут прочитаны. Эта система опирается на крошечные фрагменты РНК, называемые микроРНК, которые действуют как регуляторы тонкой настройки для тысяч генов одновременно. Когда молекулярные «машины», создающие микроРНК, работают правильно, клетки растут, делятся и специализируются контролируемым образом. Но когда эти машины повреждаются мутациями, равновесие активности генов может смещаться в сторону рака, заболеваний крови или нарушений развития мозга. В этой статье объясняется, как понимание 3D‑форм этих машин помогает учёным точно определить, что идёт не так, и как это можно исправить.
Инструментарий клетки для «приглушения» генов
МикроРНК — это короткие фрагменты РНК длиной примерно 22 нуклеотида, которые сами по себе не кодируют белки. Вместо этого они присоединяются к более длинным матричным РНК и либо помечают их для разрушения, либо блокируют их трансляцию, фактически понижая активность генов, а не полностью отключая их. Для создания микроРНК клетки пропускают более длинные предшественники РНК через тщательно организованную конвейерную систему. Сначала фермент DROSHA обрезает громоздкие первичные транскрипты в ядре клетки до более коротких фрагментов в виде «шпильки» (hairpin). Эти фрагменты затем перемещаются в цитоплазму, где другой фермент, DICER, отмеряет и разрезает их на диаплексы размеров микроРНК. Наконец, одна цепь каждого диаплекса загружается в белок Argonaute 2 (AGO2), который использует микроРНК как направляющую для поиска совпадающих сообщений и их подавления. 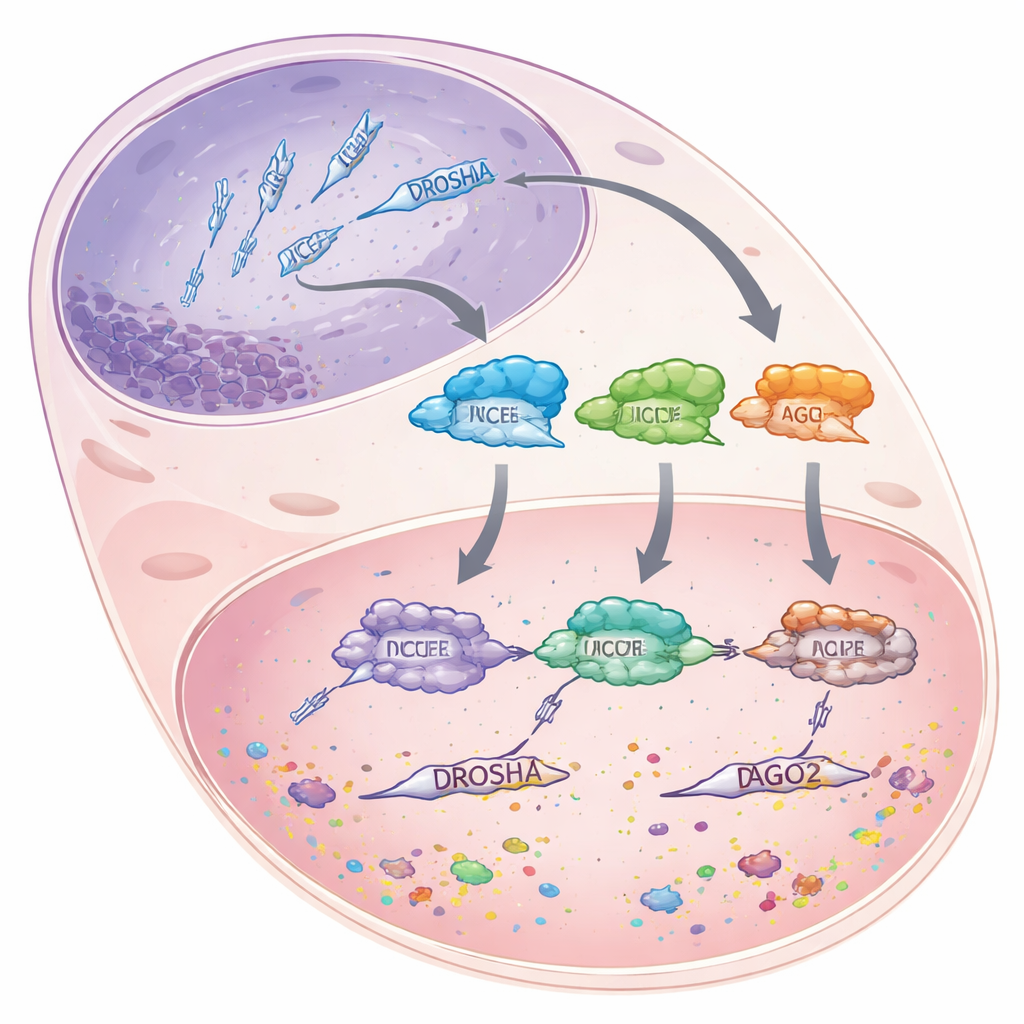
Тонкие формы для точных задач
DROSHA, DICER и AGO2 — это не простые ножницы; каждый из них состоит из нескольких взаимодействующих частей, которые должны двигаться скоординированно. DROSHA работает совместно с белковым партнёром DGCR8, чтобы захватывать концы первичной микроРНК‑шпильки и точно определять место разреза. DICER использует некий встроенный «линейку», сформированную его доменами, чтобы установить фиксированное расстояние между точкой захвата конца шпильки и каталитическим центром, который делает разрез. AGO2 обвивает одну цепь микроРНК так, чтобы её «сид»‑регион был идеально открыт для распознавания целей, в то время как ионы металлов и ключевые аминокислоты в его ядре выстраиваются для разрезания этих мишеней при достаточно сильном паровании. Во всех трёх белках положительно заряженные канавки и гибкие звенья направляют РНК‑цепи на свои места, а сайты связывания металлов и каталитические остатки осуществляют химические разрывы.
Когда ножницы изгибаются или становятся тупыми
Генетические исследования пациентов с раком, заболеваниями крови и нейроразвитием выявили кластеры мутаций в этих машинах обработки микроРНК. Многие из наиболее повреждающих изменений локализуются прямо в каталитических центрах или на плотных РНК‑захватывающих поверхностях. В DROSHA, например, замены аминокислот, такие как E1147K и D1219G, расположены в сердце участка разреза и нарушают способность удерживать необходимые ионы металлов, делая фермент неспособным обрабатывать первичные микроРНК. Другие мутации DROSHA, такие как усечения, удаляющие область разреза, или изменения, дестабилизирующие опорные спирали, ослабляют весь комплекс и вызывают глобальное снижение уровней микроРНК при опухоли Вильмса, нарушениях костного мозга и заболеваниях нервной системы. В DICER повторяющиеся мутации скапливаются в одном из двух его каталитических доменов, искажают производство так, что теряется одна из «рукавов» диаплекса микроРНК, что смещает баланс между сигналами, способствующими росту, и подавляющими его. 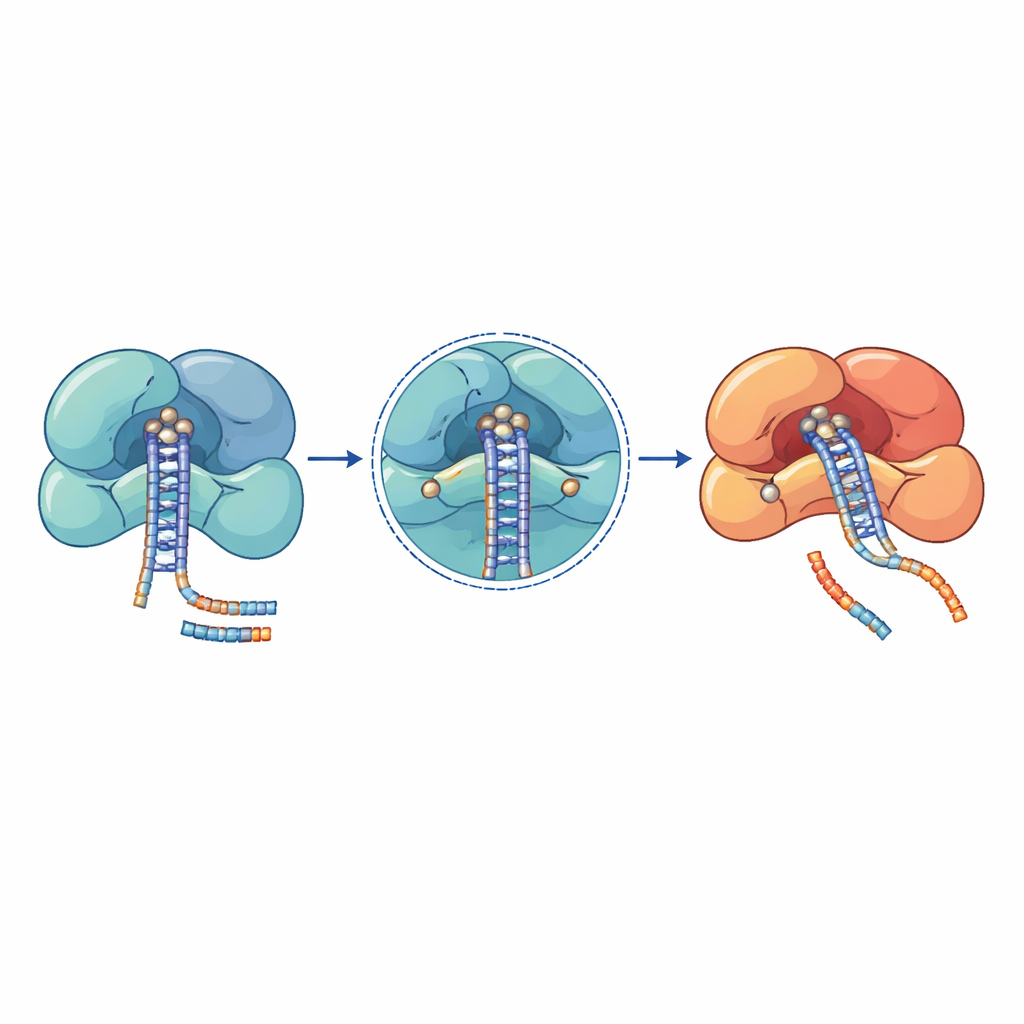
Несовпадающие направляющие в мозге и за его пределами
Мутации AGO2 рассказывают иную, но родственную историю. Прямые удары по его каталитическому ядру редки, вероятно потому, что они были бы летальными на ранних стадиях развития. Вместо этого варианты, связанные с заболеваниями, как правило, появляются в гибких линкерных регионах и на стыках доменов, которые поддерживают форму AGO2. При синдроме Лесселя–Крейенкампа, нейроразвитийном состоянии, мутации в этих линкерах и прилегающих поверхностях тонко изменяют упаковку и движение частей PAZ, MID и PIWI AGO2. Это может неверно выровнять направляющую микроРНК или ослабить её захват за целевые РНК, размывая точность генных подавлений во время развития мозга. Похожие структурные изменения в любой точке пути микроРНК — будь то в DROSHA, DICER или AGO2 — могут распространяться дальше, изменяя целые сети генов, вовлечённых в рост клеток, образование крови или проводку нейронов.
Преобразование структурных подсказок в будущие терапии
Нанесение болезненных мутаций на высокоразрешённые 3D‑карты этих белков позволяет исследователям точно классифицировать, как каждое изменение вызывает проблемы — будь то притупление режущей кромки, ослабление критических контактов с партнёрами или искривление ключевых спиралей. Эти структурные данные открывают путь к целенаправленным вмешательствам: малые молекулы, стабилизирующие ослабленные интерфейсы; разработанные РНК, возвращающие частично функциональные ферменты к правильным субстратам; или аллостерические соединения, подталкивающие мутантные белки к более активным формам. Для непрофессионала главный вывод таков: крошечные структурные правки в «РНК‑ножницах» клетки могут иметь непропорционально большие последствия для здоровья, но они также дают точные «ручки» для разработки новых, учитывающих мутации, терапий.
Цитирование: Lee, H., Lee, J. & Roh, SH. Structural insights into disease-associated mutations in the microRNA processing machinery. Exp Mol Med 58, 639–649 (2026). https://doi.org/10.1038/s12276-026-01669-4
Ключевые слова: микроРНК, РНК-интерференция, DROSHA DICER AGO2, генетика рака, нарушения нейроразвития