Clear Sky Science · ru
Регуляторные механизмы стабильности белка Snail: система убиквитин–протеасома и хаптерон-опосредованная аутофагия
Почему распространение рака зависит от хрупкого белка
Рак становится по-настоящему опасным, когда клетки отрываются от первичной опухоли и распространяются в отдалённые органы. Это распространение, или метастазирование, частично зависит от мощного «мастер-переключателя» — белка Snail, который помогает клеткам ослаблять связи и становиться более подвижными. В этой статье объясняется, как клетки обычно держат Snail на коротком поводке, быстро разрушая его двумя основными системами утилизации. Понимание этого баланса даёт новые идеи для замедления или предотвращения метастазирования.
От плотно сомкнутых клеток к блуждающим захватчикам
В здоровых тканях эпителиальные клетки формируют упорядоченные, как кирпичная кладка, слои, которые остаются на месте и плотно сцеплены с соседями. Чтобы клетке опухоли сбежать, ей часто требуется перестройка, называемая эпителиально-мезенхимальным переходом (ЭМП), при которой она теряет плотные контакты и приобретает способность двигаться и вторгаться. Snail — ключевой драйвер этой перестройки: находясь в ядре клетки, он выключает гены, поддерживающие клеточно-клеточную адгезию, и включает гены, способствующие подвижности и инвазии. Высокие уровни Snail ассоциируются с агрессивными формами рака и неблагоприятным прогнозом пациента, поэтому клетки выработали механизмы, чтобы при нормальных условиях держать Snail в дефиците и короткоживущим.
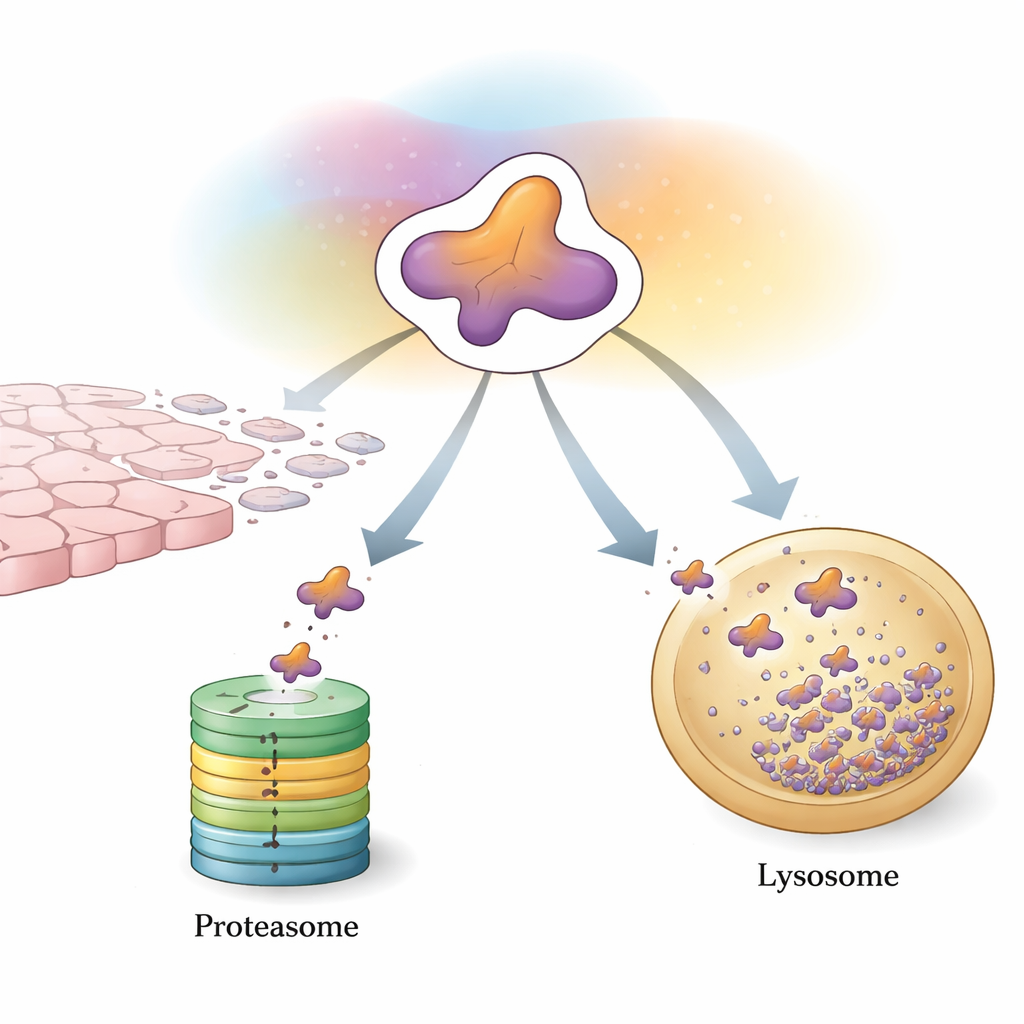
Первая линия контроля клетки: пометь и уничтожь
Один из основных способов контроля Snail — система убиквитин–протеасома, машина «пометить и измельчить» для нежелательных белков. Специализированные ферменты прикрепляют к Snail небольшие «метки» из белка убиквитина. Когда таких меток накапливается достаточно в определённой конфигурации, Snail направляют в протеасому — бочкообразный комплекс, который расщепляет его на фрагменты. Большой ансамбль вспомогательных белков тонко настраивает этот процесс. Некоторые ферменты добавляют цепочки, способствующие деградации, которые быстро отправляют Snail в шредер, помогая сдерживать рост и распространение опухоли. Другие присоединяют цепочки, которые, наоборот, стабилизируют Snail или косвенно повышают его экспрессию, сдвигая равновесие в сторону ЭМП и метастазирования. Химические модификации, такие как фосфорилирование и ацетилирование, работают как дополнительные переключатели, контролируя, какие помощники могут связываться с Snail и будет ли он разрушен или сохранён.
Снятие тормозов: ферменты, которые спасают Snail
История не заканчивается пометкой Snail для уничтожения. Другая группа ферментов, называемых дебиквитиназами, способна снимать убиквитиновые метки, спасая Snail от протеасомы. Многие из этих ферментов активированы или усилены в раковых клетках, что позволяет Snail избежать распада и сохраняться в ядре. Их действия сильно зависят от клеточного контекста: в одних условиях они напрямую стабилизируют Snail, в других — влияют на его локализацию в клетке или на то, как он взаимодействует с партнёрскими белками. Сигналы от путей, связанных с раком, таких как факторы роста и реакции на стресс, питают эту сеть, решая, будет ли Snail быстро удалён или получит возможность запустить программу ЭМП.
Вторая защитная сеть: избирательная доставка в центр переработки клетки
Помимо протеасомы, клетки полагаются на аутофагию — совокупность путей, которые доставляют белки в кислые компартменты, называемые лизосомами, для разрушения. В обзоре особое внимание уделяется высокоспецифичной форме, известной как хаптерон-опосредованная аутофагия (ХОА), как второму важному пути контроля Snail. ХОА распознаёт короткую последовательность в Snail и при помощи «эскортных» белков доставляет цитоплазматический Snail в лизосомы для разрушения. В менее агрессивных клетках рака молочной железы эта система удерживает Snail преимущественно вне ядра и делает его уязвимым для лизосомального удаления. В более агрессивных трижды-негативных раках молочной железы Snail склонен накапливаться в ядре и обходить ХОА, усиливая свою способность запускать ЭМП и метастазирование.
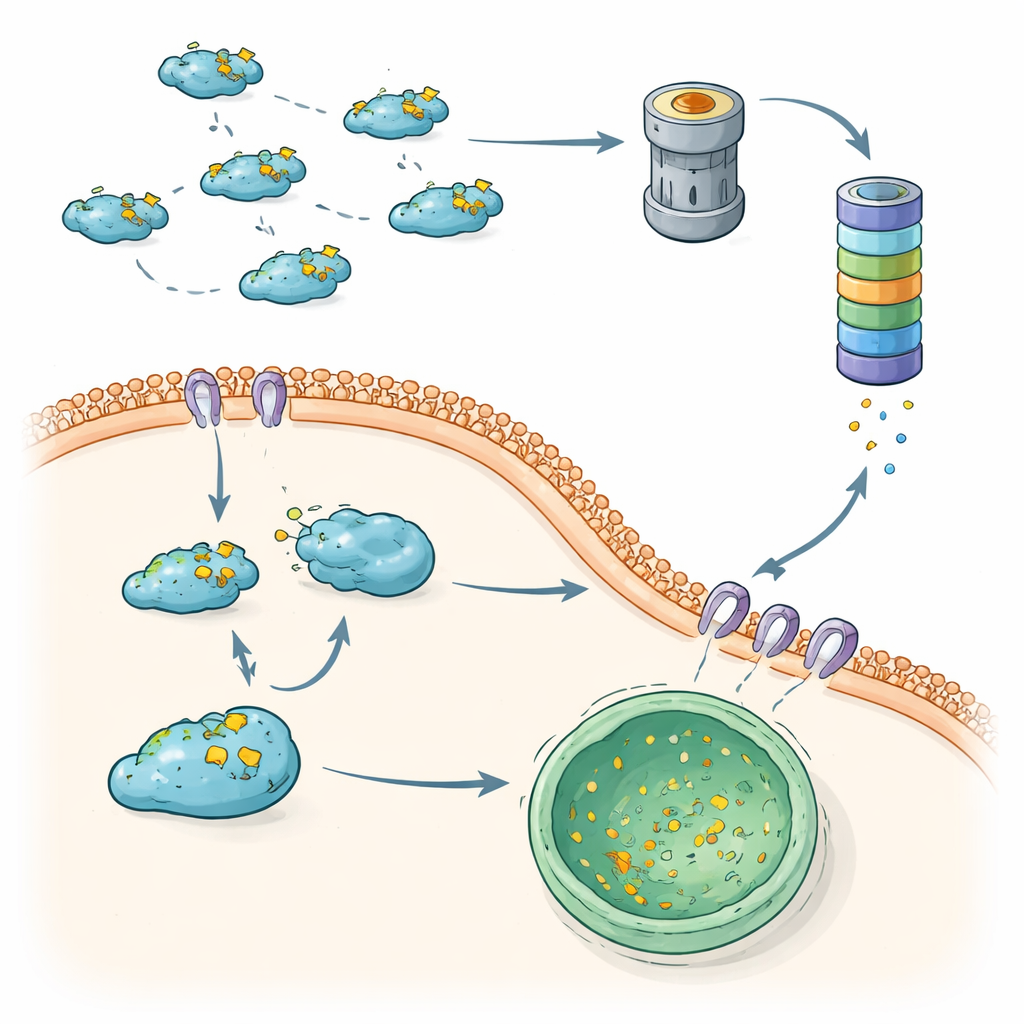
Когда контроль качества даёт сбой, метастазы получают преимущество
В совокупности эти данные показывают, что клетки используют два дополняющих друг друга «контрольно-качественных» звена для сдерживания Snail: путь убиквитин–протеасома и лизосомальная деградация на базе ХОА. Когда оба работают правильно, Snail быстро удаляется, ограничивая ЭМП и помогая предотвращать распространение опухолевых клеток. Когда любое из звеньев ослабевает — из-за изменений в ферментах маркировки, дебиквитиназах или компонентах ХОА — Snail становится более стабильным, накапливается в ядре и сильно стимулирует инвазивное поведение. Сопоставляя эти взаимосвязанные пути разрушения, статья определяет новые терапевтические возможности: препараты, которые восстанавливают или усиливают деградацию Snail, либо перенаправляют Snail обратно на путь ХОА или протеасомальной деградации, могут помочь снова затормозить метастазирование без полного отключения этих жизненно важных систем утилизации белков.
Цитирование: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
Ключевые слова: метастазирование рака, эпителиально-мезенхимальный переход, белок Snail, деградация белков, аутофагия