Clear Sky Science · ru
Зависимая от TRPV1 корнеа–тригеминальная нейровоспалительная цепь способствует корнеальной невропатии
Чувствительные глаза и продолжающаяся боль
Многие люди с сухими, раздражёнными глазами удивляются, узнав, что самые неприятные симптомы вызваны не поверхностью глаза, а нервами, которые ощущают раздражение и боль. Это исследование на мышах раскрывает скрытую петлю обратной связи между глазом и сенсорным центром мозга, что помогает объяснить, почему боль в глазах может сохраняться длительно и почему иногда затрагивает оба глаза, даже если сухость заметна только в одном. Выявив конкретный молекулярный «шлюз» в этой цепи, работа указывает на новые способы уменьшить боль в глазах, не ограничиваясь лишь добавлением слёз.

Когда система тревоги глаза даёт сбой
Прозрачное «окно» глаза, роговица, плотно усеяна нервными окончаниями, которые постоянно контролируют влажность, температуру и химический состав слёз. При заболевании сухого глаза слёзы уменьшаются или становятся слишком солёными, и пациенты часто испытывают жжение, покалывание или даже изнуряющую боль. Авторы сосредоточились на молекулярном сенсоре на болевых волокнах роговицы — TRPV1, известном как рецептор для капсаицина, основного компонента стручкового перца. Этот сенсор реагирует на тепло и на сигналы, выделяющиеся при стрессе тканей. Исследователи спросили, может ли чрезмерная активация TRPV1 из‑за сухости и повреждения вызывать не только локальное раздражение, но и более глубокие изменения в нервах, соединяющих глаз с мозгом.
Нервно‑иммунная цепь, связывающая глаз и мозг
Используя модели мышей с хирургически уменьшенным выделением слёз, исследователи показали, что сухой глаз сильно активирует волокна роговицы, несущие TRPV1. Это, в свою очередь, меняет активность генов и иммунное поведение в тройничном узле (тригеминальном ганглии) — скоплении нервных тел, где располагаются клетки корнеальных сенсорных нейронов. У нормальных мышей сухость вызвала всплеск экспрессии воспалительных и иммуноассоциированных генов в узле и изменила состояние соседних макрофагов — иммунных клеток, обвивающих сенсорные нейроны. Одновременно на поверхности сухой роговицы наблюдалась активация иммунных клеток, уменьшение плотности нервов и аномальная чувствительность: роговица стала менее отзывчивой на механическое прикосновение и на некоторые химические стимулы, но более реактивной на стимуляцию TRPV1, что указывает на сенситизацию именно этого сенсора.
Почему один повреждённый глаз может влиять на второй
Чтобы отделить прямые эффекты сухости от отдалённых сигналов, индуцированных нервами, команда создала «одностороннюю» сухость, удалив слёзную железу только справа. Поразительно, что неповреждённый левый глаз оставался влажным и с сохранённым поверхностным барьером, но со временем развивал лёгкое воспаление и явные признаки дисфункции нервов — истончение глубоких нервных волокон и изменённую чувствительность — повторяя, но с отставанием, изменения на повреждённой стороне. Эти контралатеральные изменения зависели от TRPV1: мыши, генетически лишённые этого сенсора, были защищены в обоих глазах. РнК‑секвенирование тригеминальных ганглиев подтвердило, что односторонняя сухость запускает иммунный и воспалительный профиль и на противоположной стороне, указывая на корнеа–тригеминальную–корнеальную цепь, способную переносить проблемы из одного глаза в другой.
Доказательство, что активация TRPV1 сама по себе вызывает повреждение
Сухость — сложный фактор, активирующий многие пути, поэтому авторы проверили, достаточно ли одной лишь активации TRPV1, чтобы запустить эту цепь. Они местно наносили капсаицин на роговицу одного глаза, стимулируя TRPV1 без высушивания поверхности. Обработанный глаз демонстрировал выраженную дегенерацию роговичных нервов и снижение чувствительности, хотя эпителиальный барьер оставался неповреждённым. Удивительно, что неповреждённый глаз снова показал более мягкую, но измеримую утрату нервных окончаний и изменения чувствительности, подтверждая, что сильная активация TRPV1 в одной роговице достаточно, чтобы вызвать повреждение нервов и функциональные изменения в парном глазу через общий тригеминальный путь. Мыши, лишённые Т‑ и В‑лимфоцитов, изменялись лишь в обработанном глазу, что указывает на то, что для полного двустороннего распространения требуется адаптивный иммунный ответ наряду с активацией нервов.
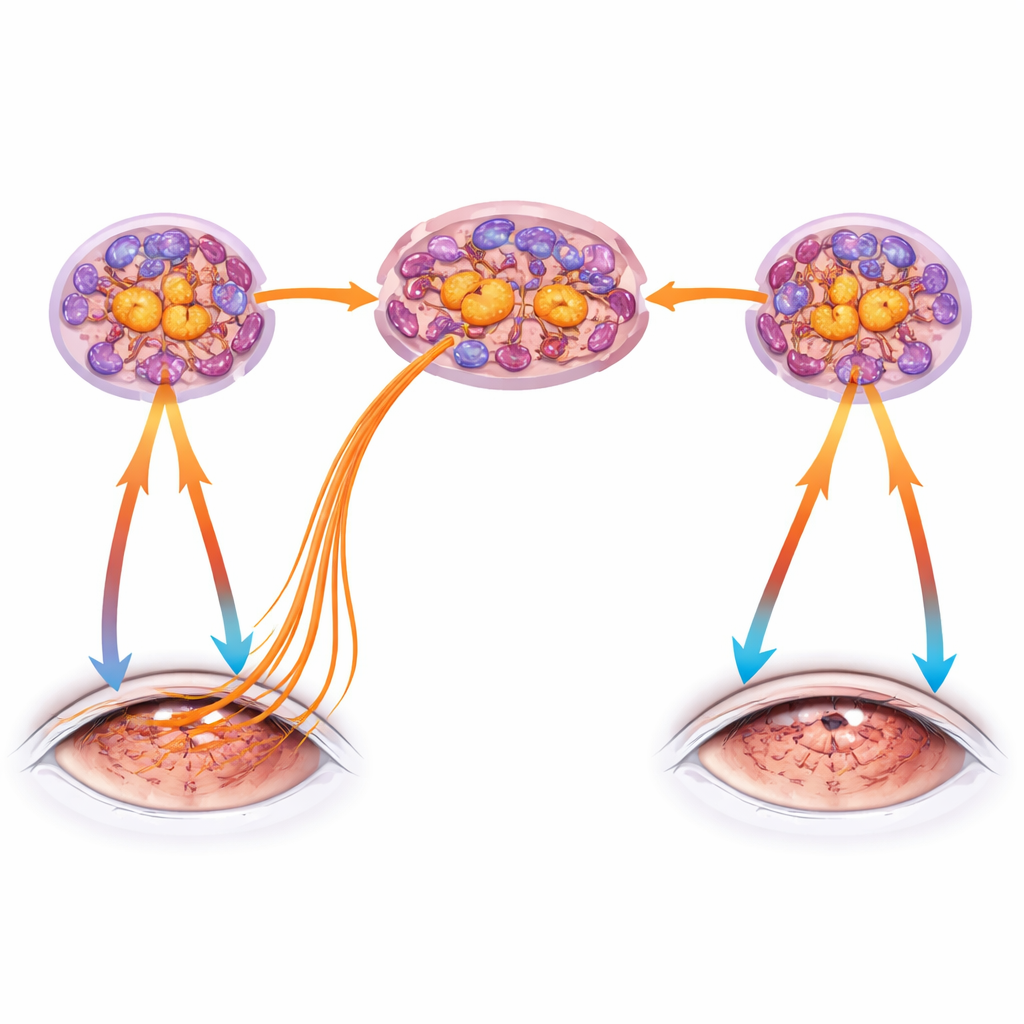
Медиатор, усиливающий боль, и возможный терапевтический подход
В исследовании также изучали субстанцию P, нейропептид, выделяющийся из активированных болевых волокон, который может усиливать воспаление тканей и повышать активность TRPV1. Блокирование рецепторов субстанции P глазными каплями в неповреждённом глазу при односторонней сухости не повредило поверхностному слою роговицы, но существенно ослабило потерю тактильной чувствительности и повышенную реакцию на стимуляцию TRPV1. Однако это не полностью предотвращало структурную утрату нервных окончаний, подчёркивая, что для повреждения роговичных нервов работают несколько сопряжённых факторов. Вместе эти данные описывают порочный круг: сухость и повреждение активируют TRPV1 в роговичных нервах, которые посылают сигналы опасности в тригеминальный ганглий, рекрутируют и перепрограммируют иммунные клетки там, а затем возвращают провоспалительные нервные сигналы и выделение нейропептидов на поверхность глаза, усугубляя дегенерацию нервов и распространяя дисфункцию между глазами.
Что это значит для людей с сухими, болезненными глазами
Для неспециалистов главный вывод таков: синдром сухого глаза — это не просто локальная проблема нехватки слёз. Он включает самоподдерживающуюся нервно‑иммунную петлю, соединяющую поверхность глаза с сенсорными центрами головы и обратно. TRPV1 находится в воротах этой петли, выступая в роли сверхчувствительной тревоги, которая, как только срабатывает, поддерживает воспаление и повреждение нервов, даже если первоначальная сухость была умеренной или односторонней. Терапии, снижающие активность TRPV1 в роговичных нервах или разрушающие downstream‑мессенджеры, такие как субстанция P, могут делать больше, чем просто успокаивать сухую поверхность — они способны разорвать глубинную болевую цепь и защитить сложную сеть нервов, которая поддерживает комфорт и чувствительность наших глаз.
Цитирование: Pizzano, M., Vereertbrugghen, A., Martinez Gomez, M.J. et al. A transient receptor potential vanilloid 1-dependent corneal–trigeminal neuroinflammatory circuit promotes corneal neuropathy. Exp Mol Med 58, 605–621 (2026). https://doi.org/10.1038/s12276-026-01653-y
Ключевые слова: сухой кератоконъюнктивит, роговичные нервы, TRPV1, нейровоспаление, субстанция P