Clear Sky Science · ru
Метаболическое взаимодействие между фибробластами, ассоциированными с раком, адипоцитами и иммунными клетками как фактор иммунодепрессивного микроокружения опухоли
Почему окружение опухоли имеет значение
Рак не развивается в изоляции. Он существует в плотной «соседской» сети поддерживающих клеток, жировых клеток и иммунных клеток, которые постоянно обмениваются питательными веществами и химическими сигналами. В этой статье объясняется, как метаболизм этого окружения — способ, которым клетки используют и делят топливо — незаметно склоняет баланс в пользу опухоли и против иммунной системы. Понимание этой скрытой экономики сахаров, жиров и аминокислот открывает новые пути для повышения эффективности иммунотерапий и для подрыва подпорок опухоли.
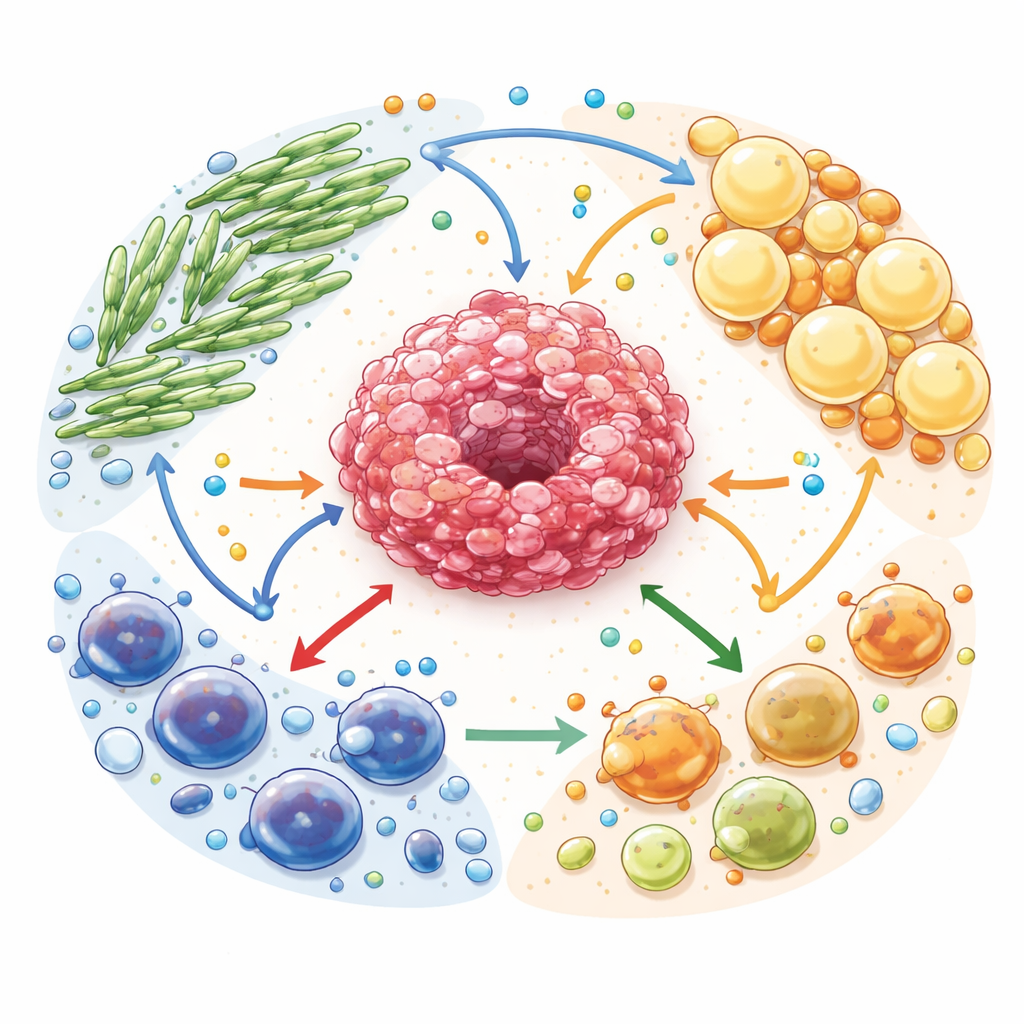
Обмен топливом в экосистеме опухоли
Авторы описывают микроокружение опухоли как сложную экосистему. Раковые клетки окружены фибробластами, ассоциированными с раком (клетками, похожими на рубцовую ткань), адипоцитами, ассоциированными с раком (перепрограммированными жировыми клетками), и множеством типов иммунных клеток. Все эти клетки конкурируют за топливо и обмениваются им — глюкозой, жирными кислотами и аминокислотами. Но этот обмен не нейтрален: поддерживающие клетки перенастраиваются, чтобы расходовать собственные запасы и экспортировать богатые энергией молекулы, питающие раковые клетки. Одновременно накапливаются продукты вроде лактата и аденозина, которые действуют как сильные сигналы, ослабляющие защитные иммунные клетки и благоприятствующие тем, кто подавляет иммунную атаку.
Как жировые клетки помогают опухолям и мешают защите
Ближайшие жировые депо выполняют гораздо больше функций, чем просто хранение калорий. Под влиянием опухолевых сигналов и гипоксии обычные жировые клетки превращаются в адипоциты, ассоциированные с раком. Они уменьшают свои жировые капли, усиливают липолиз и выбрасывают свободные жирные кислоты, провоспалительные молекулы и микровезикулы с грузом биоактивных веществ. Раковые клетки активно поглощают эти липиды и окисляют их в митохондриях, получая гибкий, длительный источник энергии, который помогает выживать при стрессе, распространяться и сопротивляться лечению. Иммунные клетки в районах с высоким содержанием жира оказываются в худшем положении: цитотоксические Т‑клетки и натуральные киллеры перегружаются липидами, испытывают оксидативный стресс и переходят в «истощённое» состояние с ослабленной способностью уничтожать опухолевые клетки. Напротив, регуляторные Т‑клетки и некоторые миелоидные клетки приспособлены к таким липидным условиям, становятся более супрессивными и дополнительно приглушают иммунный ответ.
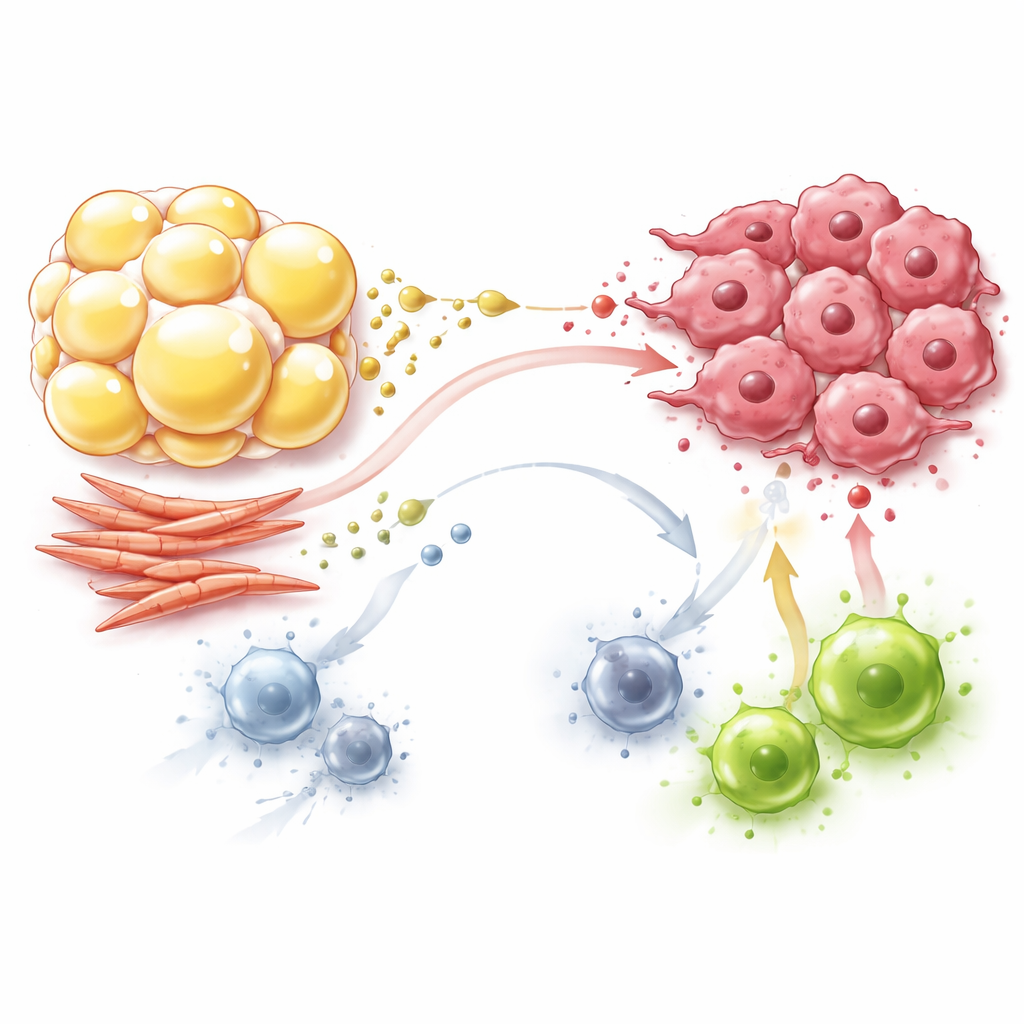
Фибробласты: строители, которые также перенастраивают метаболизм
Фибробласты, давно известные как строители рубцовой ткани вокруг опухолей, также активно участвуют в этой метаболической драме. Фибробласты, ассоциированные с раком, смещаются в сторону повышенного потребления сахаров, превращая большие количества глюкозы в лактат и пируват даже при наличии кислорода. Они экспортируют эти продукты в окружение, где раковые клетки используют их как топливо для своих энергетических центров, экономя глюкозу на рост. Фибробласты также синтезируют и обмениваются аминокислотами, такими как глутамин, пролин и аспарагин, которые поддерживают как структуру опухоли, так и её рост при нехватке питательных веществ. Одновременно фибробласты потребляют ключевые нутриенты и выделяют лактат, вытесняя эффекторные Т‑клетки, зависящие от глюкозы, и сдвигая макрофаги и Т‑клетки в более терпимое, менее агрессивное состояние.
Иммунные клетки, попавшие в метаболическую ловушку
Иммунная система внутри опухолей формируется не только антигенами, но и доступностью топлива. Цитотоксические Т‑клетки и натуральные киллеры, которым нужно быстрое сжигание сахаров для питания атаки, оказываются в пространстве, лишённом глюкозы и залитом лактатом, липидами и другими супрессивными метаболитами. Их «двигатели» застревают, митохондрии повреждаются, а на поверхности усиливаются ингибирующие «тормоза». Между тем регуляторные Т‑клетки и опухолеассоциированные макрофаги лучше приспособлены к такому суровому окружению: они предпочитают окисление липидов и окислительный метаболизм, что позволяет им процветать там, где другие терпят неудачу. Поддерживаемые фибробластами и адипоцитами, эти клетки укрепляют терпимое, похожее на заживление ран состояние, которое защищает опухоль и снижает эффективность ингибиторов чекпойнтов и других иммунотерапий.
Превращение метаболизма в терапевтическую мишень
Обзор описывает растущий набор экспериментальных препаратов, направленных на разрушение этой сети поддержки без простой интоксикации делящихся клеток. Некоторые подходы стремятся блокировать высвобождение жира из адипоцитов или поглощение и окисление липидов в раковых клетках. Другие нацелены на пути, направляемые фибробластами, которые генерируют лактат, ремоделируют внеклеточный матрикс или привлекают супрессивные миелоидные клетки. Снижая уровни лактата, блокируя конкретные транспортеры топлива или перепрограммируя сигнальные липидные переключатели внутри клеток, эти стратегии пытаются восстановить доступ к глюкозе и здоровье митохондрий в истощённых Т‑ и натуральных киллер‑клетках. Конечная цель — не только голодать опухоль, но и «перевоспитать» её окружение так, чтобы иммунные клетки снова могли видеть, достигать и эффективно атаковать раковые клетки.
Цитирование: Kim, T.H., Lim, S.H., Lee, H. et al. Metabolic crosstalk among cancer-associated fibroblasts, adipocytes and immune cells as an immunosuppressive tumor microenvironment driver. Exp Mol Med 58, 366–381 (2026). https://doi.org/10.1038/s12276-026-01650-1
Ключевые слова: микроокружение опухоли, метаболизм рака, фибробласты, ассоциированные с раком, адипоциты, ассоциированные с раком, иммунная супрессия опухоли