Clear Sky Science · ru
Суплементация L-аспартатом корректирует MASLD и MASH у мышей, ингибируя фрагментацию митохондрий, опосредованную взаимодействием тромбоцитов и гепатоцитов, через ось ATP–P2X7–NEK7–DRP1
Почему это исследование печени важно
У многих людей в печени откладывается лишний жир, и они об этом не знают. Эта бесшумная проблема, ныне называемая метаболически ассоциированной стеатотической болезнью печени (MASLD), может прогрессировать до выраженного воспаления, фиброза и даже рака печени. В статье, суммируемой здесь, исследуют, может ли простая естественная аминокислота L-аспартат защищать печень у мышей, и выявляют неожиданный виновник повреждения печени: гиперактивные тромбоциты, которые повреждают «энергетические станции» клеток печени — митохондрии.
Распространённая проблема печени в современной жизни
MASLD тесно связана с ожирением и сахарным диабетом 2 типа и вскоре может затронуть более трети населения Земли. При MASLD клетки печени наполняются жиром, испытывают стресс и начинают умирать, что запускает воспаление и образование рубцовой ткани. В норме здоровые митохондрии сжигают жиры и сахара для получения энергии, но при этом заболевании они повреждаются и фрагментируются, из‑за чего печень хуже утилизирует жиры и они накапливаются. Несмотря на масштаб проблемы, одобрен лишь один препарат, помогающий лишь части пациентов, поэтому учёные ищут безопасные и доступные средства, восстанавливающие энергетическую работу печени.
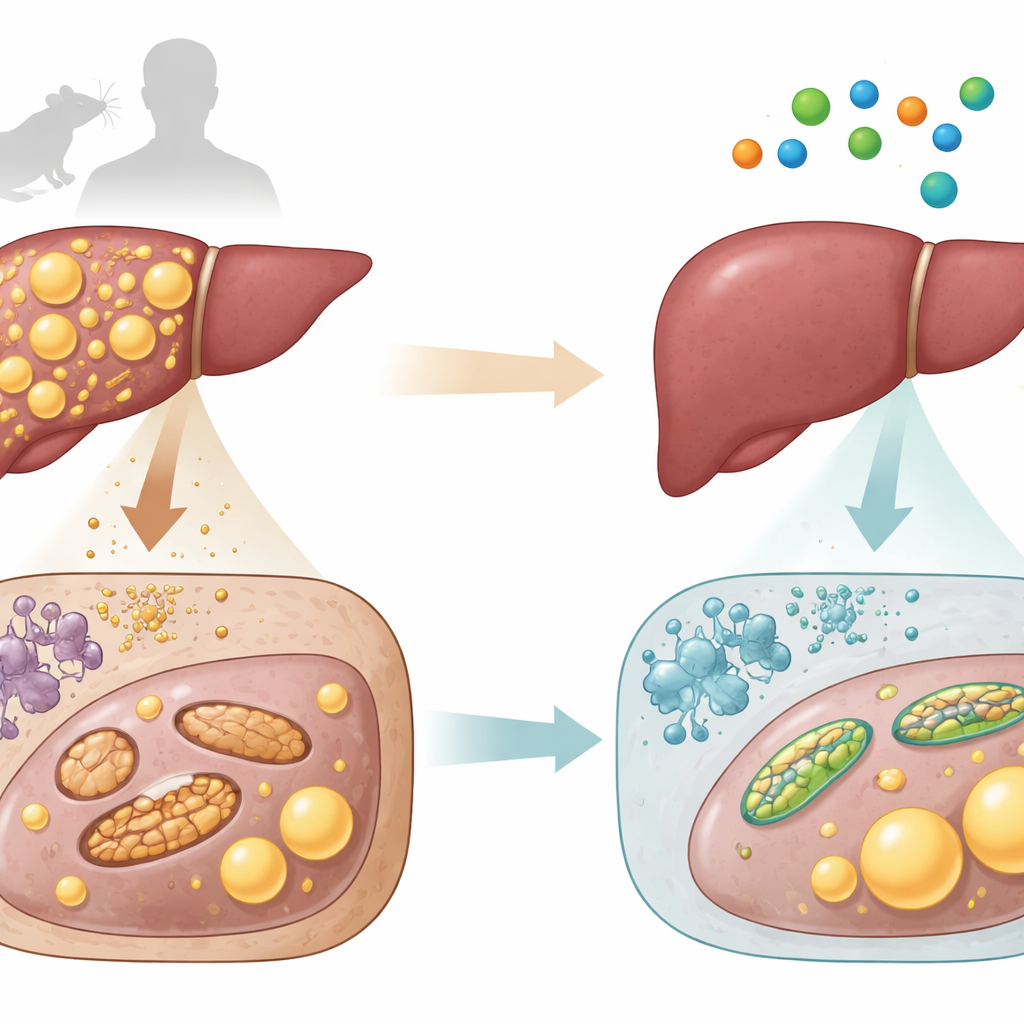
Простая аминокислота как потенциальный помощник
L-аспартат — небольшая структурная единица белков, которая также участвует в энергетических циклах организма и уже используется в клинической практике как поддерживающее печень соединение. Исследователи сначала измерили уровни L-аспартата в крови и образцах печени у мышей и у людей. Они обнаружили, что у животных и пациентов с более жирной и повреждённой печенью концентрации L-аспартата в ткани печени стабильно ниже. В обеих видах чем меньше было L-аспартата, тем выше было содержание жира и интенсивнее маркеры повреждения печени. Этот паттерн указывал на то, что снижение L-аспартата может сопровождаться ухудшением состояния печени.
Обратимое жировое перерождение и воспаление у мышей
Затем команда проверила, может ли восстановление L-аспартата действительно лечить болезнь. Мышей кормили диетой с высоким содержанием жиров и холестерина или специальной диетой, вызывающей выраженное воспаление и фиброз печени, имитируя человеческие MASLD и её продвинутую форму MASH. Когда этим мышам вводили L-аспартат в дозах, сопоставимых с клиническими, их печень становилась легче и менее жирной, уровни печёночных ферментов в крови снижались, а при микроскопии наблюдали меньше жировых капель, меньше воспаления и уменьшенный фиброз. Эти преимущества проявлялись как на ранних стадиях стеатоза, так и при продвинутом воспалительном заболевании и были сопоставимы с эффектами эталонных препаратов в тех же моделях.
Защита «энергетических станций» клетки
При изучении печени исследователи заметили, что у больных мышей митохондрий становилось меньше, многие из них были увеличены и повреждены или раздроблены на мелкие фрагменты. Лечение L-аспартатом восстанавливало более здоровую сеть удлинённых митохондрий. Оно усиливало активность ключевых ферментных комплексов, производящих энергию, увеличивало потребление кислорода митохондриями и выработку АТФ, а также повышало маркеры аутофагии и обновления митохондрий. Измерения у целых животных показали повышенное потребление кислорода и энергорасход, что указывает на то, что мыши сжигали больше топлива в целом, а не просто меньше ели.
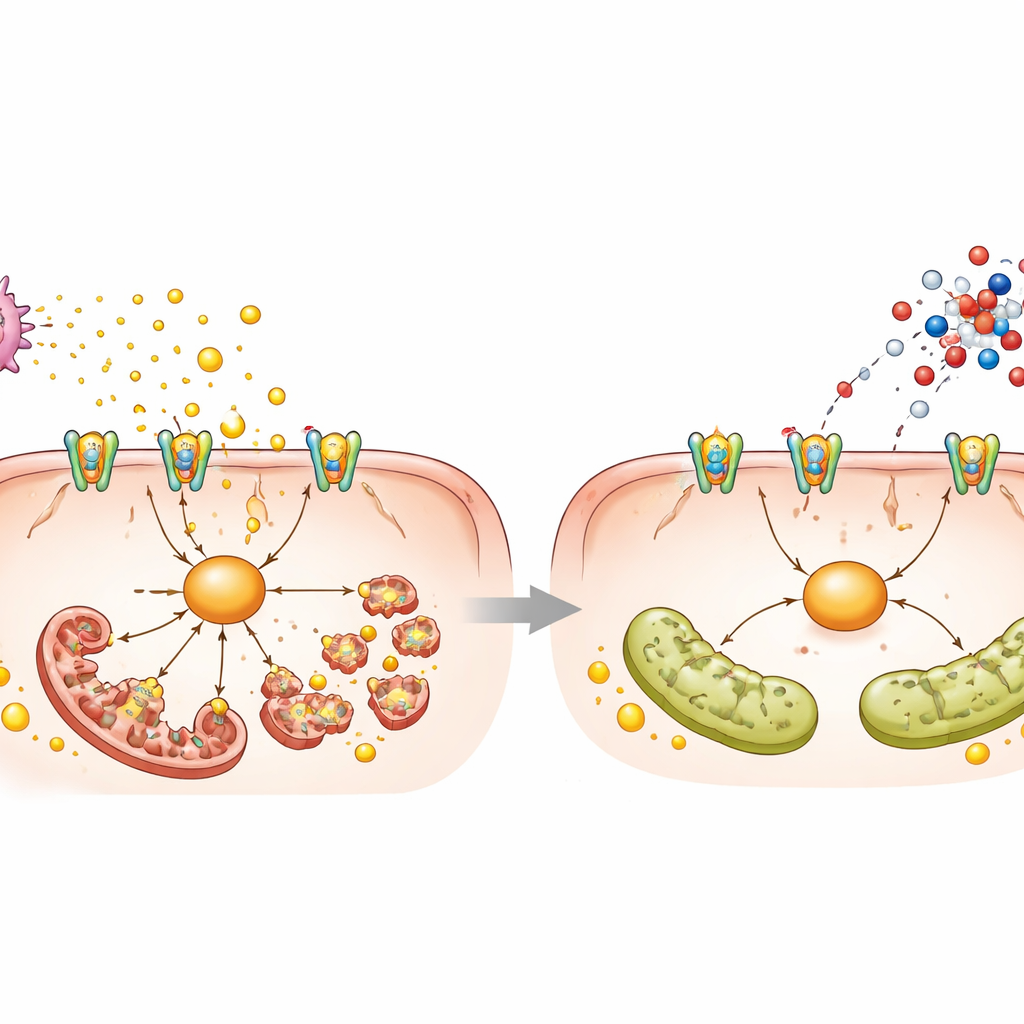
Тромбоциты, токсический сигнал и молекулярная цепочка
Чтобы понять, как действует L-аспартат, исследователи объединили анализ экспрессии генов и метаболитный профиль после одной дозы. Всплыл неожиданный сигнал: пути, связанные с активацией тромбоцитов, и сигнальная молекула cGMP. При жировой болезни печень и кровь содержали больше активированных тромбоцитов, которые выделяли дополнительный АТФ — обычную молекулу энергии, становящуюся вредной при выбросе во внеклеточную среду. Этот АТФ активировал рецептор P2X7 на гепатоцитах, что в свою очередь включало белок NEK7 и белок деления DRP1, приводя к фрагментации митохондрий и способствуя накоплению жира и гибели клеток. L-аспартат повышал уровень cGMP внутри тромбоцитов, снижал их активацию и агрегацию, уменьшал выброс АТФ и успокаивал цепь P2X7–NEK7–DRP1 в клетках печени. Прямое блокирование тромбоцитов аспирином, ингибирование P2X7 или угнетение NEK7 воспроизводило многие защитные эффекты L-аспартата, поддерживая идею, что перекрёстная связь тромбоцитов и печени является центральной для повреждения.
Что это может значить для пациентов
В совокупности эти результаты указывают на то, что при жировой болезни печени гиперактивные тромбоциты засыпают печень АТФ, что запускает молекулярную каскаду, разрушающую митохондрии и усугубляющую накопление жира и повреждение. У мышей добавление L-аспартата разрывает этот цикл: оно делает тромбоциты спокойнее, ограничивает выброс АТФ, сохраняет форму и функцию митохондрий и обращает как простой стеатоз, так и воспалительное фиброзное заболевание. Поскольку L-аспартат недорог и уже применяется как печёночный поддерживающий агент, работа выделяет его как перспективного кандидата для клинических испытаний при MASLD и MASH, а также указывает на тромбоцитарно-опосредованное митохондриальное повреждение как новую мишень для будущих терапий.
Цитирование: Cao, WJ., Su, R., Fu, HL. et al. Supplementation of L-aspartate corrects MASLD and MASH in mice by inhibiting platelet–hepatocyte interaction-mediated mitochondrial fragmentation via the ATP–P2X7–NEK7–DRP1 axis. Exp Mol Med 58, 533–547 (2026). https://doi.org/10.1038/s12276-026-01648-9
Ключевые слова: жировая болезнь печени, тромбоциты, митохондрии, L-аспартат, метаболическое заболевание печени