Clear Sky Science · ru
PAK4 при метаболических заболеваниях: регуляция сигналами о питании и терапевтические перспективы
Почему переключатель в клетке важен для повседневного здоровья
Ожирение, диабет 2 типа и жировая болезнь печени часто сводят к избытку калорий, но глубоко внутри клеток молекулярные переключатели решают, сжигать ли топливо или запасать его. В этом обзоре рассматривается один такой переключатель — белок PAK4 — и объясняется, как он реагирует на изменения сигналов от питательных веществ и гормонов, перестраивая обмен веществ в жировой ткани, печени и мышцах. Понимание этой скрытой системы контроля может открыть путь к новым методам лечения, которые борются с несколькими метаболическими заболеваниями одновременно, а не с одной лишь симптоматикой. 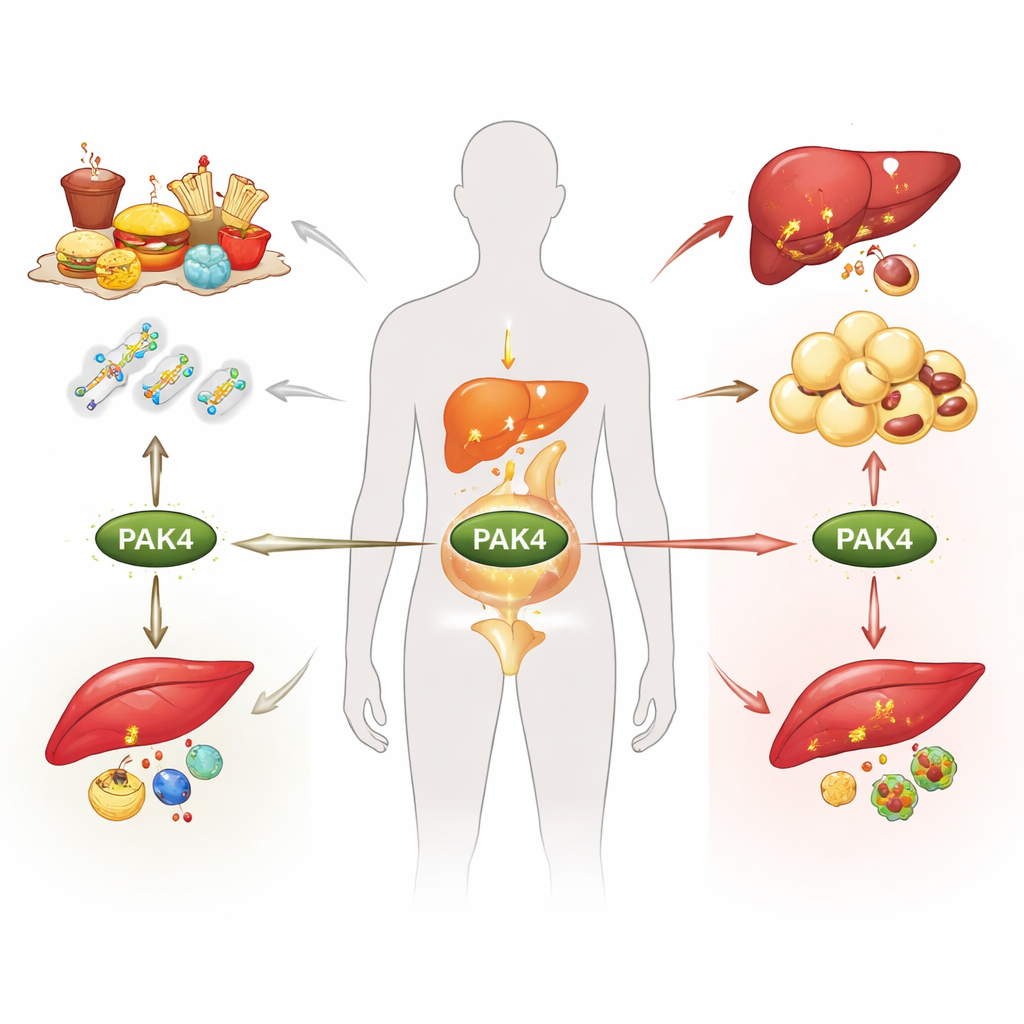
Главный переключатель, скрытый в наших клетках
PAK4 относится к семейству ферментов, передающих сигналы от небольших молекулярных «посланцев» внутри клетки. В норме PAK4 присутствует в небольших количествах в основных метаболических органах. Когда энергетический баланс нарушается, как при ожирении или диабете 2 типа, его уровень повышается в жировой ткани, печени и скелетных мышцах. Активность PAK4 регулируется несколькими способами: через верхушечные сигналы, меняющие его конформацию, и посредством химических меток, добавляемых или удаляемых после синтеза белка. Среди них — фосфатные метки, которые могут либо активировать PAK4, либо помечать его для разрушения, а также другие модификации, влияющие на стабильность и активность белка. Голод, приём пищи, гормоны и стресс влияют на эти метки, поэтому PAK4 фактически «ощущает» нутритивное состояние организма и передаёт эту информацию ключевым метаболическим путям.
Как PAK4 склоняет жировые клетки к накоплению
В жировых клетках PAK4 действует как тормоз для сжигания жира. Обычно при голодании или повышении уровня гормонов стресса другой фермент, называемый PKA, запускает контролируемый распад запасённого жира в маленьких каплях. В обзоре описано, как PAK4 противодействует этому процессу, добавляя ингибирующие фосфатные метки непосредственно на гормонозависимую липазу и на белок, связывающий жирные кислоты, который помогает транспортировать молекулы жира. Эти изменения ослабляют механизм высвобождения жира из запасов. PAK4 также способствует формированию новых жировых клеток на ранних стадиях жизни, помогая белкам клеточного цикла направлять предшественники в зрелые клетки, запасающие жир. Удаление или блокада PAK4 в модельных животных приводит к тому, что жировые клетки сжигают больше топлива, демонстрируют черты «побеления» (browning) с повышенным расходом энергии, и животные получают защиту от набор веса при вредной диете. 
Роль PAK4 в жировой болезни печени и обработке сахара в мышцах
В печени PAK4 снова склоняет баланс в пользу накопления, а не сжигания. Во время голодания или на кето-диете уровни PAK4 падают, что позволяет клеткам печени усиливать распад жира и производство кетонов, которые снабжают энергией другие ткани и даже могут замедлять рост опухолей. Когда PAK4 избыточно, он добавляет фосфатные метки на ядерный корепрессор, который затем подавляет PPARα — главный регулятор β-окисления жирных кислот и образования кетонов. В результате в печени накапливается больше жира, а в крови становится меньше защитных кетонов. В скелетных мышцах PAK4 мешает работе AMPK — центрального энергетического сенсора, который стимулирует как поглощение глюкозы, так и митохондриальную активность. Путём модификации AMPK, блокирующей его активацию, PAK4 снижает количество транспортёров глюкозы на поверхности мышечной клетки и способствует развитию инсулинорезистентности. Специфическое удаление PAK4 в мышцах у мышей обращает эти эффекты, улучшая контроль уровня сахара в крови даже при ожирении.
Стресс, защитные механизмы и связь с другими клеточными переключателями
Обзор также подчёркивает влияние PAK4 за пределами повседневного метаболизма. Во время эпизодов сниженного кровотока и последующей реперфузии в органах, таких как печень, PAK4 ослабляет антиоксидантные защиты, помечая и делая нестабильным Nrf2 — ключевой защитный фактор против окислительного стресса. В то же время другой член семейства, PAK1, часто выполняет более поддерживающие роли в сердечной и скелетной мышце, а также в инсулин-секретирующих клетках поджелудочной железы, помогая поддерживать нормальную регуляцию глюкозы. Этот контраст между вредными сигналами PAK4 при метаболических заболеваниях и обычно полезными действиями PAK1 подчёркивает необходимость в высокоизбирательных препаратах, которые подавляют PAK4, не нарушая функции родственных белков, важных для сердца и эндокринной системы.
От открытия к лечению
Поскольку PAK4 гиперактивен при раке и метаболических расстройствах, разработчики лекарств искали малые молекулы, блокирующие его активность, а также новые «деградирующие» препараты, помечающие сам PAK4 для удаления. Ранние соединения-блокаторы PAK4 показали противоопухолевый потенциал, но столкнулись с проблемами специфичности и фармакокинетики. Более поздние молекулы, точнее нацеленные на PAK4, дали впечатляющие результаты у ожиревших мышей: снижение массы тела без уменьшения потребления пищи, улучшение состояния печени, более активные мышцы и лучший контроль уровня глюкозы. Деградирующие препараты идут дальше, физически устраняя PAK4, и ранние исследования на животных указывают, что они могут защищать от потери мышечной массы и некоторых видов рака. В совокупности эти данные поддерживают идею, что снижение активности PAK4 может одновременно смягчать ожирение, диабет и жировую болезнь печени, превращая когда-то малоизвестный клеточный переключатель в перспективную мишень для будущих метаболических терапий.
Цитирование: Bang, I.H., Park, BH. & Bae, E.J. PAK4 in metabolic diseases: regulation by nutrient signals and therapeutic implications. Exp Mol Med 58, 416–424 (2026). https://doi.org/10.1038/s12276-026-01645-y
Ключевые слова: PAK4, метаболическое заболевание, ожирение, жировая болезнь печени, инсулинорезистентность