Clear Sky Science · ru
Окислительно-чувствительный белок HMGB1: внутриклеточные и внеклеточные роли
Почему изменчивая форма белка важна для здоровья
Практически в каждой клетке вашего организма находится небольшой белок HMGB1, который ведёт себя как многофункциональный инструмент. В спокойных условиях он тихо помогает упорядочивать ДНК. Но когда клетки испытывают стресс или повреждаются, HMGB1 может покинуть ядро, попасть в окружающую ткань и выступить в роли сигнала тревоги для иммунной системы. В этом обзорном материале объясняется, как крошечные химические изменения, вызванные окислением, превращают HMGB1 в очень разные биологические «личности» — такие, что могут защищать ткани, запускать воспаление или способствовать хроническим заболеваниям. Понимание этой молекулярной «фазовой индикации» может открыть новые пути для успокоения чрезмерного воспаления без полного подавления иммунитета.
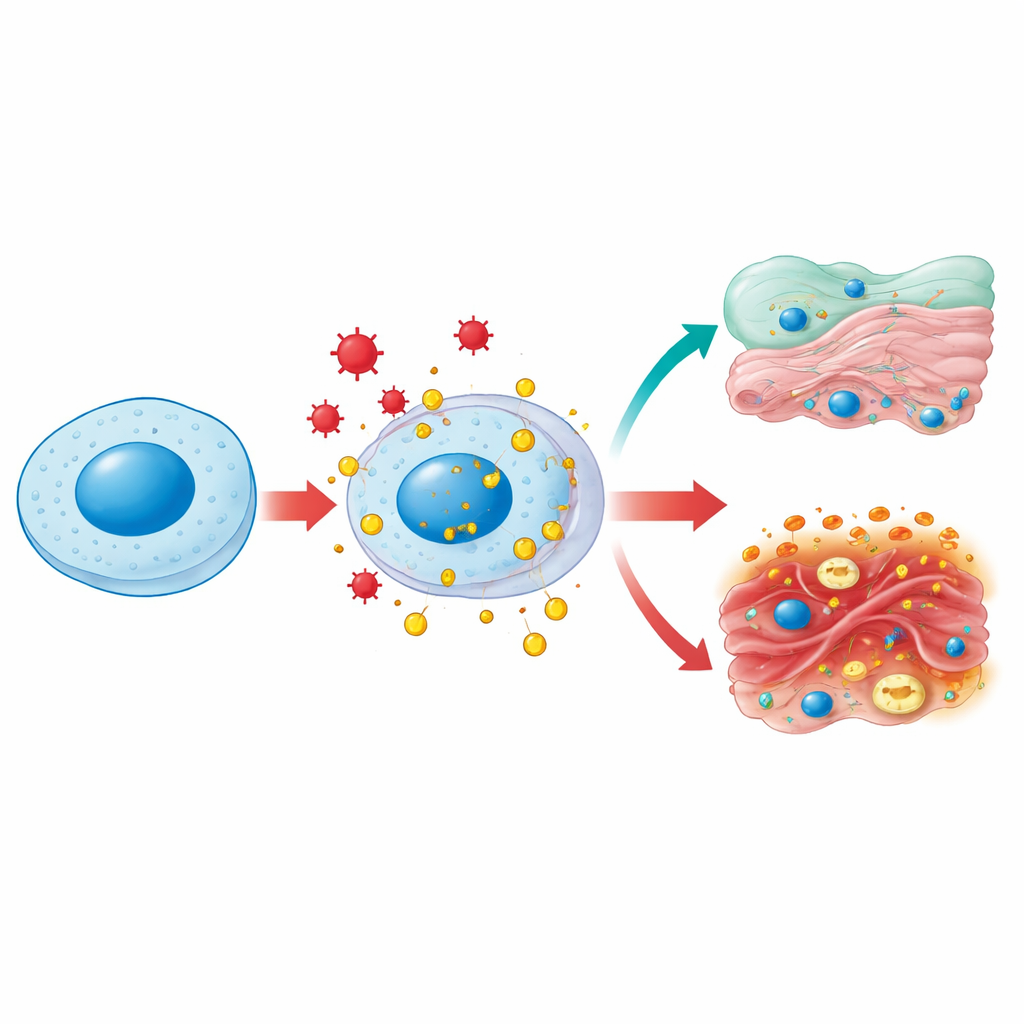
Один белок — много локаций
В норме HMGB1 обитает в клеточном ядре, где он изгибает и разрыхляет ДНК, чтобы гены могли копироваться и восстанавливаться. При стрессе — например, при инфекции, высоком уровне сахара в крови или токсическом повреждении — он может подвергаться химическим модификациям и выводиться в цитоплазму, а затем во внеклеточное пространство. В цитоплазме HMGB1 помогает сохранять здоровье митохондрий, «энергетических станций» клетки, стимулируя аутофагию и предотвращая чрезмерную фрагментацию этих органелл. Попав наружу, HMGB1 превращается в классический «сигнал опасности»: иммунные клетки распознают его как признак повреждения тканей и устремляются к очагу. Таким образом, одна и та же молекула выполняет функции «уборщика» внутри клетки и сигнала тревоги снаружи — в зависимости от места локализации и её химической модификации.
Как окисление переписывает её поведение
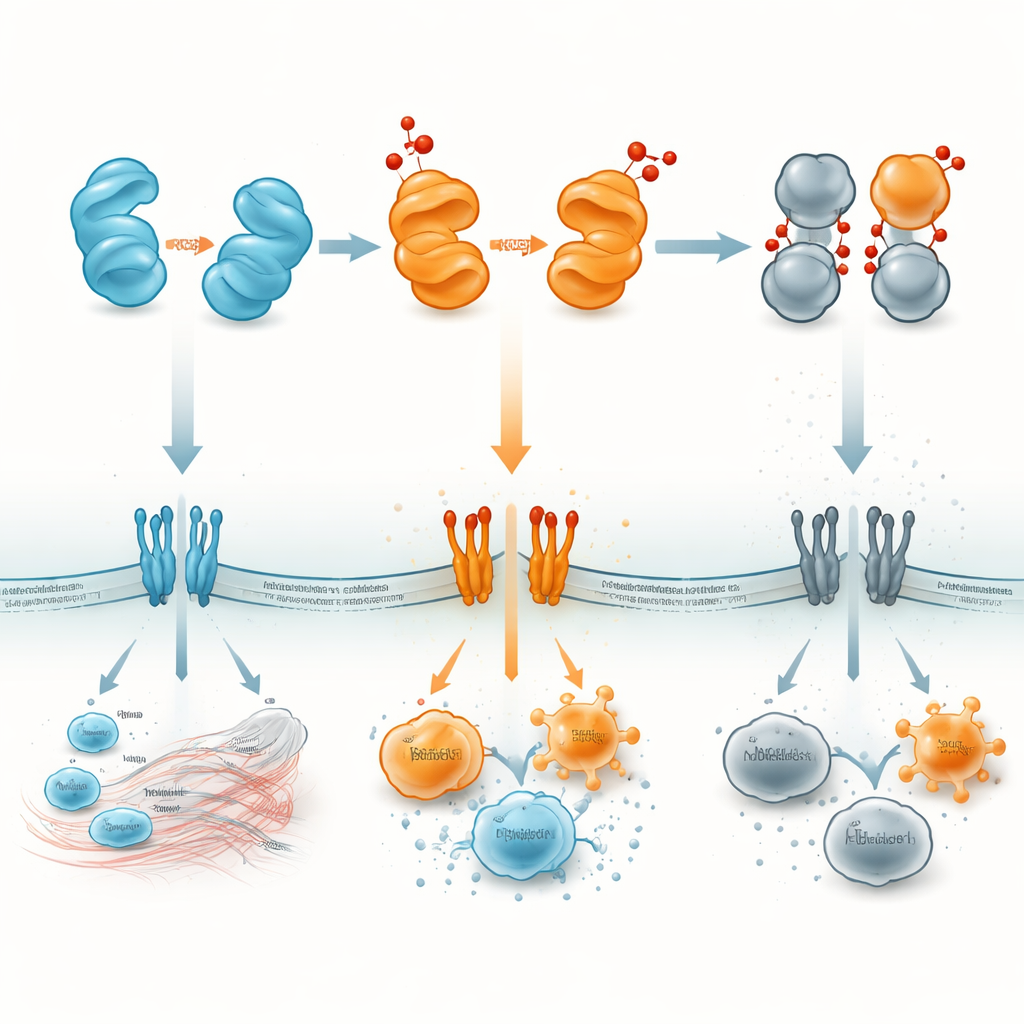
Центральная идея обзора — то, как окисление, реакции, управляемые реактивными формами кислорода (ROS), перекраивает свойства HMGB1. В белке есть три серосодержащих остатка, действующих как крошечные переключатели. В полностью восстановленном состоянии HMGB1 способствует выживанию клеток и привлечению клеток восстановления. Лёгкое окисление может связать два таких участка внутри одной молекулы, образовав «дисульфидную» форму, которая особенно хорошо связывается с иммунными рецепторами, такими как Toll-подобные рецепторы и RAGE на поверхности клеток. Эта форма сильно стимулирует выработку провоспалительных медиаторов. Более выраженный окислительный стресс может продвинуть молекулу в перенасыщенную, «перокислённую» форму, которая уже не способна эффективно связываться с ДНК или рецепторами; эта «выгоревшая» версия становится иммунологически молчаливой и связана с фазой разрешения воспаления и программами клеточной смерти, не вызывающими иммунного ответа.
От сигналов клеточной смерти до факторов болезни
HMGB1 тесно переплетён с множеством путей клеточной гибели. При насильственных формах смерти, таких как некроз, некроптоз, ферроптоз и піроптоз, HMGB1 вытекает или активно транспортируется из клеток, неся редокс-подпись, отражающую оксидативные условия окружающей среды. На ранних стадиях некроза он склонен быть в восстановленной форме, тогда как продолжительный стресс сдвигает его к более окисленным состояниям. Попав наружу, восстановленный HMGB1 может способствовать защитной аутофагии в некоторых раковых клетках, помогая им пережить химиотерапию, тогда как дисульфидные и димерные формы усиливают воспалительные каскады и активацию комплемента, что может усугублять повреждение тканей. HMGB1 также способен подкреплять определённые пути смерти — например, в сочетании с бактериальными липидами вызывать некроптоз или усиливать железозависимую гибель клеток в глиальных клетках мозга после инсульта. Таким образом, HMGB1 одновременно маркирует и модулирует баланс жизни и смерти в тканях.
Связи с воспалением, аутоиммунитетом и раком
Поскольку поведение HMGB1 сильно зависит от степени окисления, разные варианты белка встречаются в характерных паттернах при различных заболеваниях. Дисульфидная форма тесно связана с хроническим воспалением: её обнаруживают в воспалённых суставах при ревматоидном артрите, в фиброзной печени, при повреждении лёгких, при ишемии‑реперфузионном повреждении после операции и при сепсисе, где её уровни в крови коррелируют с тяжестью состояния и риском смерти. Восстановленная форма HMGB1, напротив, часто ассоциируется с миграцией клеток и ремоделированием тканей, например с перемещением кардиальных фибробластов или моноцитов под влиянием хемокина CXCL12. Перокислённая, иммунологически тихая форма обогащена в ситуациях поздней апоптоза, когда организму важно утилизировать умирающие клетки без провокации атаки. В опухолях дисульфидная форма поддерживает иммуносупрессивную, ростопригодную среду, тогда как блокирование HMGB1 может приводить к уменьшению опухолей и повышать эффективность иммунотерапии с блокаторами контрольных точек.
Превращение молекулярной тревоги в терапевтическую цель
Для неспециалиста HMGB1 можно представить как небольшой белковый сигнал тревоги, чей «громкость» и послание меняются с его химическим состоянием. Восстановленная форма склонна звать ремонтные бригады; дисульфидные и димерные формы могут поднимать резкий сигнал, подпитывающий повреждающее воспаление; а полностью окисленная форма фактически замолкает, помогая завершить воспаление. Нанёсши карту того, где и когда появляется каждая версия — в ядрах, в цитоплазме, в крови или в отдельных органах — исследователи надеются разработать препараты, которые либо блокируют вредные формы, либо стабилизируют полезные. Такие стратегии могут позволить лечить сепсис, аутоиммунные болезни, инсульт, повреждение лёгких или рак, воздействуя не только на сам HMGB1, но и на окислительный «реостат», контролирующий, как этот белок «общается» с иммунной системой.
Цитирование: Kwak, M.S., Jung, S.F., Park, I.H. et al. The redox-sensitive protein HMGB1: intracellular and extracellular roles. Exp Mol Med 58, 345–356 (2026). https://doi.org/10.1038/s12276-026-01640-3
Ключевые слова: HMGB1, воспаление, окислительный стресс, клеточная смерть, аутоиммунное заболевание