Clear Sky Science · ru
UBE2M как мост между неддилированием и регуляцией клеточного цикла при аденокарциноме толстой кишки
Почему это исследование важно при раке кишечника
Колоректальный рак — один из самых распространённых и смертоносных видов рака в мире, во многом потому, что опухолевые клетки обучаются бесконтрольно делиться. Это исследование выявляет ранее скрытый переключатель, который помогает клеткам колоректального рака пройти критический контрольный пункт деления. Показав, как этот переключатель работает на молекулярном уровне, и продемонстрировав, что существующий противогрибковый препарат может вмешиваться в него, работа указывает на потенциально новый способ замедлить или остановить рост опухоли.
Скрытый уровень контроля внутри опухолевых клеток
Клетки не делятся случайно; они проходят упорядоченный цикл с контрольными точками, которые проверяют, безопасно ли копировать ДНК и делиться на две дочерние клетки. Раковые клетки часто вмешиваются в работу этих контрольных пунктов. Авторы сосредоточились на процессе химической маркировки белков, называемом неддилированием, который тонко изменяет белки после их синтеза. Ранние исследования указывали, что неддилирование активнее во многих типах рака, но не было ясно, как оно связано с циклом деления клеток при колоректальном раке. Используя крупные одномолекулярные наборы данных из человеческих опухолей, а также массивные данные экспрессии генов более чем у 1800 пациентов, команда обнаружила, что активность неддилирования особенно высока в злокачественных клетках кишечника, находящихся в фазе G2/M — последнем рубеже перед делением клетки.
В центре внимания молекулярный «мост»
Чтобы установить, какие молекулы связывают неддилирование с делением клеток, исследователи применили сетевые вычислительные анализы для отбора тысяч генов. Выделился один белок: UBE2M, фермент, помогающий прикреплять маленькую метку NEDD8 к другим белкам. UBE2M был не только тесно связан с путями неддилирования и клеточного цикла в данных; его также обнаруживали в значительно повышенных количествах в опухолях толстой кишки по сравнению с близкой нормальной тканью. У пациентов с опухолями, содержащими больше UBE2M, как правило, была худшая выживаемость, что свидетельствует о его роли драйвера, а не просто наблюдателя. Когда команда снижала уровень UBE2M в раковых клеточных линиях и в мышиных моделях опухолей, рост опухолей замедлялся, клетки реже делились, и число программируемой гибели клеток увеличивалось. Наоборот, вынужденная сверхэкспрессия UBE2M ускоряла рост и прогрессирование клеточного цикла.
Релейная цепочка, защищающая ключевой белок, стимулирующий рост
Углубляясь, учёные выяснили, как UBE2M способствует делению клеток. Они обнаружили, что UBE2M не действует в одиночку, а запускает релейную цепочку с участием двух других белков — USP39 и PABPC1. В норме PABPC1 помечается для разрушения цепочкой убиквитина, направляющей его в клеточный комплекс утилизации белков. Команда показала, что UBE2M модифицирует USP39 меткой NEDD8. Эта модификация усиливает способность USP39 отрезать цепочки убиквитина с PABPC1, спасая его от разрушения и повышая его стабильность. При избытке PABPC1 клетка эффективнее переводит определённые мРНК в белок, в том числе мРНК для CCNB1 — циклина, действующего как педаль газа на контрольной точке G2/M. По сути, UBE2M стабилизирует PABPC1, что в свою очередь увеличивает синтез CCNB1 и облегчает продвижение клеток к делению.
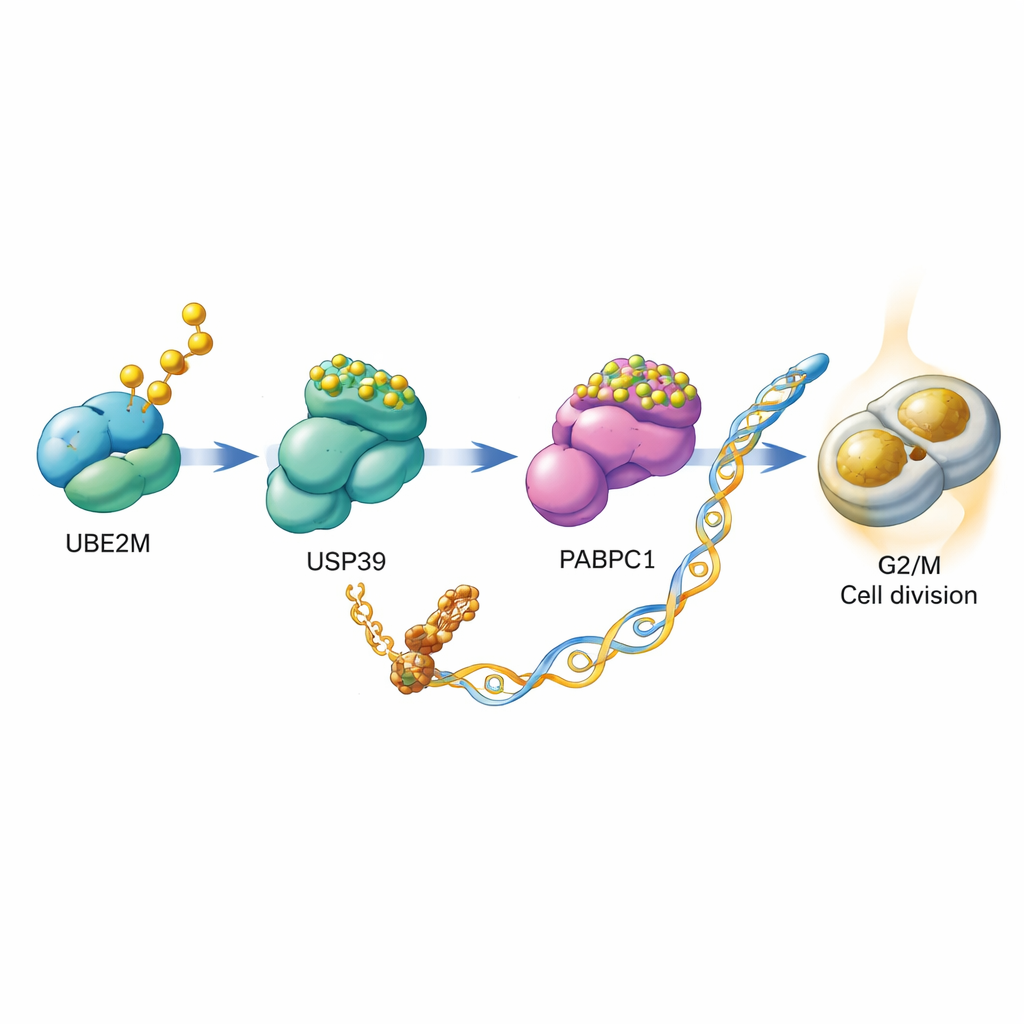
От молекулярного механизма к лекарственной возможности
Открытие цепочки UBE2M–USP39–PABPC1–CCNB1 выявило новую уязвимость в клетках колоректального рака. Авторы обратились к микaфунгину, препарату, уже применяемому для лечения грибковых инфекций и недавно идентифицированному как ингибитор нэддилирующей активности UBE2M. В клетках кишечного рака, выращенных в культуре, микaфунгин ослаблял неддилирование USP39, усиливал деградацию PABPC1 и снижал уровни белка CCNB1. В результате деление клеток замедлялось, больше клеток застревало на контрольной точке G2/M, и увеличивался апоптоз. У мышей с имплантированными клетками колоректального рака ежедневное лечение микaфунгином значительно уменьшало опухоли по сравнению с животными без лечения, без необходимости непосредственно удалять UBE2M.
Что это означает для пациентов в долгосрочной перспективе
Эта работа наглядно показывает, как один фермент, UBE2M, может связать тонкую систему маркировки белков с решением клетки кишечника о делении. Стабилизируя фактор трансляции (PABPC1) через USP39, UBE2M косвенно повышает уровни мощного регулятора клеточного цикла CCNB1, позволяя опухолям расти быстрее. Хотя необходимы дополнительные исследования и клинические испытания, результаты указывают на то, что блокирование этой релейной цепочки — возможно, с помощью репурпозированных препаратов, таких как микaфунгин — может предоставить новую таргетную стратегию для замедления прогрессирования колоректального рака и улучшения исходов для пациентов.
Цитирование: Wang, Z., Wang, Y., Chen, Y. et al. UBE2M as a bridge spanning neddylation and cell cycle regulation in colorectal adenocarcinoma. Exp Mol Med 58, 501–518 (2026). https://doi.org/10.1038/s12276-026-01636-z
Ключевые слова: колоректальный рак, клеточный цикл, неддилирование, UBE2M, таргетная терапия