Clear Sky Science · ru
Токсичность лекарств для желудочно-кишечного тракта и целостность барьера: нарушение, опосредованное цитоскелетом, в клинически релевантной модели человеческого кишечного эпителия
Почему побочные эффекты в кишечнике имеют значение
Многие лекарства против рака, воспалений и других заболеваний могут непреднамеренно повредить оболочку кишечника. Когда этот внутренний «слой кожи» кишки нарушен, у пациентов появляются диарея, боль, тошнота и плохое всасывание питательных веществ, иногда настолько тяжёлые, что врачам приходится прекращать или снижать жизнеобеспечивающие терапии. Тем не менее современные лабораторные тесты часто не выявляют эти проблемы до того, как препараты попадают к пациентам. В этом исследовании представлена более реалистичная лабораторная модель человеческого кишечника и показано, как она может раньше обнаруживать вредные для кишечника лекарства и раскрывать механизмы ослабления естественного барьера.
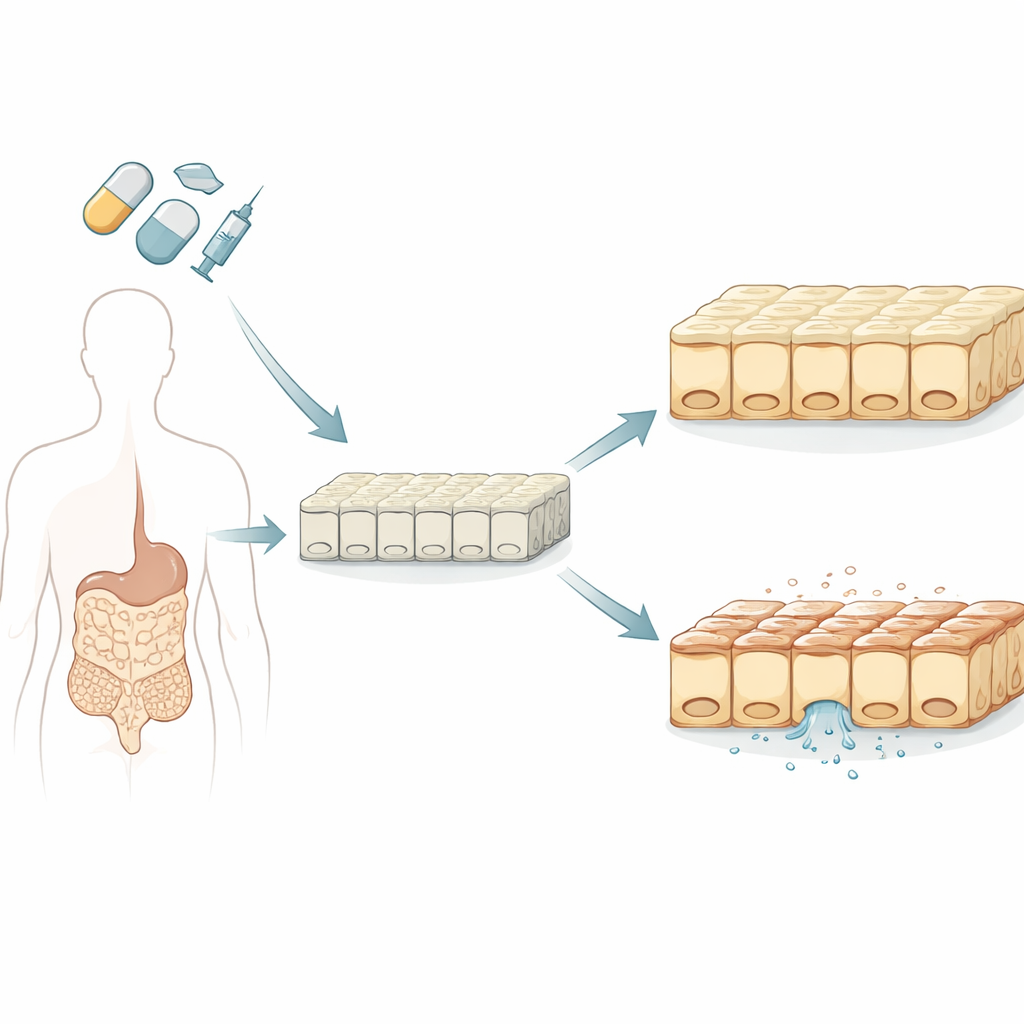
Создание лучшего мини-кишка
Исследователи начали с выращивания в лаборатории пластов человеческих кишечных клеток из стволовых клеток, которые способны развиваться в разные типы тканей. В отличие от традиционной опухолевой линии клеток, долго используемой для тестирования лекарств, эти клетки, полученные из стволовых, сформировали смешанное сообщество, ближе по составу к настоящему тонкому кишечнику, включая клетки, выделяющие слизь, и клетки, производящие гормоны. Команда подтвердила, что эти выращенные в лаборатории оболочки обладают реалистичной герметичностью, правильной апикально-базальной полярностью и ключевыми транспортными и метаболическими свойствами, которые влияют на то, как лекарства проходят через кишечник и обрабатываются в нём.
Измерение электрической плотности барьера
Для оценки безопасности кишечника группа сосредоточилась на трансэпителиальном электрическом сопротивлении, или TEER, неинвазивном показателе того, насколько плотно соседние клетки сцеплены между собой. Высокое TEER означает плотный, защитный барьер; падение TEER указывает на то, что стенка между кишечником и кровотоком становится проницаемой. Учёные сопоставили TEER со стандартным тестом на выживаемость клеток, который измеряет молекулы энергии, такие как АТФ. Они подвергли и новую модель кишечника, и старую опухолевую модель воздействию 17 препаратов, известных различной частотой вызова желудочно-кишечных побочных эффектов, включая распространённые химиотерапевтические средства, таргетные противораковые препараты и болеутоляющие, такие как ибупрофен и другие противовоспалительные препараты.
Выявление скрытого повреждения до гибели клеток
В обследуемой группе препаратов измерения TEER в кишечной выстилке, полученной из стволовых клеток, превзошли традиционный тест на АТФ и барьер старой опухолевой линии. Несколько химиотерапевтических препаратов почти не изменяли уровни АТФ, что указывало на то, что клетки ещё живы, но при этом вызывали сильное падение TEER и явные повреждения на изображениях с окраской «живые—мертвые». Это означает, что барьер может разрушаться до того, как клетки полностью погибнут — раннее предупреждение, которое пропускают классические тесты жизнеспособности. Сопоставив лабораторные результаты с клиническими данными о частоте кишечных симптомов для каждого препарата, новая TEER-ассай правильно пометила почти все лекарства с повышенным риском и дала верное успокоение для препаратов с низким риском, достигнув очень высокой точности.
Как лекарства подрывают внутренний каркас
Чтобы выяснить, что именно идёт не так внутри клеток, учёные проанализировали активность генов после лечения двумя химиотерапевтическими агентами, нацеленными на микротрубочки — ключевую часть внутреннего каркаса клетки. Они обнаружили широкое снижение экспрессии генов, вовлечённых в цитоскелет, клеточно-клеточные адгезии и внеклеточный матрикс — сеть, помогающую клеткам фиксироваться в окружении. Дополнительные эксперименты показали дозозависимое увеличение реактивных форм кислорода, нестабильных молекул, содержащих кислород, которые могут повреждать клеточные структуры. В совокупности эти изменения указывают на цепочку событий, при которой некоторые препараты нарушают внутренний каркас и соединения кишечных клеток, ослабляя барьер и позволяя веществам просачиваться между клетками.
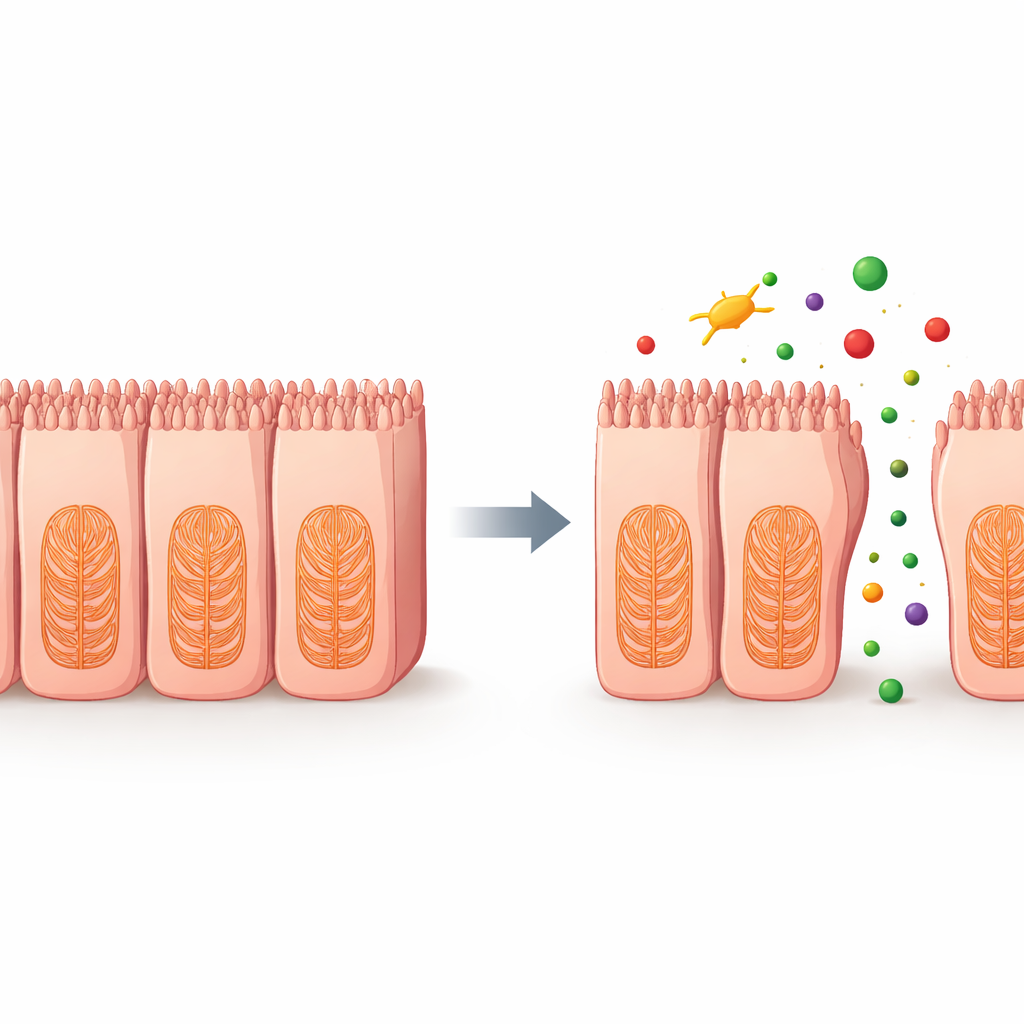
Что это означает для пациентов
Эта работа показывает, что человеческая кишечная выстилка на основе стволовых клеток в сочетании с простыми электрическими измерениями плотности барьера может более надёжно предсказывать, какие лекарства способны вызвать повреждение кишечника, по сравнению с длительно используемыми лабораторными методами. Обнаруживая ослабление барьера на ранней стадии и связывая его с лежащим в основе повреждением клеточного каркаса, эта платформа может помочь разработчикам лекарств отбраковывать или перерабатывать рискованные соединения ещё до их попадания в клинику. В долгосрочной перспективе такие реалистичные «мини-кишечные» тесты могут снизить неприятные или опасные желудочно-кишечные побочные эффекты у пациентов и позволить врачам безопаснее применять мощные терапии.
Цитирование: Yu, W.D., Lee, S., Cho, HS. et al. Drug-induced gastrointestinal toxicity and barrier integrity: cytoskeleton-mediated impairment in a clinically relevant human intestinal epithelium model. Exp Mol Med 58, 487–500 (2026). https://doi.org/10.1038/s12276-025-01635-6
Ключевые слова: токсичность желудочно-кишечного тракта, кишечный барьер, модель на стволовых клетках, безопасность лекарств, побочные эффекты химиотерапии