Clear Sky Science · pt
Detecção ultrassensível de biomarcadores da doença de Alzheimer com biossensores fotônicos de cristal em nanopilares
Por que um simples exame de sangue para perda de memória é importante
Com o surgimento de novos medicamentos que podem retardar a doença de Alzheimer, os médicos precisam com urgência de testes simples que revelem quem está em risco muito antes dos sintomas se tornarem óbvios. Hoje, confirmar Alzheimer geralmente significa imagens cerebrais caras ou punções lombares que poucas pessoas recebem na rotina clínica. Este estudo descreve um sensor minúsculo baseado em luz que pode identificar moléculas relacionadas ao Alzheimer em uma gota de sangue em níveis clinicamente relevantes, abrindo potencialmente o caminho para testes rápidos e de baixo custo que poderiam ser usados em clínicas comuns ou mesmo à beira do leito.
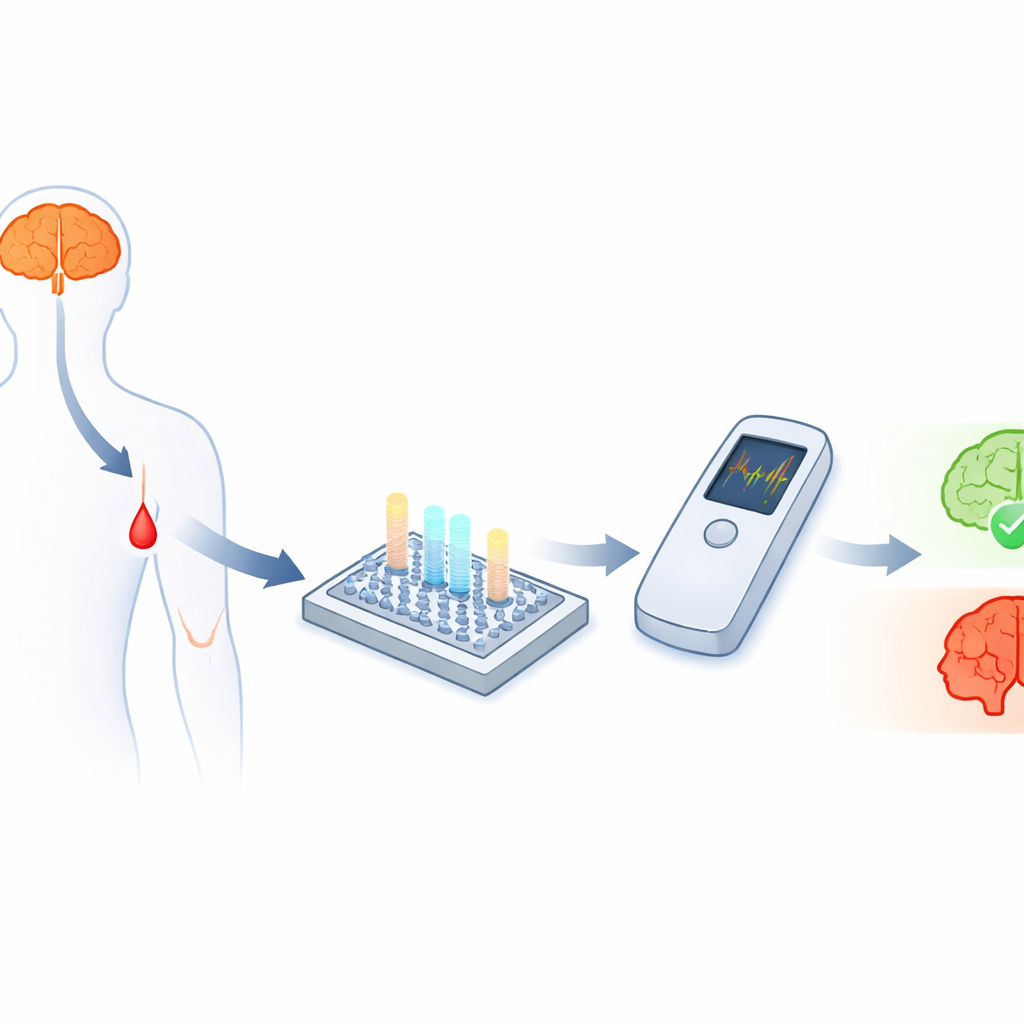
Procurando pistas no sangue
A doença de Alzheimer está fortemente relacionada a pequenos fragmentos proteicos chamados beta‑amiloide, especialmente duas formas conhecidas como Aβ40 e Aβ42. Suas quantidades, e particularmente a razão entre elas, carregam pistas importantes sobre se a doença está presente e como ela está progredindo. O desafio é que esses fragmentos são minúsculos e circulam no sangue em níveis extremamente baixos — trilionésimos de grama por mililitro — tornando-os muito difíceis de medir com precisão fora de laboratórios especializados. Embora sensores eletroquímicos possam, em princípio, detectar concentrações tão baixas, transformá‑los em testes robustos e acessíveis para uso ponto‑de‑atendimento que acompanhem vários biomarcadores ao mesmo tempo tem se mostrado difícil.
Guiando a luz por entre pilares minúsculos
A equipe enfrentou esse desafio usando nanofotônica — estruturas que controlam a luz em uma escala menor que o comprimento de onda dessa luz. Eles construíram um chip coberto por uma grade regular de pares de pilares de silício finíssimos sobre vidro. Quando a luz incide sobre essa superfície padronizada, ela fica presa em um modo ressonante especial que é extremamente sensível a mudanças perto das extremidades dos pilares, de modo parecido com o tom de um diapasão que muda se material é adicionado. Ao ajustar cuidadosamente a distância entre os pilares de cada par, os pesquisadores equilibraram três propriedades cruciais ao mesmo tempo: quão bem definida é a ressonância óptica, quão fortemente ela muda com o ambiente e quão grande sinal ela produz. Esse projeto em um “ponto ideal” torna o chip particularmente adequado para detectar quantidades minúsculas de material.
Tornando moléculas invisíveis visíveis
Mesmo com esse projeto otimizado, os marcadores de Alzheimer sozinhos mal perturbariam a luz. Para ampliar o efeito, os pesquisadores usaram uma estratégia em sanduíche com nanopartículas de ouro. Primeiro, revestiram a superfície do sensor com camadas de química adesiva que orientam corretamente anticorpos especializados, de modo que seus sítios de ligação fiquem voltados para o líquido. Esses anticorpos capturam Aβ40 ou Aβ42 da amostra. Em seguida, nanopartículas de ouro, cada uma decorada com um segundo anticorpo que reconhece outra extremidade do mesmo fragmento amiloide, são fluídas sobre o chip. Sempre que um fragmento amiloide está presente, ele faz a ponte entre a superfície e uma partícula de ouro, efetivamente “sinalizando” sua presença. Como o ouro perturba fortemente o ambiente óptico local, cada fragmento capturado produz uma mudança muito maior na ressonância do sensor do que o peptídeo sozinho, aumentando a sensibilidade em cerca de uma a duas ordens de grandeza enquanto ainda preserva um sinal óptico limpo.
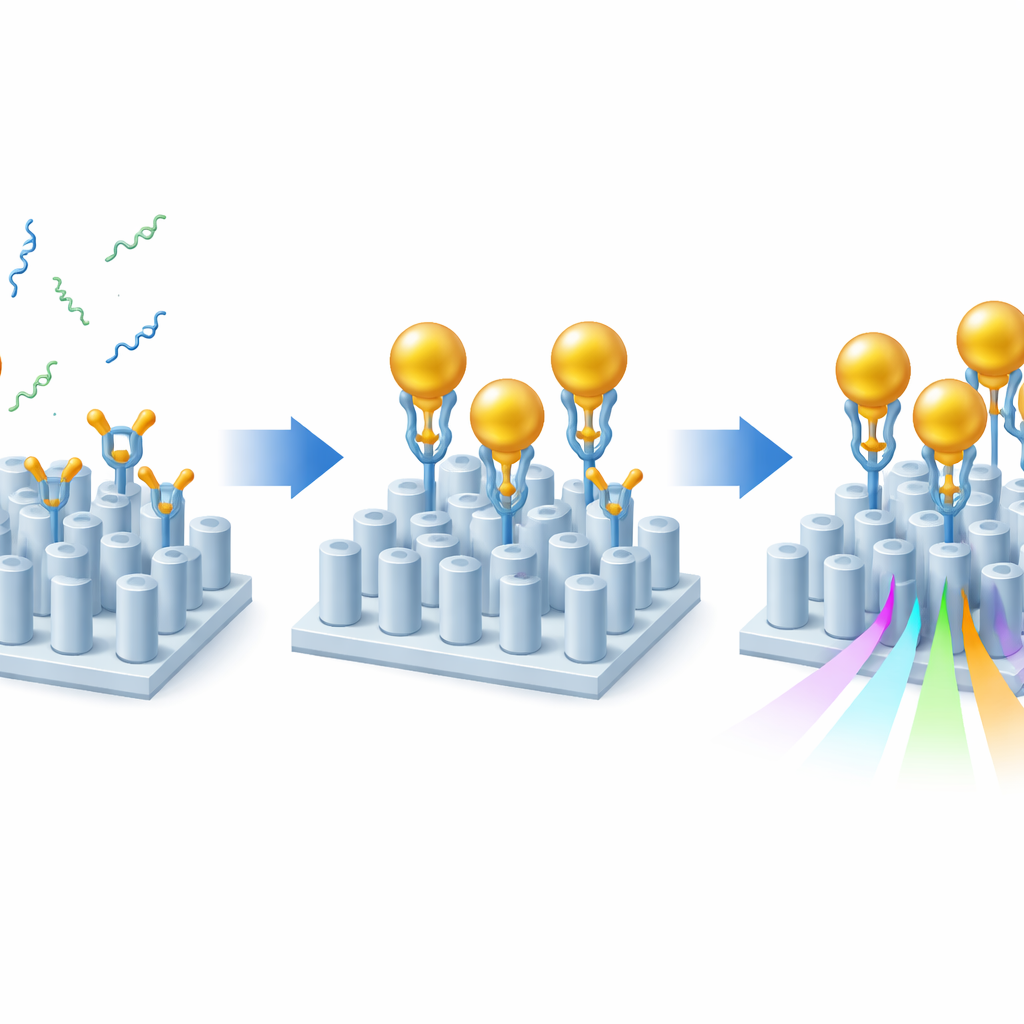
Testando amostras realistas
Para demonstrar que a abordagem funciona além de tampões laboratoriais simples, a equipe testou seu sensor com soro sanguíneo humano. Eles diluíram o soro para torná‑lo compatível com o manuseio microfluídico, mantendo os níveis de amiloide representativos dos encontrados em pacientes. De modo importante, conseguiram detectar tanto Aβ40 quanto Aβ42 a 0,2 picogramas por mililitro nesse soro diluído — equivalente ao nível clinicamente relevante de 20 picogramas por mililitro em sangue total. Ao posicionar diferentes anticorpos de captura em regiões separadas no mesmo chip, mediram simultaneamente ambas as formas de amiloide dentro de um único canal minúsculo, um passo chave para avaliar sua razão a partir de uma única pequena amostra. Os sinais distinguiram claramente amostras adicionadas com amiloide extra daquelas contendo apenas os níveis de fundo naturalmente presentes mesmo em pessoas saudáveis.
O que isso pode significar para os cuidados futuros
Em conjunto, esses avanços mostram que um sensor compacto baseado em luz, reforçado por nanopartículas de ouro, pode atingir as sensibilidades necessárias para testes sanguíneos significativos para Alzheimer enquanto lida com mais de um biomarcador ao mesmo tempo. Embora mais trabalho seja necessário para transformar isso em um dispositivo comercial robusto e para adicionar outros marcadores, como formas da proteína tau, a tecnologia subjacente é construída a partir de materiais escaláveis e pode ser pareada com ópticas simples e portáteis. Se totalmente desenvolvida, poderia permitir que clínicos monitorem a saúde cerebral usando apenas uma pequena amostra de sangue, tornando muito mais fácil detectar o Alzheimer precocemente e acompanhar quão bem os tratamentos estão funcionando ao longo do tempo.
Citação: Guilherme S. Arruda, Katie Morris, Augusto Martins, Yue Wang, Sian Sloan-Dennison, Duncan Graham, Steven D. Quinn, Emiliano R. Martins, and Thomas F. Krauss, "Ultrasensitive Alzheimer’s disease biomarker detection with nanopillar photonic crystal biosensors," Optica 12, 1587-1596 (2025). https://doi.org/10.1364/OPTICA.566672
Palavras-chave: teste sanguíneo para Alzheimer, biossensor nanofotônico, beta amiloide, nanopartículas de ouro, diagnóstico precoce