Clear Sky Science · pt
Ablatação tumoral seletiva via laser de femtossegundo ressonante com colágeno
Transformando a luz em uma ferramenta direcionada contra o câncer
O câncer de pâncreas é um dos mais letais da medicina, em parte porque é difícil removê‑lo sem prejudicar o órgão frágil que o envolve. Este estudo explora uma nova maneira de usar pulsos ultrarrápidos de luz infravermelha invisível para queimar tumores pancreáticos com maior precisão, ao mirar em um componente estrutural que os tumores carregam em excesso. O trabalho sugere tratamentos futuros que poderiam poupar mais tecido saudável mantendo um ataque eficaz ao câncer.
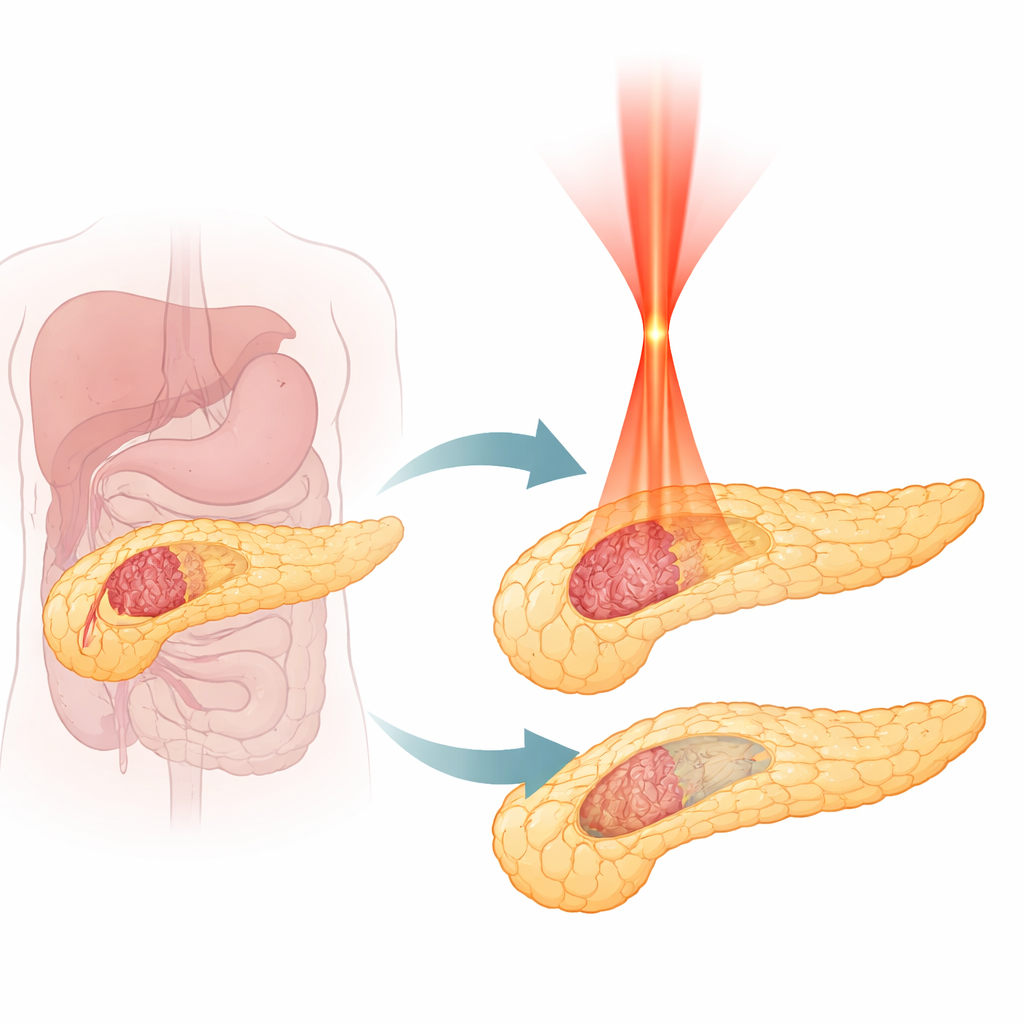
Por que os tumores pancreáticos são tão difíceis de tratar
O adenocarcinoma ductal pancreático, a forma mais comum de câncer de pâncreas, cresce de maneira agressiva e frequentemente é detectado tardiamente. Apenas uma pequena parcela dos pacientes é candidata à cirurgia, e mesmo a quimioterapia e a radioterapia modernas oferecem benefício limitado. Tratamentos baseados em calor que destroem tecido, como radiofrequência, micro-ondas ou ablação a laser convencional, podem reduzir tumores, mas tendem a queimar tudo em seu caminho. Como o pâncreas fica próximo a vasos sanguíneos vitais e estruturas digestivas delicadas, ampliar a zona de tratamento implica risco de complicações sérias. Por isso os médicos precisam de um método capaz de distinguir tumor de pâncreas normal durante a destruição, em vez de simplesmente cozinhar uma área ampla.
Encontrando um ponto fraco oculto no tecido tumoral
Os autores concentraram‑se em uma diferença física chave entre tumores pancreáticos e pâncreas saudável: os tumores estão repletos de material fibroso rígido rico em colágeno, enquanto o tecido normal é mais macio e frouxo. Usando colorações teciduais padrão e microscopia eletrônica em amostras cirúrgicas, mostraram que o tecido canceroso contém feixes densos de fibras de colágeno, enquanto o pâncreas saudável próximo apresenta muito menos. Em seguida, empregaram espectroscopia no infravermelho para medir o quanto esses tecidos absorvem diferentes cores de luz no infravermelho médio. Ambos os tecidos absorvem em comprimentos de onda semelhantes, mas os tumores exibem um pico muito mais forte próximo a 6,1 micrômetros, que corresponde a vibrações do colágeno. Isso sugeriu que um laser afinado precisamente para esse comprimento de onda poderia aquecer e decompor o tecido tumoral de maneira mais eficiente que o pâncreas normal.
Construindo um laser que “ouve” o colágeno
Para testar a ideia, a equipe construiu um laser potente no infravermelho médio que emite pulsos ultracurtos — durando apenas algumas centenas de quadrilionésimos de segundo — centrados em 6,1 micrômetros. Esses pulsos “femtossegundo” limitam a propagação indesejada de calor, de modo análogo a uma série de pequenos e controlados relâmpagos. O sistema converte luz de um laser industrial de alta potência para o comprimento de onda desejado usando cristais especiais e pode entregar mais de um watt de potência média; isso é suficiente para ablação tecidual prática. Os pesquisadores também desenvolveram uma fibra oca de vidro capaz de guiar essa luz ao longo de um trajeto flexível, um passo importante rumo a conduzir o laser por uma agulha fina para dentro do corpo em procedimentos minimamente invasivos.
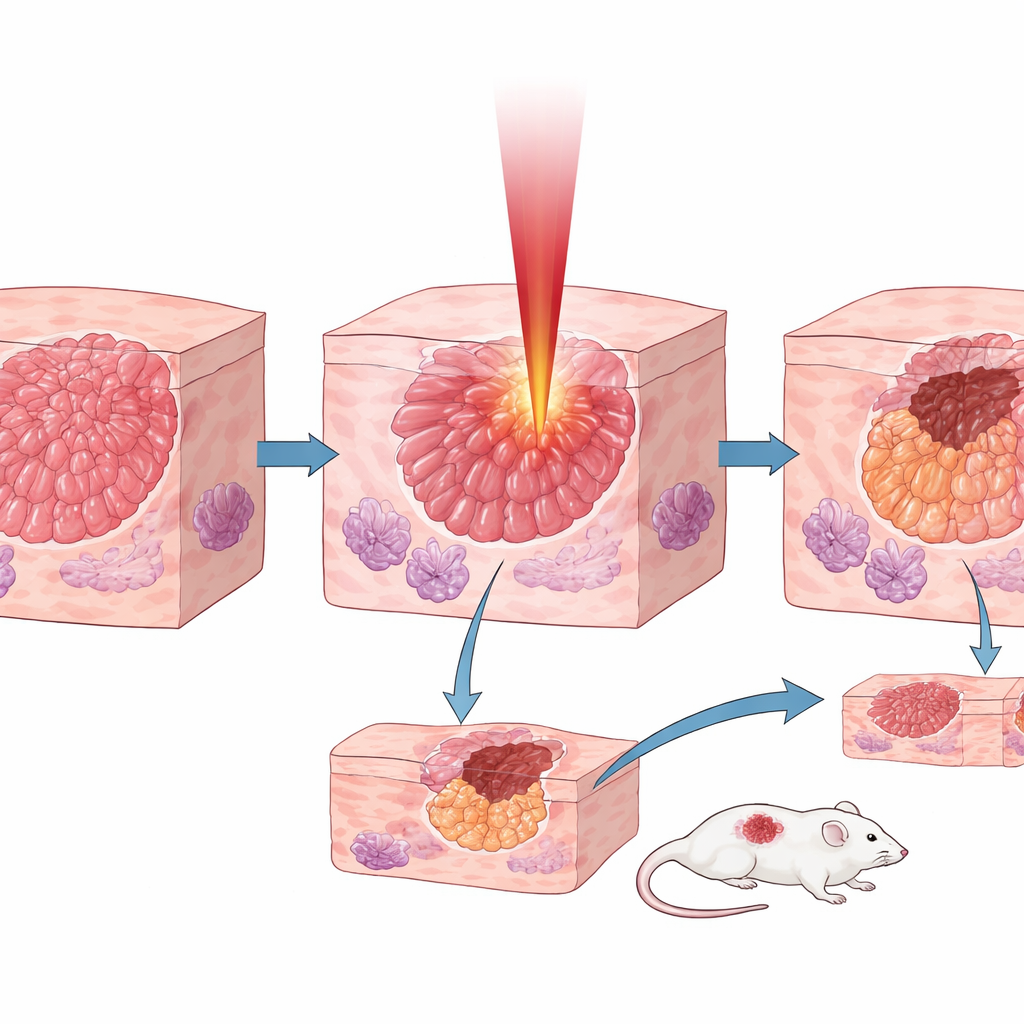
Testando a seletividade em células, camundongos e tecido humano
Em culturas celulares de duas linhagens de câncer pancreático, o laser de 6,1 micrômetros foi muito mais letal do que lasers em 1 ou 3 micrômetros, reduzindo acentuadamente a sobrevivência celular em segundos a minutos de exposição. Em camundongos com tumores pancreáticos sob a pele, três comprimentos de onda foram comparados. Apesar de o feixe de 1 micrômetro transportar potência muito maior, ele removeu apenas camadas superficiais do tumor. O laser afinado no colágeno, de 6,1 micrômetros, alcançou profundidades de ablação cinco a dez vezes maiores e retardou o crescimento tumoral de forma tão dramática que os tumores tratados ficaram em média apenas cerca de um oitavo do tamanho dos dos animais não tratados. Mais importante, quando aplicaram o laser de 6,1 micrômetros em amostras humanas de tumor e do pâncreas normal adjacente, os cortes no tumor foram duas a três vezes mais profundos do que no tecido saudável sob as mesmas condições, revelando verdadeira seletividade. Em contraste, ao testar outro tipo de tumor hepático que não acumula colágeno extra, a vantagem desapareceu em grande parte, reforçando o papel central do colágeno. Por fim, demonstraram que a fibra oca podia entregar o mesmo efeito seletivo, apoiando tratamentos futuros baseados em agulha.
O que isso pode significar para o futuro do cuidado contra o câncer
O estudo demonstra que rajadas cuidadosamente afinadas de luz no infravermelho médio podem explorar uma diferença material entre tumores e tecido saudável para alcançar destruição mais seletiva. Ao mirar regiões ricas em colágeno, o laser femtossegundo de 6,1 micrômetros penetra mais fundo no câncer pancreático poupando maior parte do órgão circundante. Embora o trabalho ainda esteja em estágio experimental, e mais testes em modelos realistas e cenários clínicos sejam necessários, aponta para uma nova classe de procedimentos guiados por imagem e entregues por fibra que poderiam tratar não apenas tumores pancreáticos mas também outros cânceres ricos em colágeno com maior precisão e menos efeitos colaterais.
Citação: Dunxiang Zhang, Xing Huang, Xuemei Yang, Ning Xia, Kan Tian, Jinmiao Guo, Maoxing Xiang, Linzhen He, Zhizhuo Fu, Ang Deng, Han Wu, Yuxi Wang, Wonkeun Chang, Bole Tian, Junjie Xiong, Qi Jie Wang, Anderson S. L. Gomes, and Houkun Liang, "Selective tumor ablation via femtosecond laser resonant with collagen," Optica 12, 1578-1586 (2025). https://doi.org/10.1364/OPTICA.561337
Palavras-chave: câncer de pâncreas, ablação por laser, colágeno, infravermelho médio, cirurgia minimamente invasiva