Clear Sky Science · pt
A origem na estrutura quaternária da fibrilação da hemoglobina falciforme: um estudo por dinâmica molecular
Por que esta história do sangue importa
A doença falciforme começa com uma mudança minúscula em uma proteína sanguínea, mas pode remodelar glóbulos vermelhos, bloquear vasos e causar dor ao longo da vida. Este estudo examina de perto, com base em princípios físicos, como essa única alteração faz a hemoglobina empilhar-se em fibras rígidas dentro da célula. Usando simulações computacionais avançadas, os autores conectam detalhes atômicos a problemas em escala celular, oferecendo pistas novas sobre como futuros medicamentos podem impedir que a hemoglobina trave a circulação.
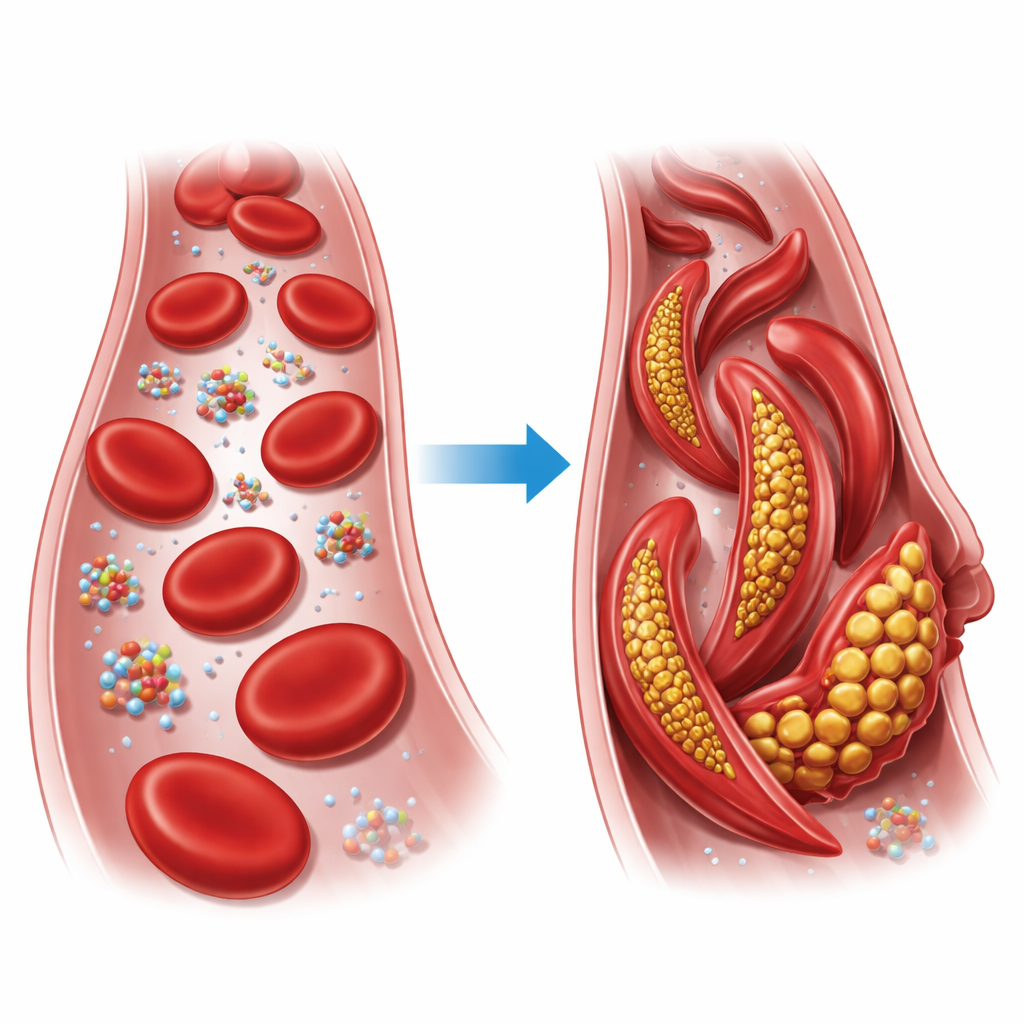
Uma troca pequena com grandes consequências
A hemoglobina é a proteína transportadora de oxigênio que ocupa nossos glóbulos vermelhos. Cada unidade de hemoglobina é formada por quatro cadeias que podem se organizar em duas formas gerais principais, conhecidas como estado relaxado (R) e estado tenso (T). Na doença falciforme, apenas um bloco construtivo em uma dessas cadeias é trocado: um glutamato carregado é substituído por uma valina apolar na posição seis da cadeia beta. Em condições de baixo oxigênio, essa versão alterada, chamada hemoglobina falciforme, liga-se em longas fibras que deformam glóbulos vermelhos normalmente arredondados em formas rígidas e em foice, que podem entupir pequenos vasos e privar tecidos de oxigênio.
Acompanhar a mudança de forma da hemoglobina
Os autores concentram-se em como unidades inteiras de hemoglobina giram e se empacotam em uma fibra. Eles acompanham essa mudança de grande escala com um único ângulo que mede como duas metades da proteína se torcem entre si. Usando simulações de dinâmica molecular — experimentos virtuais que calculam como átomos se movem ao longo do tempo em água e sal — eles forçam esse ângulo por uma ampla faixa e calculam quanto energia cada conformação exige. Descobrem que tanto a hemoglobina normal quanto a falciforme podem explorar muitas dessas formas na temperatura corporal. A hemoglobina falciforme mostra um ângulo ligeiramente preferido, mas essas preferências de forma por si só não explicam por que apenas a forma falciforme forma fibras estáveis.
Por que as fibras falciformes aderem e as normais se desfazem
Para investigar a formação da fibra, o estudo mede quão fortemente unidades vizinhas de hemoglobina se atraem ao longo e através da fibra. A equipe calcula a energia coesiva — a força líquida que mantém as unidades unidas — para muitas conformações gerais diferentes. Na hemoglobina falciforme, essa energia coesiva permanece negativa (ou seja, atrativa) ao longo de toda a faixa de formas testadas, de modo que as fibras permanecem estáveis e não se desfazem facilmente. Na hemoglobina normal, em contraste, algumas conformações apresentam energia coesiva positiva, tornando as fibras nesses ângulos instáveis e propensas à quebra espontânea. Uma diferença chave é como os grupos laterais da valina mutada se encaixam nas proteínas vizinhas: na hemoglobina falciforme, essas manchas apolares formam contatos robustos tanto lateralmente quanto ao longo do eixo da fibra, promovendo diretamente o crescimento da fibra.
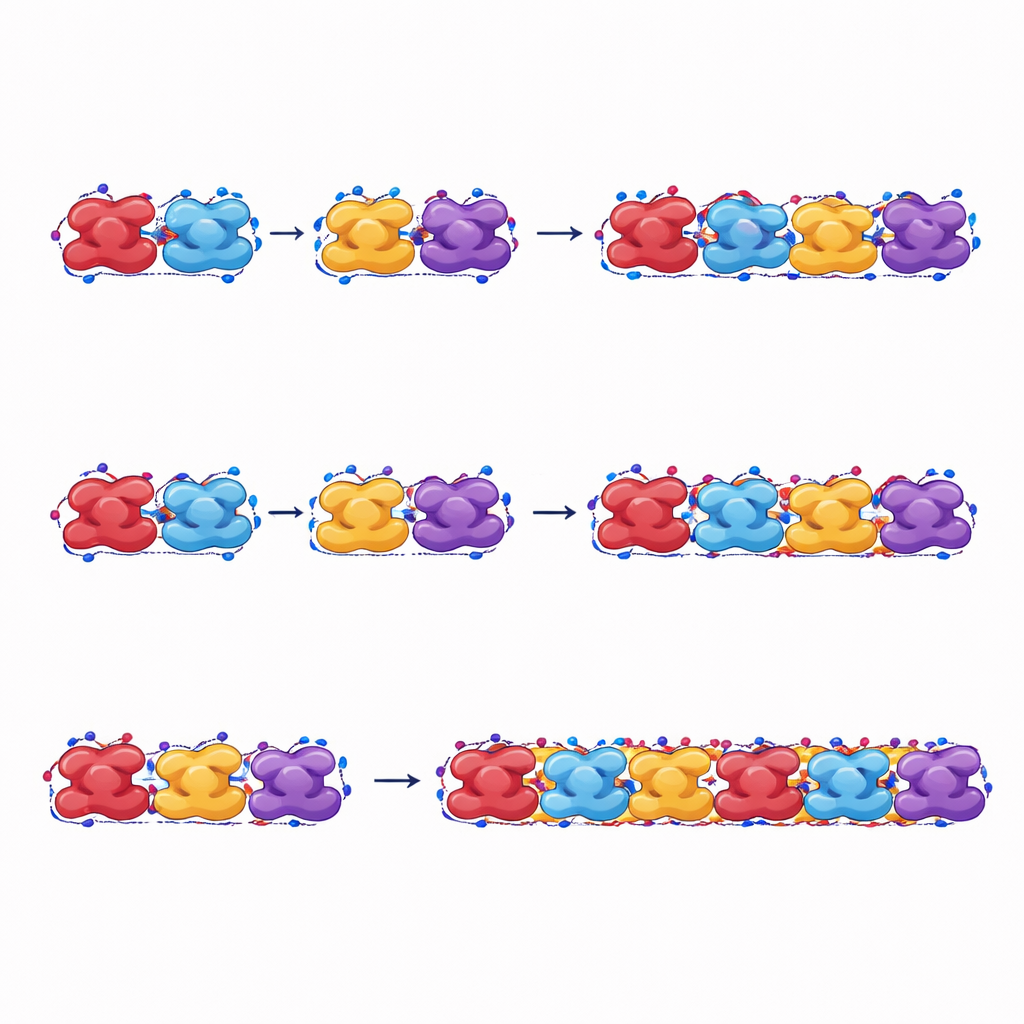
Como essas fibras suportam carga e quebram
Os autores também esticam suas fibras simuladas para mimetizar estresse mecânico. Quando puxadas ao longo de seu comprimento, fibras feitas de hemoglobina falciforme suportam forças e deformações maiores e dissipam mais energia antes de romper do que aquelas feitas de hemoglobina normal. Mesmo a forma relaxada das fibras falciformes, que não é a que aparece inicialmente, ainda consegue manter a cadeia por meio de mudanças plásticas na conformação, ajudando a manter a fibra íntegra uma vez formada. Fibras de hemoglobina normal, por outro lado, se separam mais facilmente entre unidades vizinhas e absorvem menos energia antes da falha, confirmando que são menos estáveis sob tensão.
Pistas para tratamentos futuros e novos materiais
No conjunto, as simulações mostram que uma única mudança de aminoácido remodela a maneira como unidades de hemoglobina se encontram, torcendo o arranjo geral para ângulos que favorecem forte atração, especialmente no estado tenso. Essa combinação de geometria e adesão permite que a hemoglobina falciforme forme fibras longas e rígidas que resistem tanto ao movimento térmico quanto à tração mecânica, o que, em última instância, deforma glóbulos vermelhos e bloqueia o fluxo sanguíneo. Ao apontar recursos específicos do arranjo proteico que controlam a estabilidade da fibra, o trabalho sugere que fármacos antisickling eficazes poderiam agir empurrando a hemoglobina para formas em que as fibras se tornem energeticamente desfavoráveis e mecanicamente frágeis — transformando um entupimento molecular letal de volta em um fluxo sanguíneo livre.
Citação: Jiang, M., Qin, Z. The quaternary structure origin of the fibrillation of sickle hemoglobin: a molecular dynamics study. npj Soft Matter 2, 7 (2026). https://doi.org/10.1038/s44431-026-00019-8
Palavras-chave: doença falciforme, fibras de hemoglobina, agregação de proteínas, dinâmica molecular, distúrbios sanguíneos