Clear Sky Science · pt
A dinamina otimiza interações proteína-membrana para a fissão
Como as células pinçam com precisão suas próprias membranas
Cada segundo, suas células estão ocupadas pinçando minúsculas bolhas de membrana para movimentar cargas, remodelar compartimentos internos e combater vírus. Esse ato aparentemente simples de cortar um tubo de membrana fino em dois pedaços revela-se surpreendentemente difícil do ponto de vista físico. Este artigo faz uma pergunta aparentemente básica: como uma proteína chamada dinamina torna o corte da membrana tanto possível quanto confiável, e quais características da proteína são realmente essenciais para a tarefa?
Os pinçadores celulares em ação
A dinamina é uma máquina molecular que forma um colar em torno de tubos de membrana finos e se aperta como um laço para ajudar a sua ruptura. Eventos de fissão desse tipo sustentam processos como a endocitose, em que as células internalizam material, bem como a divisão de estruturas internas como as mitocôndrias. Se deixado sozinho, um tubo de membrana resiste fortemente a quebrar, porque primeiro precisa ser comprimido até quase a espessura da própria membrana e passar por um estado intermediário instável. Essa barreira energética é muito maior que a energia de agitação aleatória disponível dentro de uma célula, portanto proteínas especializadas de fissão como a dinamina são essenciais.
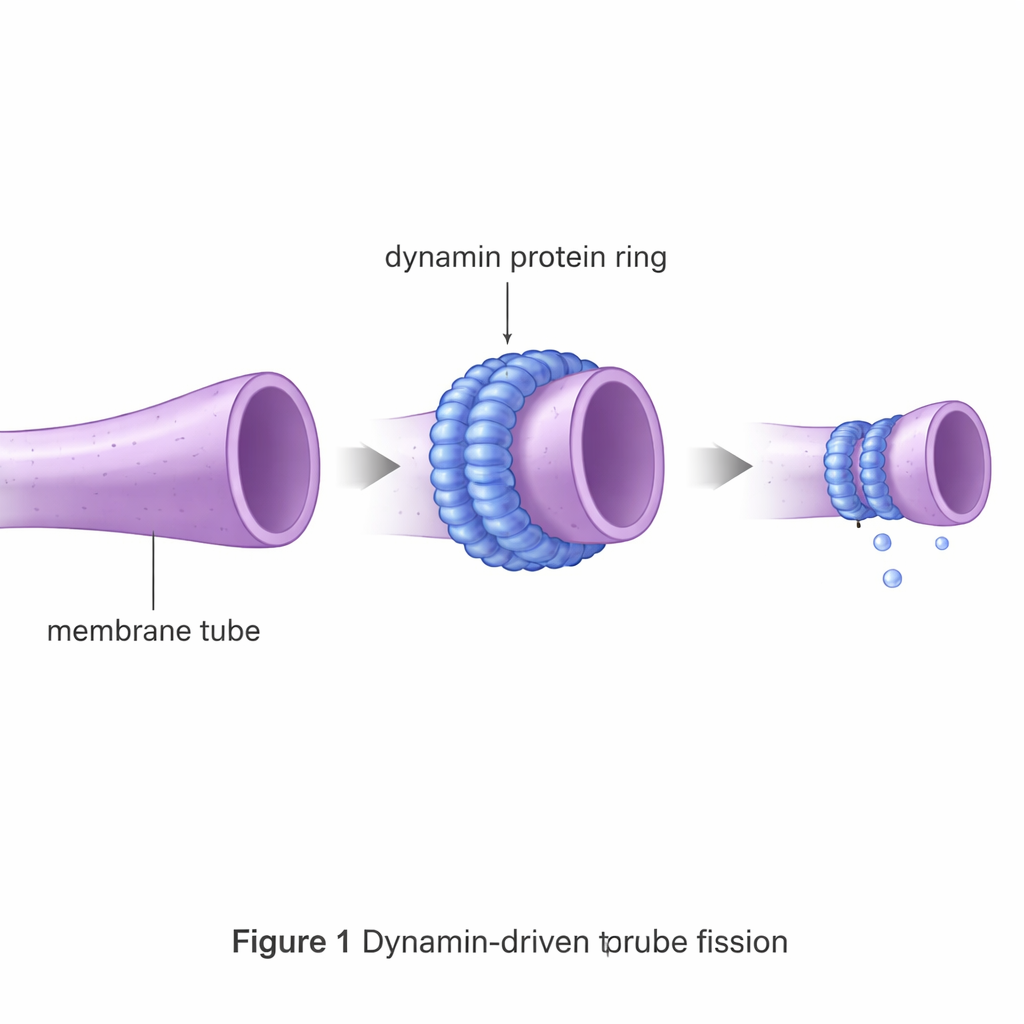
Usando membranas virtuais para testar projetos de proteínas
Observar diretamente o instante crítico em que um tubo se rompe é extremamente difícil em experimentos: imagens rápidas carecem de detalhe molecular, e métodos de alta resolução congelam o sistema no tempo. Para preencher essa lacuna, os autores usam uma poderosa ferramenta teórica chamada teoria de campo autoconsistente. Em vez de acompanhar cada átomo, eles descrevem lipídios e solvente como cadeias flexíveis que sentem campos que variam de forma suave. As proteínas são introduzidas não como estruturas atômicas completas, mas como potenciais externos em forma de toro que ou simplesmente excluem espaço, aderem à superfície da membrana ou se inserem na camada externa. Com esse arcabouço, eles podem calcular tanto as formas resultantes da membrana quanto o custo livre total de energia para ir de um tubo intacto até o intermediário de fissão.
Que tipo de aderência ajuda um tubo a romper?
A equipe varia sistematicamente como uma proteína semelhante à dinamina interage com a membrana. Algumas proteínas-modelo apenas aglomeram a superfície, atuando como uma braçadeira rígida; outras são moderada ou fortemente aderentes aos grupamentos de cabeça externos; ainda outras imitam o domínio PH real da dinamina inserindo partes hidrofóbicas na monocamada externa e “afastando” os grupamentos de cabeça. Para cada caso, eles examinam três quantidades interligadas: quão fortemente a proteína adere a um tubo não constrito, quanta curvatura e constrição ela induz quando ligada, e quão alta permanece a barreira energética para o tubo passar a um estado de hemifissão em que as camadas internas se fundiram. Eles descobrem que a simples compressão reduz a barreira, mas não o suficiente para explicar a fissão eficiente, e que forte adesão superficial pode realmente dificultar a quebra porque a membrana precisa primeiro descolar da proteína para completar o colapso.
Por que inserção rasa vence compressão simples
O desenho mais eficaz é aquele em que a proteína se insere parcialmente entre os grupamentos de cabeça lipídicos e puxa suas caudas para cima, criando uma curvatura local em forma de “chevron” na membrana. Esse “splay” desloca o ponto mais estreito do tubo ligeiramente para o lado do anel proteico em vez de diretamente abaixo dele. Como resultado, a membrana pode completar o colapso crítico até o intermediário de hemifissão sem se destacar da proteína, e a barreira energética global cai mais de uma ordem de grandeza em comparação com um tubo nu. Quando os autores permitem que os parâmetros da proteína se ajustem automaticamente para minimizar essa barreira, a solução ótima corresponde de perto ao tamanho e à ação do domínio PH da dinamina: uma mancha hidrofóbica moderadamente larga que se insere de forma rasa, não uma superfície ampla e excessivamente pegajosa que arrancaria lipídios da solução.
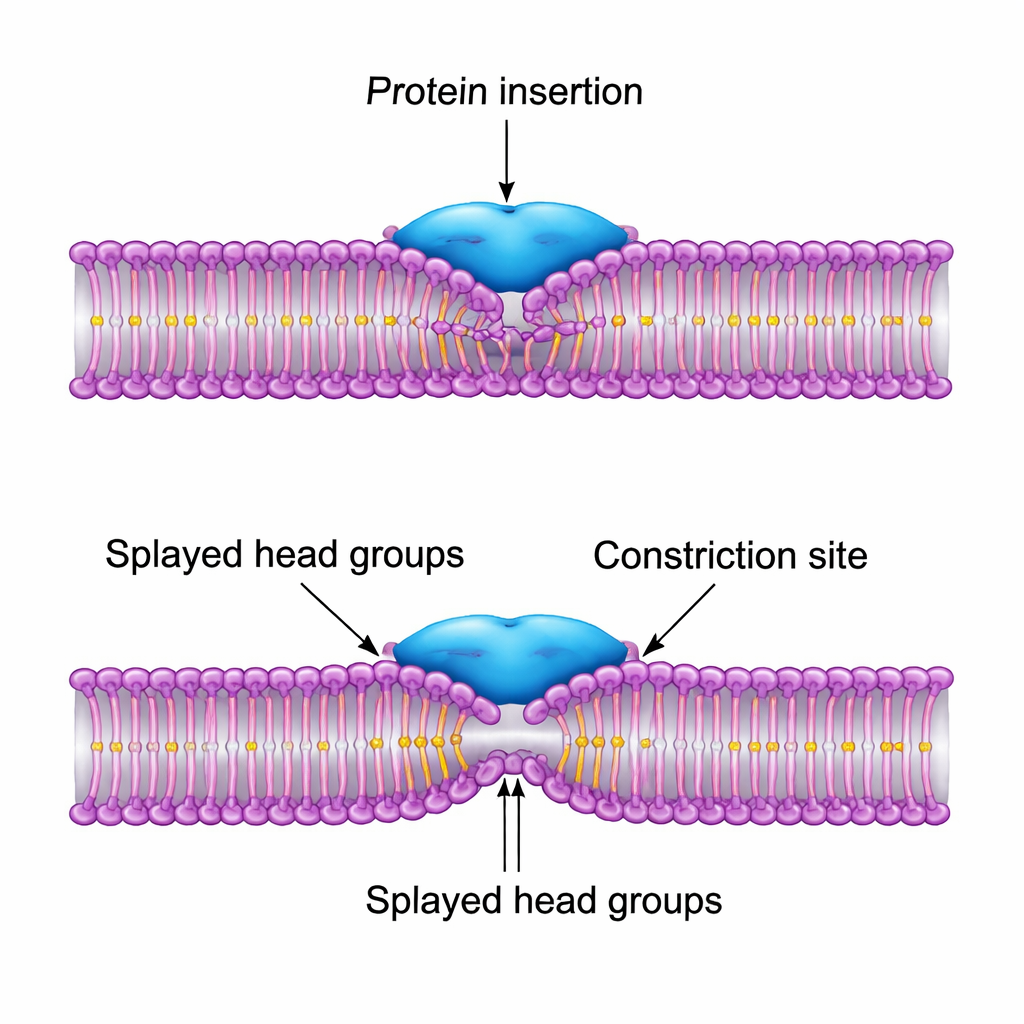
Regras de projeto para a natureza e para a nanotecnologia
Para um não especialista, a mensagem-chave é que a dinamina não age apenas apertando um cinto em volta da membrana, mas ajustando cuidadosamente como e onde ela prende a camada externa. Uma cunha rasa que afasta os lipídios externos e concentra a curvatura logo ao lado da proteína prova-se muito mais eficaz do que constrição bruta ou adesão forte. Esses resultados ajudam a explicar por que a evolução favoreceu a arquitetura particular da dinamina e sugerem princípios de projeto para proteínas sintéticas ou fármacos que precisam cortar ou remodelar membranas de forma controlada na medicina e na nanotecnologia.
Citação: Spencer, R.K.W., Müller, M. Dynamin optimizes protein-membrane interactions for fission. npj Soft Matter 2, 6 (2026). https://doi.org/10.1038/s44431-026-00018-9
Palavras-chave: fissão de membrana, dinamina, interações proteína–membrana, curvatura de membrana, teoria de campo autoconsistente