Clear Sky Science · pt
Ponte entre modelagem computacional e experimental: aproveitando modelos de linguagem grandes para priorizar terapias para Alzheimer com base na comparação de modelos de aprendizado
Por que isso importa para famílias e pacientes
A doença de Alzheimer rouba das pessoas a memória, a independência e a qualidade de vida, e tratamentos realmente eficazes continuam escassos. Este estudo explora uma maneira mais rápida de encontrar novos tratamentos usando medicamentos já existentes, combinando modelos computacionais poderosos com um grande modelo de linguagem — o mesmo tipo de IA agora usado em chatbots cotidianos — para vasculhar enormes quantidades de dados médicos e artigos científicos. O objetivo é reduzir uma longa lista de fármacos possíveis a um conjunto pequeno e realista que cientistas e médicos possam realmente testar em pacientes.
Reaproveitando medicamentos antigos para um novo propósito
Desenvolver um medicamento totalmente novo do zero pode levar mais de uma década e custar bilhões de dólares, sem garantia de sucesso. Uma alternativa é o “reposicionamento de medicamentos”, que busca novos usos para fármacos já aprovados para outras condições, como Parkinson ou depressão. Como esses medicamentos têm perfis de segurança conhecidos, eles frequentemente podem avançar mais rapidamente para ensaios clínicos para Alzheimer. Mas os métodos computacionais modernos que vasculham bancos de dados biológicos e a literatura médica agora geram listas enormes de candidatos — muito mais do que os pesquisadores podem avaliar manualmente — criando um novo gargalo no processo.
Combinando vários modelos inteligentes
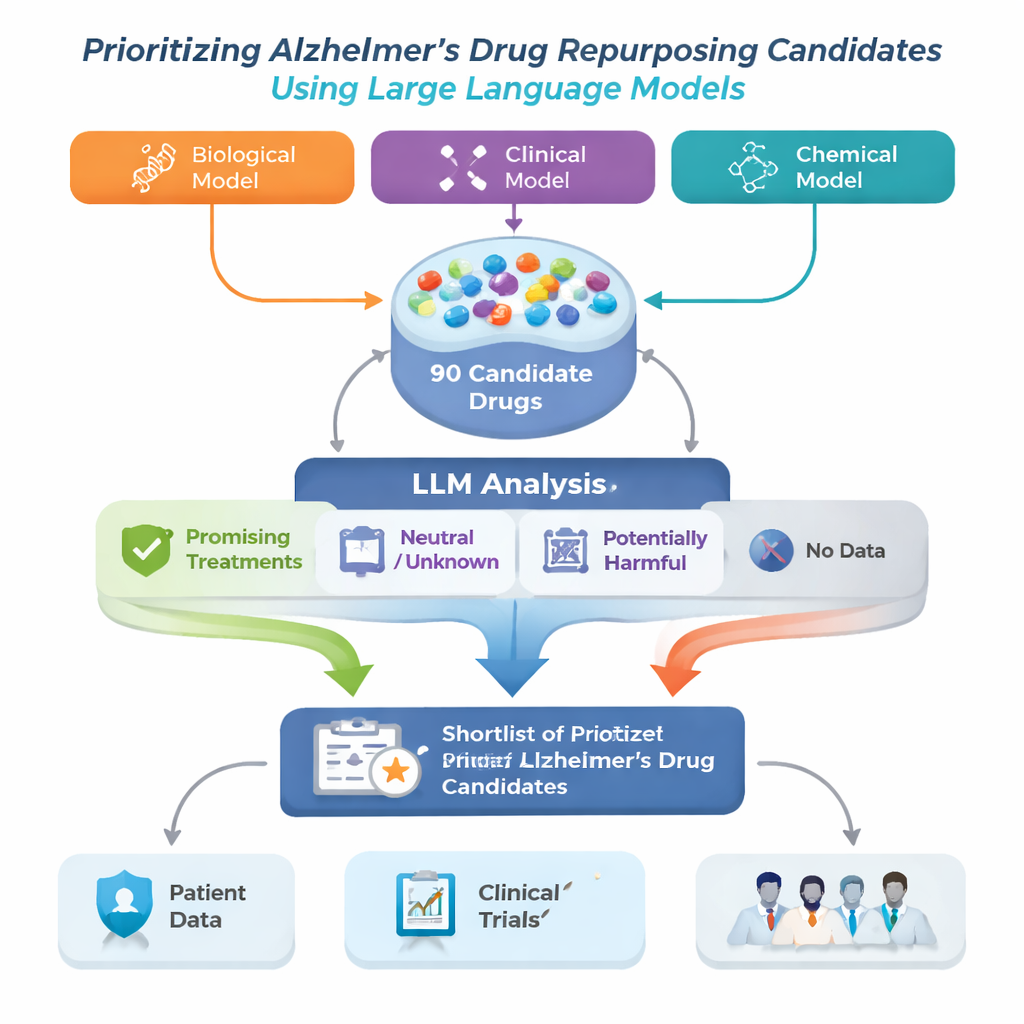
A equipe de pesquisa enfrentou esse problema construindo uma estrutura de Reposicionamento de Medicamentos para Alzheimer que começa com três modelos computacionais avançados diferentes. Cada modelo examina um grande “mapa” biomédico chamado grafo de conhecimento, que liga doenças, medicamentos, genes e outros conceitos médicos, e sugere drogas que podem ajudar no Alzheimer. Como cada modelo percebe padrões de maneira diferente, suas listas não se sobrepõem totalmente. Os autores combinaram as 30 melhores sugestões de cada modelo em um único conjunto de 90 medicamentos candidatos e então usaram um grande modelo de linguagem (LLM) para atuar como um avaliador automatizado, porém cauteloso, lendo estudos publicados sobre cada medicamento e julgando se as evidências pareciam úteis, neutras ou prejudiciais para o Alzheimer.
Como a IA lê a literatura médica
Para cada medicamento candidato, o sistema reuniu até 200 resumos científicos do PubMed além de descrições detalhadas dos medicamentos em um banco de dados farmacêutico. O LLM recebeu instruções para basear seu julgamento apenas no texto apresentado a ele e rotular cada resumo como positivo, neutro ou negativo para o tratamento do Alzheimer. Essas etiquetas foram então transformadas em pontuações simples: a proporção de resumos que foram positivos, neutros ou negativos. Usando dois conjuntos de regras — uma mais rigorosa que exigia evidência positiva clara, e outra mais permissiva que identificava qualquer indício de benefício — a estrutura classificou os medicamentos em quatro grupos: tratamentos promissores, potencialmente prejudiciais, incertos ou neutros, e medicamentos sem nenhum artigo relacionado ao Alzheimer. Este último grupo, embora pouco estudado, pode conter oportunidades especialmente novas.
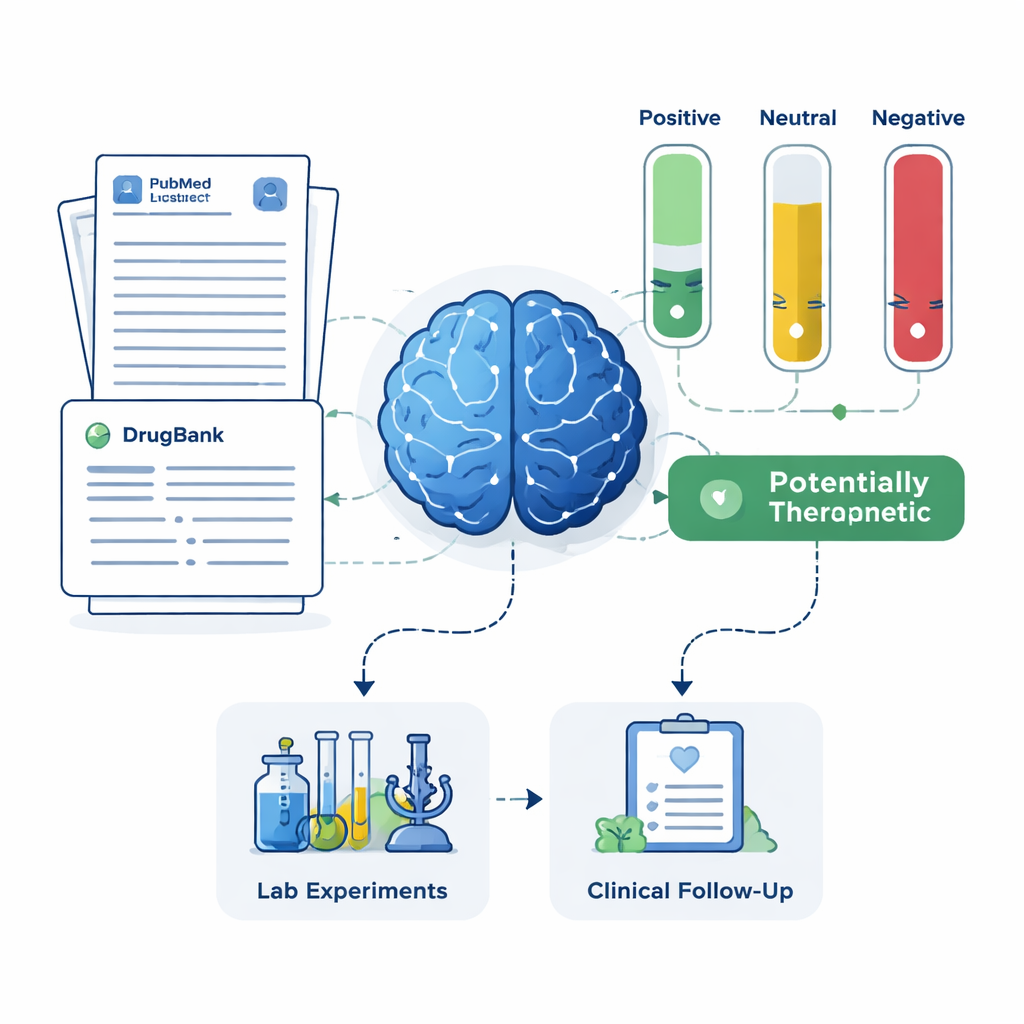
Conferindo com pacientes reais e ensaios clínicos
Para verificar se a lista curta da IA fazia sentido no mundo real, a equipe comparou seus resultados com duas fontes independentes: um grande registro de pacientes com Alzheimer e registros de ensaios clínicos registrados. A estrutura recuperou com sucesso a memantina, um medicamento existente para Alzheimer com sinais protetores fortes em dados de pacientes e extensa história de ensaios, como um candidato de alta prioridade. Ela também destacou drogas como magnésio, minociclina, pimavanserina, testosterona e doxiciclina, que apresentam níveis variados de pesquisa de apoio, mas haviam sido consideradas promissoras por clínicos especialistas. Ao mesmo tempo, o sistema identificou medicamentos cuja literatura sugeria possível dano ou ausência de benefício, recomendando que esses fossem despriorizados ou investigados quanto a efeitos colaterais em vez de tratados como opções terapêuticas.
Das previsões computacionais aos próximos passos práticos
Em termos práticos, essa estrutura atua como um assistente de pesquisa ultrarrápido e cuidadoso que lê milhares de artigos, cruza padrões em grandes bancos de dados médicos e entrega aos especialistas humanos uma lista muito mais curta e melhor organizada de candidatos a medicamentos para Alzheimer em que se concentrar. O estudo mostra que, ao combinar diferentes tipos de IA — modelos baseados em grafos para gerar ideias e um modelo de linguagem para julgar as evidências — os pesquisadores podem encontrar mais rapidamente tanto medicamentos bem respaldados quanto novas opções intrigantes para testar. Embora essa abordagem, por si só, não cure o Alzheimer, ela oferece uma nova maneira poderosa de conectar ideias geradas por computador ao trabalho árduo de experimentos de laboratório e ensaios clínicos, potencialmente acelerando o caminho para tratamentos mais eficazes.
Citação: Li, M., Niu, S., Xu, Y. et al. Bridging the computational-experimental gap: leveraging large language model to prioritize Alzheimer’s therapeutics based on comparison of learning models. npj Health Syst. 3, 20 (2026). https://doi.org/10.1038/s44401-026-00074-3
Palavras-chave: Doença de Alzheimer, reposicionamento de medicamentos, inteligência artificial, modelos de linguagem grandes, grafos de conhecimento