Clear Sky Science · pt
A mutação APP E590D aumenta a geração de peptídeos Aβ e Aη e agrava a tauopatia
Por que essa mutação rara importa
A doença de Alzheimer costuma ser entendida como o acúmulo lento de duas proteínas nocivas, amiloide e tau, no cérebro. A maioria das pessoas desenvolve Alzheimer sem uma causa única e clara, mas algumas famílias carregam alterações genéticas raras que podem deslocar esse equilíbrio de forma drástica. Este artigo examina uma dessas mudanças incomuns no gene da proteína precursora amiloide (APP) e mostra como ela pode turbinar a produção de fragmentos proteicos tóxicos e piorar o processo de emaranhamento conhecido como tauopatia. Entender esse caso raro fornece pistas que podem se aplicar de forma muito mais ampla a como o Alzheimer se inicia e depois acelera.
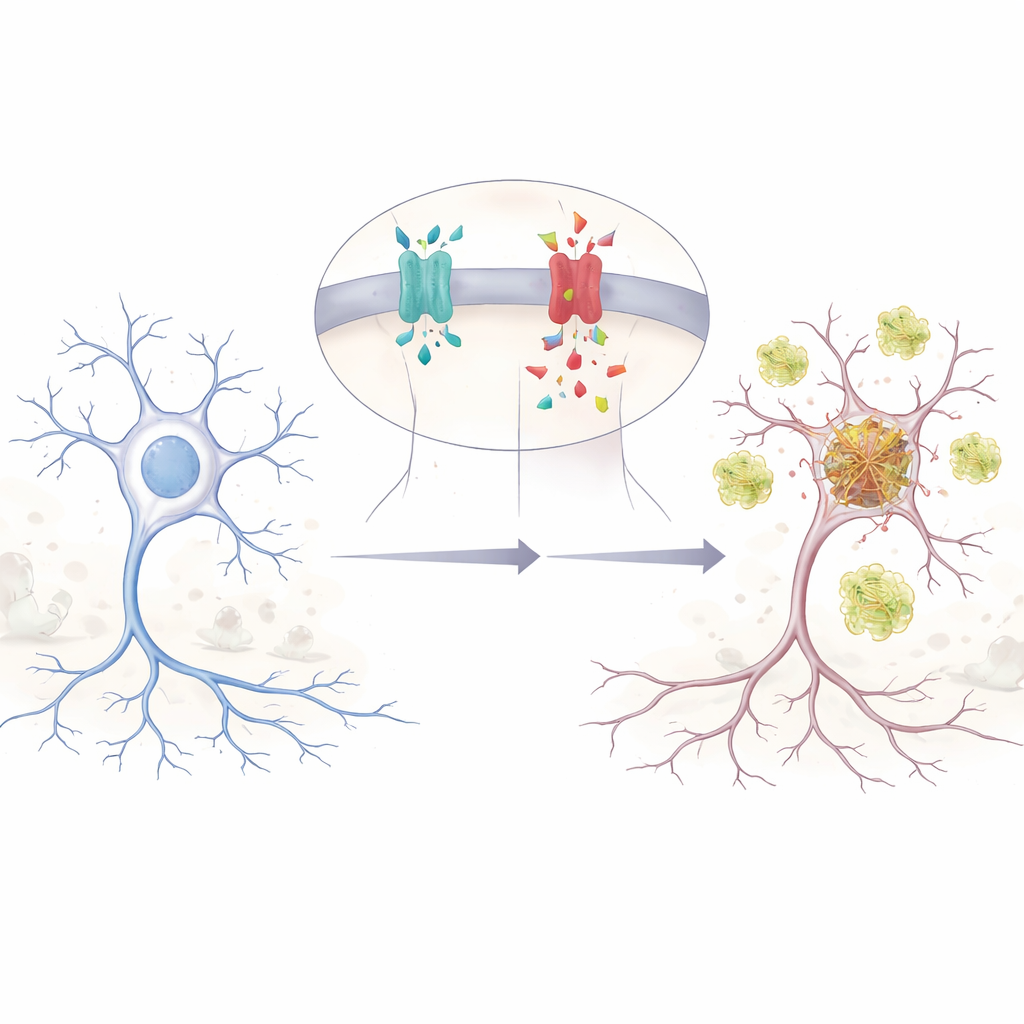
Uma pequena mudança genética com grandes efeitos
Os autores concentram-se em uma mudança de uma única letra no gene APP, chamada E590D na forma principal de APP do cérebro. Essa mutação foi relatada em apenas duas pessoas, ambas com diagnóstico confirmado de Alzheimer em idades relativamente jovens e com problemas de memória e comportamento incomuns e muito precoces. Por ser tão rara, os cientistas não tinham certeza se ela realmente causa a doença ou é apenas uma associada inocente. Para descobrir, a equipe recriou a mutação em células humanas e em neurônios de camundongos, e depois acompanhou como a APP era cortada em seus vários fragmentos. Eles descobriram que a APP mutante produz muito mais beta-amiloide (Aβ), o peptídeo pegajoso associado ao Alzheimer há muito tempo, do que a APP normal quando os níveis são comparados de maneira justa.
Dois peptídeos tóxicos em vez de um
A APP pode ser cortada de várias maneiras, como um tronco sendo fatiado em pontos diferentes. A via clássica do Alzheimer gera Aβ, mas outro corte produz um fragmento menos conhecido chamado Aη. Trabalhos anteriores mostraram que Aη pode prejudicar as conexões entre neurônios e enfraquecer a capacidade do cérebro de reforçar memórias. Em seus experimentos, os pesquisadores constataram que a mutação E590D não apenas aumenta Aβ; ela também eleva fortemente Aη e um fragmento a montante que alimenta ambas as vias. Isso significa que a mutação desloca o processamento da APP para um duplo impacto de peptídeos prejudiciais, potencialmente perturbando circuitos cerebrais mesmo antes de se esperar o aparecimento das placas amiloides clássicas.
Como a mutação acelera o tráfego celular
Para entender por que mais fragmentos tóxicos são produzidos, a equipe estudou onde a APP se localiza e se movimenta na superfície celular. Muitos dos cortes que geram Aβ ocorrem apenas depois que a APP é internalizada pela célula por meio de um processo chamado endocitose. Usando imagens e truques bioquímicos que marcam proteínas na superfície e depois rastreiam sua internalização, os cientistas mostraram que a APP mutante é menos abundante na superfície das células e é captada mais rapidamente para compartimentos internos do que a APP normal. Uma vez dentro desses endossomos iniciais, a APP encontra as enzimas que geram Aβ, e o tráfego alterado parece dar a essas enzimas mais oportunidade de agir. Ao mesmo tempo, o corte no sítio η na superfície também é aumentado, explicando a elevação de Aη.
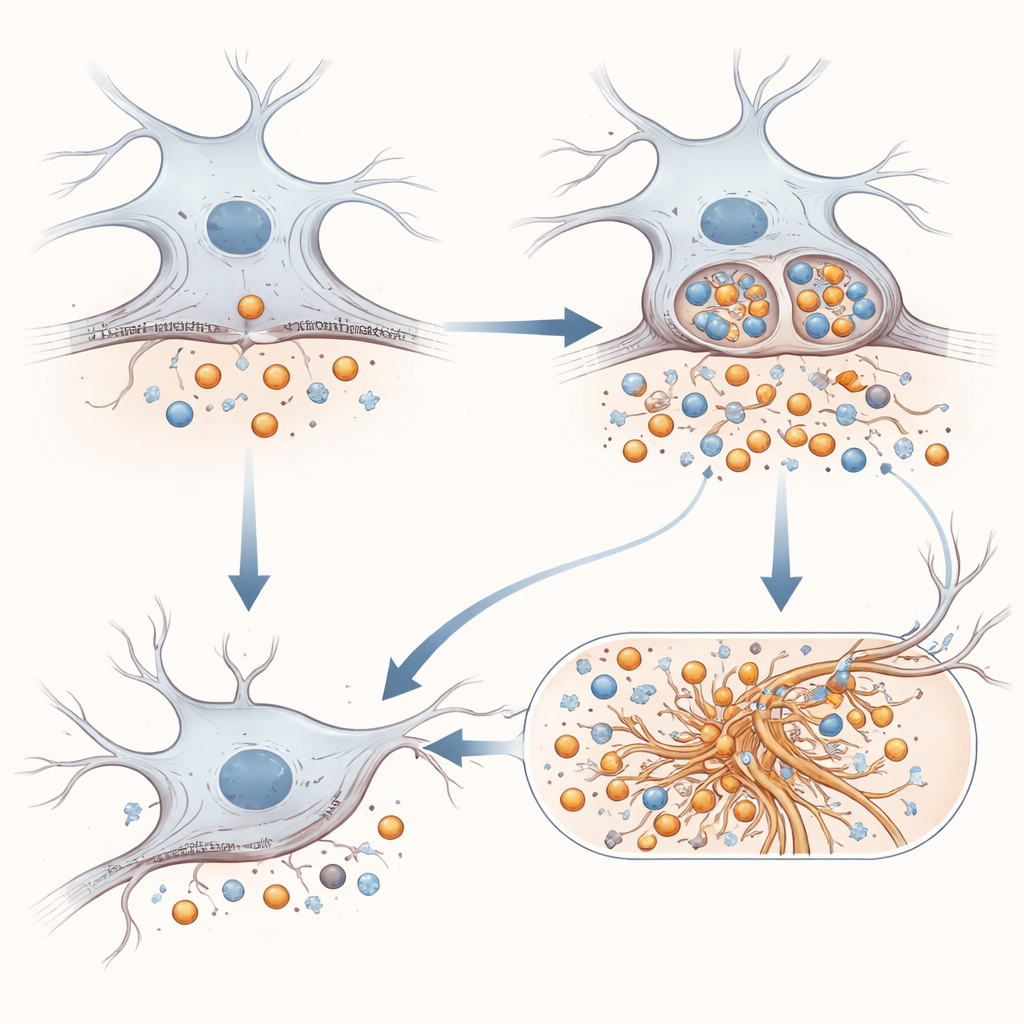
Dos fragmentos proteicos ao emaranhado de tau e à inflamação cerebral
A história não termina nos fragmentos relacionados ao amiloide. Os pesquisadores testaram se a APP mutante influenciaria a tau, a proteína estrutural que forma fibras torcidas em muitas demências. Em modelos celulares que acendem quando sementes de tau induzem a formação de novos agregados, a presença da APP E590D levou a uma agregação mais intensa do que tanto a APP normal quanto a ausência de APP. Em um modelo de camundongo já propenso a problemas de tau, injetar um vírus que expressa a APP mutante no hipocampo piorou os emaranhados de tau e desencadeou uma ativação mais forte de astrócitos e micróglias, as células de suporte e imunes do cérebro. Curiosamente, peças solúveis padrão do amiloide foram difíceis de detectar nesses cérebros de camundongo, mas um fragmento distinto derivado da APP apareceu apenas quando a mutação estava presente, sugerindo um processamento alterado em tecido vivo.
O que isso significa para entender o Alzheimer
Em conjunto, os achados mostram que essa rara mutação da APP não é benigna. Ela empurra o processamento da APP na direção de gerar mais de um peptídeo tóxico, acelera os passos de internalização que favorecem cortes prejudiciais e amplifica o emaranhamento de tau e a inflamação no cérebro. Para leigos, a mensagem principal é que a biologia do Alzheimer não é movida por um único vilão, mas por uma rede de fragmentos proteicos e respostas celulares interagindo entre si. Estudar variantes genéticas tão potentes quanto incomuns oferece uma visão ampliada dessa rede. Neste caso, sugere que as terapias podem precisar considerar tanto o amiloide quanto peptídeos alternativos derivados da APP, como o Aη, bem como seu impacto combinado sobre a tau, em vez de mirar apenas uma via isoladamente.
Citação: Liu, T., Wetzel, L., Roy, D. et al. APP E590D mutation increases generation of Aβ and Aη peptides and exacerbates tauopathy. npj Dement. 2, 21 (2026). https://doi.org/10.1038/s44400-026-00069-9
Palavras-chave: Doença de Alzheimer, proteína precursora amiloide, emaranhados de tau, neuroinflamação, mutação genética