Clear Sky Science · pt
Uma plataforma quantitativa de alto rendimento usando organoides cerebrais humanos dissociados em 2D para modelar neuroinflamação na doença de Alzheimer
Por que infecções podem importar para a perda de memória
A doença de Alzheimer costuma ser descrita como um acúmulo lento de proteínas pegajosas no cérebro, mas evidências crescentes sugerem que infecções podem ajudar a desencadear esse processo. Este estudo explora essa ideia usando pequenos modelos cerebrais cultivados em laboratório para responder a uma pergunta simples: um vírus comum de herpes labial pode desencadear mudanças semelhantes às da doença de Alzheimer em células cerebrais humanas, e um medicamento antiviral pode reverter essas mudanças?
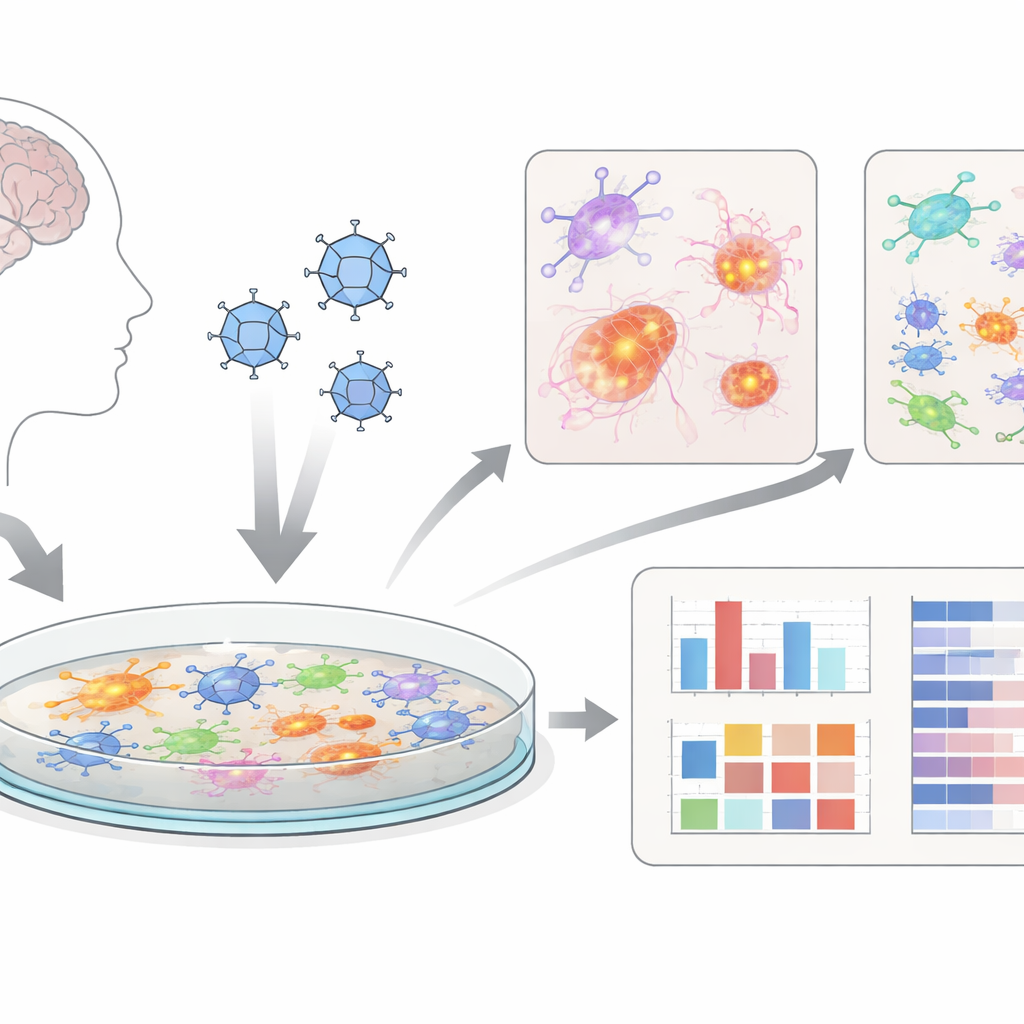
Mini-cérebros em uma placa
Em vez de trabalhar apenas com animais, os pesquisadores usaram “organoides cerebrais” — aglomerados de células semelhantes às do cérebro cultivados a partir de células-tronco humanas. Eles então dissociaram suavemente esses organoides 3D em camadas planas de células cerebrais mistas, incluindo neurônios, células de suporte chamadas astrócitos e microglia com função imune. Essas culturas bidimensionais, que eles chamam de dcOrgs, são mais fáceis de infectar de maneira uniforme e de testar em alto rendimento, o que significa que muitas placas e condições de drogas podem ser examinadas em paralelo. Isso torna o sistema atraente como ferramenta de triagem para novos tratamentos.
Um vírus de herpes labial como faísca
A equipe infectou dcOrgs com o vírus herpes simplex tipo 1 (HSV-1), o vírus responsável pela maioria dos herpes labiais e há muito suspeito de contribuir para demência em algumas pessoas. Eles compararam culturas infectadas com controles tratados com veículo, com culturas tratadas com um antiviral (aciclovir), com culturas expostas a um vírus diferente (influenza A) e com vírus inativado por luz ultravioleta. Usando análise automática de células e sequenciamento de célula única, confirmaram que o HSV-1 infectou robustamente muitos tipos celulares na placa, enquanto o vírus inativado e a influenza produziram padrões de alteração muito diferentes e mais leves.
Mudanças semelhantes às da Alzheimer dentro e entre células
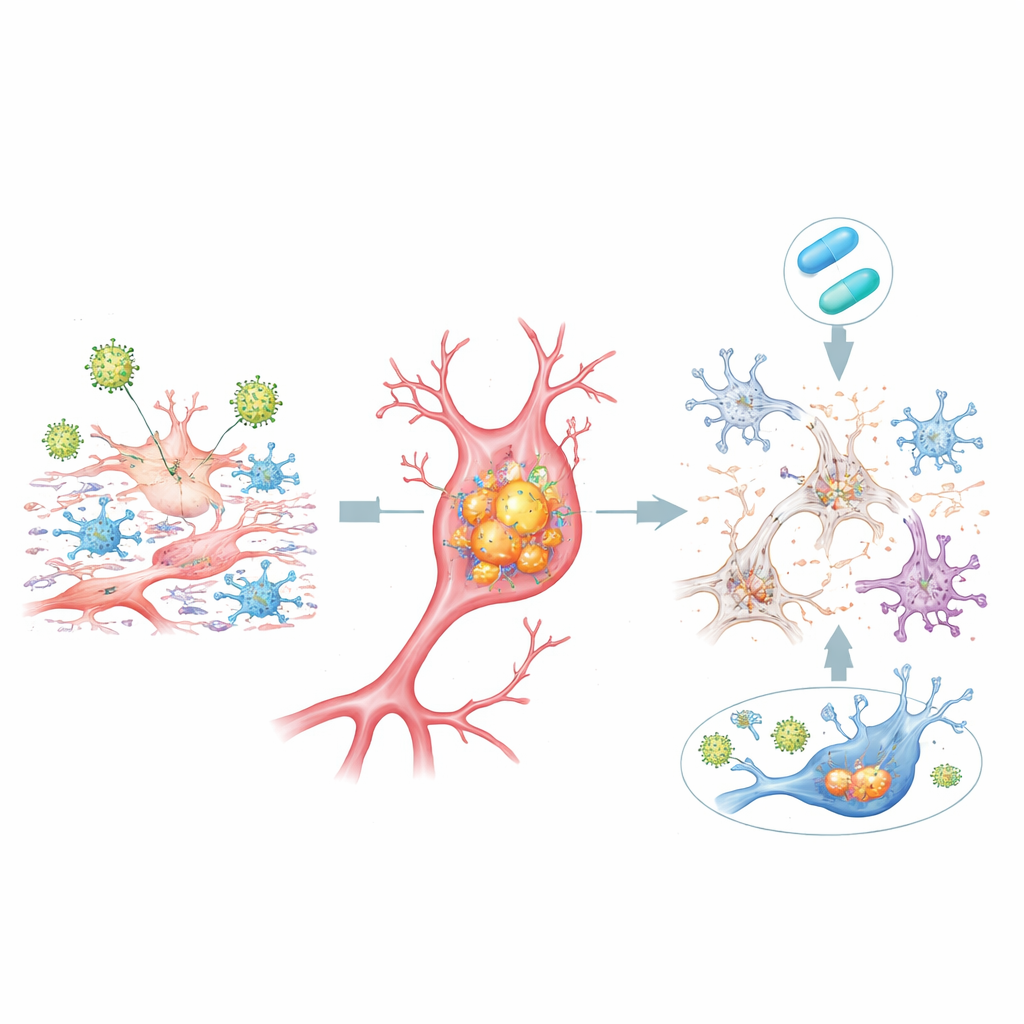
Nas dcOrgs infectadas por HSV-1, muitas células acumularam altos níveis das mesmas formas de proteína vistas em cérebros de pacientes com Alzheimer: beta-amiloide aglutinada dentro das células e múltiplas versões “fosforiladas” da tau, outra proteína chave da doença. Esses acúmulos estavam fortemente ligados às células que continham proteínas virais e foram especialmente pronunciados em células moribundas. Ao mesmo tempo, menos do fragmento beta-amiloide mais longo (Aβ42) foi liberado para o fluido circundante em relação às formas mais curtas, uma mudança que espelha padrões medidos no líquido cefalorraquidiano de pacientes com Alzheimer. As populações celulares também mudaram: o número de neurônios diminuiu, enquanto astrócitos e microglia se expandiram, ecoando a perda neuronal e a inflamação reativa observadas em tecido cerebral de pacientes.
Atividade gênica conecta o modelo ao Alzheimer humano
Quando os pesquisadores examinaram a atividade gênica em todo o genoma, descobriram que a infecção por HSV-1 em dcOrgs ligou e desligou muitos genes previamente associados ao risco de Alzheimer em grandes estudos genéticos humanos. Essas mudanças não foram observadas em culturas mais simples de células-tronco nem em dcOrgs infectadas por influenza, sugerindo uma interação específica entre o HSV-1 e o ambiente misto semelhante ao cerebral. O sequenciamento de célula única revelou que algumas das alterações em genes ligados ao Alzheimer provinham de células que haviam sido expostas ao vírus, mas continham pouco ou nenhum material genético viral, sugerindo que sinais de vizinhos infectados podem espalhar programas inflamatórios prejudiciais.
O que o tratamento antiviral pode e não pode consertar
Adicionar o antiviral aciclovir logo após a exposição ao HSV-1 reduziu a expressão de genes virais, atenuou muitas respostas inflamatórias, diminuiu o acúmulo de beta-amiloide e tau tóxicos dentro das células e restaurou parcialmente o equilíbrio entre os diferentes tipos celulares. Para uma fração substancial dos genes associados ao Alzheimer, seus níveis de atividade voltaram em direção ao normal. No entanto, nem todas as alterações foram reversíveis: um grupo considerável de genes humanos permaneceu inalterado ou até mais perturbado pelo tratamento, especialmente quando o medicamento foi menos eficaz em bloquear genes virais tardios. Isso ressalta que, embora interromper a replicação viral possa ajudar, pode não reverter completamente a cascata biológica uma vez iniciada.
O que isso significa para a compreensão do Alzheimer
Para um leitor não especialista, a conclusão é que um vírus humano de herpes labial, atuando dentro de uma mistura realista de células cerebrais humanas, pode rapidamente produzir muitos elementos característicos da doença de Alzheimer — desde aglomerados proteicos e neurônios moribundos até padrões genéticos já observados em pacientes. O sistema baseado em organoides planos desenvolvido aqui é rápido, quantitativo e escalável, tornando-se um campo de testes poderoso para antivirais e outras terapias destinadas a acalmar a inflamação cerebral. Embora isso não prove que infecções por herpes causem Alzheimer em todos os pacientes, fortalece o argumento de que, para um subconjunto de pessoas, infecções virais crônicas ou reativadas podem ser uma peça importante do quebra-cabeça — e um alvo potencial para prevenção.
Citação: Olson, M.N., Barton, N.J., Feng, L. et al. A high-throughput, quantitative platform using 2D dissociated human cerebral organoids to model neuroinflammation in Alzheimer’s disease. npj Dement. 2, 20 (2026). https://doi.org/10.1038/s44400-026-00066-y
Palavras-chave: Doença de Alzheimer, vírus herpes simplex, organoides cerebrais, neuroinflamação, terapia antiviral