Clear Sky Science · pt
Codificando arestas funcionais em grafos para modelar relações espacialmente variáveis no microambiente tumoral
Por que mapear o entorno do câncer importa
O câncer não cresce isoladamente. Células tumorais vivem em um bairro movimentado de células imunes, células de suporte, vasos sanguíneos e sinais químicos, todos compartilhando o mesmo espaço. A maneira como esses vizinhos estão organizados e a intensidade com que influenciam uns aos outros pode determinar se um câncer se espalha, responde ao tratamento ou permanece controlado. Este artigo apresenta o SPIFEE, uma nova estrutura de inteligência artificial que transforma imagens microscópicas e mapas moleculares de tumores em redes, ajudando pesquisadores a identificar quais interações entre células e vias estão mais associadas ao tipo de doença e ao desfecho do paciente.
Transformando tecido em mapa de rede
Estudos modernos sobre câncer conseguem medir muito mais do que a aparência de um tumor ao microscópio. Alguns métodos destacam dezenas de proteínas em células individuais, outros produzem lâminas coloridas detalhadas da estrutura tecidual, e ferramentas mais recentes registram quais genes estão ativos em milhares de pontos ao longo de uma fatia tumoral. O SPIFEE trata tudo isso como vistas diferentes do mesmo entorno. Ele representa cada amostra como um grafo: nós correspondem a entidades-chave no microambiente tumoral — como tipos celulares, padrões visuais do tecido ou vias moleculares — enquanto arestas capturam como essas entidades interagem no espaço. De maneira crucial, o SPIFEE não reduz uma interação a um único número como “distância”. Em vez disso, cada aresta armazena uma pequena curva descrevendo quão fortemente duas entidades se misturam ou se repelam ao longo de uma faixa de distâncias, preservando um detalhe espacial muito mais rico.
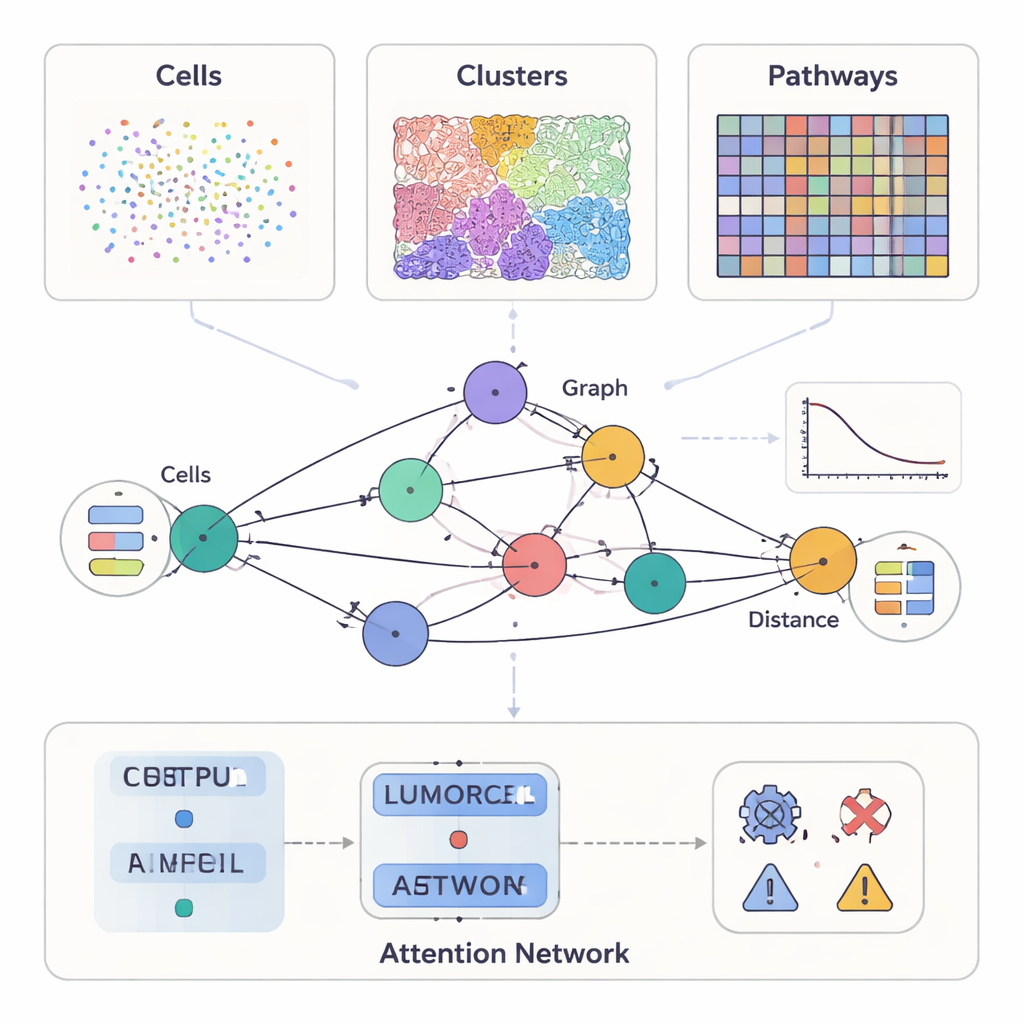
Uma lente flexível para muitos tipos de dados do câncer
Os autores testaram o SPIFEE em vários grandes conjuntos de dados independentes sobre câncer, abrangendo diferentes tecnologias e escalas. Em amostras pancreáticas marcadas com imunofluorescência multiplex, cada nó do grafo representava um tipo celular, e as características dos nós vinham de sequenciamento de RNA de célula única que resumiam como essas células tendem a se comunicar. Em lâminas de câncer de pulmão coradas pelo método rotineiro de hematoxilina e eosina, os nós representavam padrões visuais recorrentes do tecido, descobertos automaticamente por um sistema de aprendizado auto-supervisionado. Em um terceiro cenário, lâminas padrão de câncer de pulmão foram convertidas por uma ferramenta de deep learning em transcriptômica espacial virtual, e os nós do SPIFEE representaram vias moleculares como hipóxia, sinalização por estrogênio ou JAK–STAT, com características derivadas da atividade gênica. Em todos esses contextos, a mesma estrutura conseguiu ingerir diferentes tipos de nós e ainda construir grafos espaciais comparáveis.
Encontrando as interações que distinguem desfechos clínicos
Uma vez que o SPIFEE constrói um grafo, ele o processa por meio de uma rede de atenção em grafos, um tipo de rede neural que aprende não apenas a prever um desfecho — como subtipo de câncer, risco de sobrevida ou doença versus inflamação não cancerosa —, mas também a destacar quais arestas foram mais importantes para essa previsão. Em tecido pancreático, o SPIFEE distinguiu pancreatite crônica de adenocarcinoma ductal pancreático com maior precisão do que métodos anteriores baseados em grafos. O modelo concentrou-se de maneira consistente em interações envolvendo células epiteliais (semelhantes a tumorais) e células T regulatórias, células apresentadoras de antígeno e células T auxiliares, apontando para um microambiente imunossupressor mais proeminente no câncer do que na inflamação. Em lâminas de adenocarcinoma pulmonar, o SPIFEE identificou padrões estroma–tumor específicos cujas interações se correlacionaram com sobrevida melhor ou pior, sugerindo que as “zonas de fronteira” entre tumor e tecido de suporte codificam pistas prognósticas importantes que análises padrão podem perder.
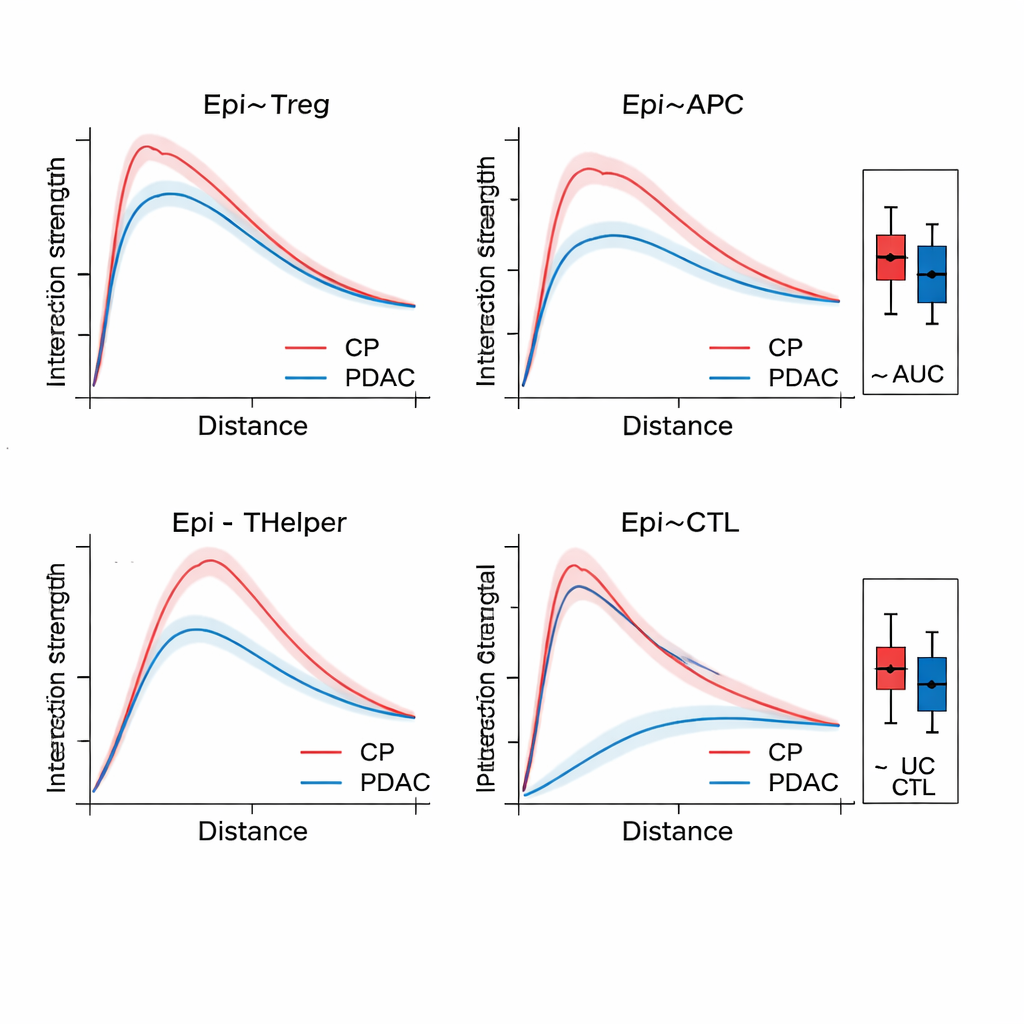
Lendo a comunicação molecular a partir de lâminas de rotina
Talvez de forma mais notável, o SPIFEE pôde inferir interações de vias significativas a partir de imagens patológicas comuns depois que elas foram traduzidas em mapas preditos de atividade gênica. Ao tratar vias como nós e sua coocorrência espacial como arestas funcionais, o método destacou pares como hipóxia com EGFR ou JAK–STAT com PI3K — combinações já conhecidas por promover evasão imune e resistência a medicamentos no câncer de pulmão. Também destacou vias relacionadas ao estrogênio em adenocarcinoma pulmonar e certas vias imunes e de estresse em tumores escamosos, achados que se alinharam com padrões observados em sequenciamento de RNA em massa e em um conjunto de dados independente de transcriptômica espacial real. Isso sugere que, mesmo quando medidas moleculares são aproximadas, padrões espaciais em lâminas de rotina ainda carregam sinais recuperáveis sobre como vias-chave interagem em tumores vivos.
O que isso significa para o cuidado futuro do câncer
Para um público não especializado, a mensagem central é que o SPIFEE oferece uma nova forma de ler a “vida social” das células cancerosas diretamente a partir de imagens e mapas moleculares. Ao codificar como as relações mudam com a distância em vez de achatá-las em pontuações únicas, e ao usar redes neurais baseadas em atenção para ranquear quais interações são mais relevantes, a estrutura pode descobrir combinações de células, padrões teciduais e vias que distinguem tipos de câncer e predizem sobrevida. Embora essas descobertas ainda precisem de validação biológica e clínica, abordagens como o SPIFEE apontam para um futuro em que amostras tumorais rotineiras podem fornecer não apenas instantâneos estáticos, mas mapas dinâmicos de pontos críticos de interação que ajudam a orientar o diagnóstico, a estratificação de risco e, eventualmente, escolhas de terapias personalizadas.
Citação: Tsang, A.P., Krishnan, S.N., Kulkarni, R. et al. Encoding functional edges in graphs to model spatially varying relationships in the tumor microenvironment. npj Artif. Intell. 2, 27 (2026). https://doi.org/10.1038/s44387-026-00075-5
Palavras-chave: microambiente tumoral, transcriptômica espacial, redes neurais em grafos, patologia do câncer, interações célula-célula